Clear Sky Science · zh
以CPF‑CF终止的snoRNA通过由mRNA守护蛋白介导的监视机制穿梭于细胞质
微小RNA向意外绕行的一瞥
在每个细胞内,蛋白质的生成依赖精确的分子协同。这个舞蹈的关键一环由小核仁RNA(snoRNA)控制,它们帮助塑造细胞的核糖体——构建蛋白质的机器。该研究揭示,一些这种微小的向导出人意料地离开细胞核,短暂进入细胞质然后返回,这一切都与它们产生时的终止方式有关。理解这一隐蔽的运输路径有助于阐明细胞如何维持RNA质量并保护遗传信息。
更近距离观察细胞的RNA助手
snoRNA是短小的RNA分子,充当向导,定向对其他RNA(尤其是构成核糖体的RNA)进行化学修饰。在酵母细胞中,大多数snoRNA在细胞核内产生并被认为终生留在核内,与特定蛋白形成稳定复合体,成为执行核糖体RNA修饰的snoRNP。然而,早期研究曾检测到snoRNA与通常参与将信使RNA(mRNA)输出核外的蛋白发生接触。这一令人费解的观察引发疑问:snoRNA是否有时会前往细胞质,如果会,原因何在?
发现snoRNA在移动
通过重新审视来自精心分离的核与细胞质分馏的RNA测序数据,作者发现许多snoRNA确实存在于正常酵母细胞的细胞质中,其丰度与典型mRNA相当。当他们使关键的输出因子Mex67和Xpo1失活时,细胞质中的snoRNA池缩小,而未成熟的、携带3′延长序列的snoRNA前体在细胞核中积累。使用荧光探针的显微镜成像证实了这种转变:通常出现在核仁并在细胞质中呈微弱信号的snoRNA,在阻断输出时变为强烈的核内信号。这些发现表明,一部分snoRNA(通常仍带有末端额外序列)是被主动运输出核而非样品污染或被动泄漏。
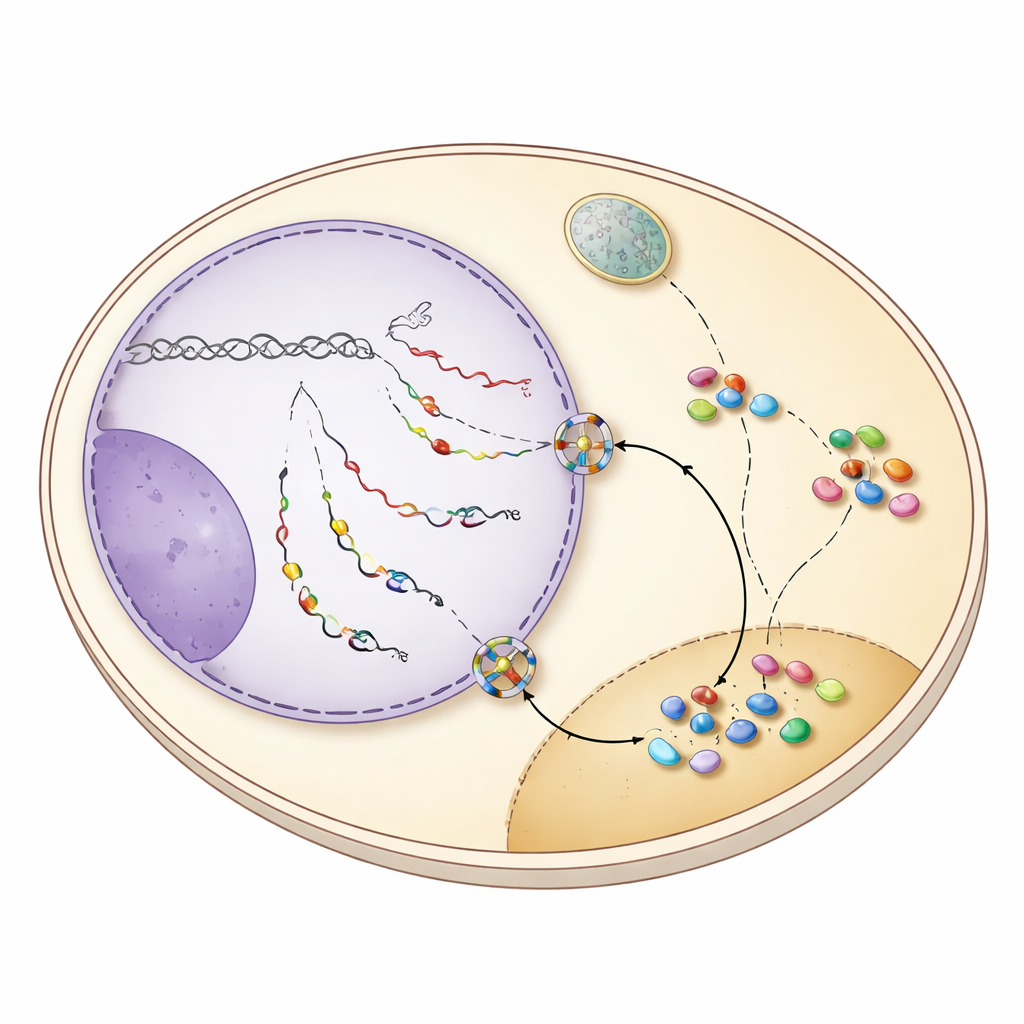
将snoRNA送出的守护蛋白开关
这种穿梭行为的关键在于snoRNA转录的终止方式。在酵母中,大多数snoRNA通常由称为NNS的系统从转录机器上切离,这会留下短尾巴并在核内迅速修剪。然而,许多snoRNA基因也包含被第二套系统CPF‑CF识别的备用终止信号,CPF‑CF以完成mRNA的终止并添加长的poly(A)尾而著称。当NNS终止失败时,snoRNA转录本会延伸到下游的CPF‑CF位点并获得更长的尾巴。这种改变的末端招募了一组“守护”蛋白——例如Hrp1和Nab2——它们既检查加工是否正确,又同时吸引输出因子Mex67。研究表明,当snoRNA由CPF‑CF完成时,守护蛋白与Mex67协同工作,将这些带尾的snoRNA通过核孔送到细胞质中。
往返车票与质量控制
snoRNA一旦进入细胞质,并不会无人照看。它们仍被Lsm蛋白组成的保护环和因子Lhp1包裹,屏蔽脆弱的RNA末端。这些特征使两个输入受体Cse1和Mtr10能够识别正在穿梭的snoRNA并将其带回细胞核。当作者使这些输入因子或Lsm环失活时,未成熟的snoRNA在细胞质中积累,证实了该机制介导其返回。回到细胞核后,长尾被核外切体修剪,核心snoRNP蛋白完成组装,成熟复合体重新定位到核仁。重要的是,经历这一绕行的snoRNA仍然完全功能性:作为模型的snoRNA snR13在被CPF‑CF终止并经由细胞质后,仍能对核糖体RNA执行其特定的化学修饰。
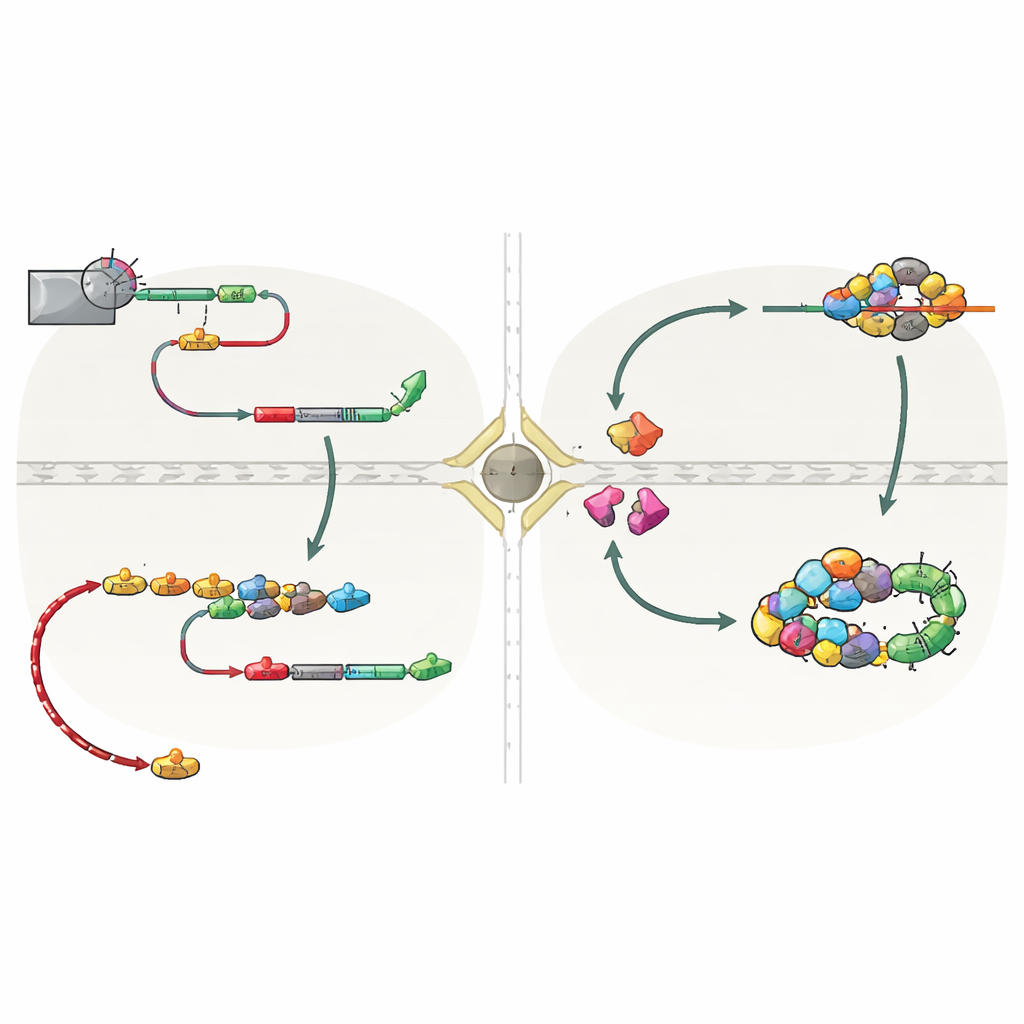
为何这条隐蔽通路重要
这项工作表明,snoRNA的旅行并非个别现象,而是由转录终止方式控制的内置备用途径。当主要的NNS系统被削弱时——例如在特定的细胞周期阶段——下游的CPF‑CF信号可救援snoRNA的产生。这既避免了已合成RNA的浪费,也防止了可能干扰邻近基因并损伤DNA的失控转录。作者还发现在人类细胞中存在类似备用机制的线索,独立编码的snoRNA也可在相关位点获得poly(A)尾。简而言之,该研究表明,snoRNA基因末端选择的“停止信号”决定了该RNA是静默地在核内成熟,还是在守护蛋白的监视下短暂外出再返回。这种以转录终止驱动的监视机制有助于保持细胞RNA景观的灵活性与安全性。
引用: Yu, F., Zaccagnini, G., Duan, Y. et al. CPF-CF-terminated snoRNAs shuttle through the cytoplasm via an mRNA guard protein-mediated surveillance mechanism. Nat Commun 17, 2328 (2026). https://doi.org/10.1038/s41467-026-70373-8
关键词: snoRNA, RNA质量控制, 核输出, 转录终止, 酵母遗传学