Clear Sky Science · zh
靶向Tudor结构域含蛋白9的siRNA纳米颗粒通过促进中性粒细胞铜致死缓解临床前模型中的铜绿假单胞菌肺损伤
将机体的第一响应者转变为精确的盟友
由细菌Pseudomonas aeruginosa引起的肺炎治疗难度大,尤其是在免疫功能低下或肺组织损伤的患者中。该研究探索了一种新方法,旨在帮助机体自身的免疫细胞——中性粒细胞——更安全、更有效地清除这些感染。通过将微小的遗传物质包装在专门设计的纳米颗粒中递送,研究者重新编程中性粒细胞,使其在恰当的时间和部位死亡,从而在继续抗菌的同时减轻肺损伤。
为何这种细菌如此难以击退
Pseudomonas aeruginosa是一种高度适应性的病原体,能抵抗多种抗生素并形成保护性生物膜,使肺部感染难以控制。对此,机体会大量动员中性粒细胞作为第一响应者。尽管它们对杀灭微生物至关重要,但中性粒细胞过度聚集并在肺中延迟清除,可能适得其反,导致肿胀、液体积聚和组织破坏。目前的治疗大多侧重直接攻击细菌,而针对安全调节免疫反应的手段仍然有限。
中性粒细胞中的一条意外基因线索
研究团队首先检测来自肺炎患者的肺液中分离的中性粒细胞,将感染Pseudomonas的样本与其他类型肺炎或无肺炎的样本进行比较。通过RNA测序,他们发现一个名为TDRD9的基因在来自Pseudomonas患者的中性粒细胞中被强烈激活。TDRD9此前主要与精子发育相关,而非肺病,但其升高在人体样本和被感染的小鼠中均一致出现。这表明TDRD9可能在严重细菌性肺部感染中驱动有害的中性粒细胞行为。
让中性粒细胞的死亡为愈合服务
中性粒细胞在完成任务后通常以受控方式死亡,从而使炎症得以消退。研究者关注一种新近识别的细胞死亡形式——铜致死(cuproptosis),其依赖细胞内的铜。在被Pseudomonas感染的小鼠和人类中性粒细胞中,他们发现TDRD9帮助保护中性粒细胞免受铜致死,使其在发炎的肺中存活更久。当有意降低TDRD9水平时,中性粒细胞更易发生这种与铜相关的死亡,整体肺损伤得到改善:肺液减少、炎性分子降低、细菌计数下降。机制实验显示,TDRD9通过涉及PD-L1、CD80及p38 MAPK通路的信号链发挥作用,p38 MAPK是已知的细胞内应激反应调控者。
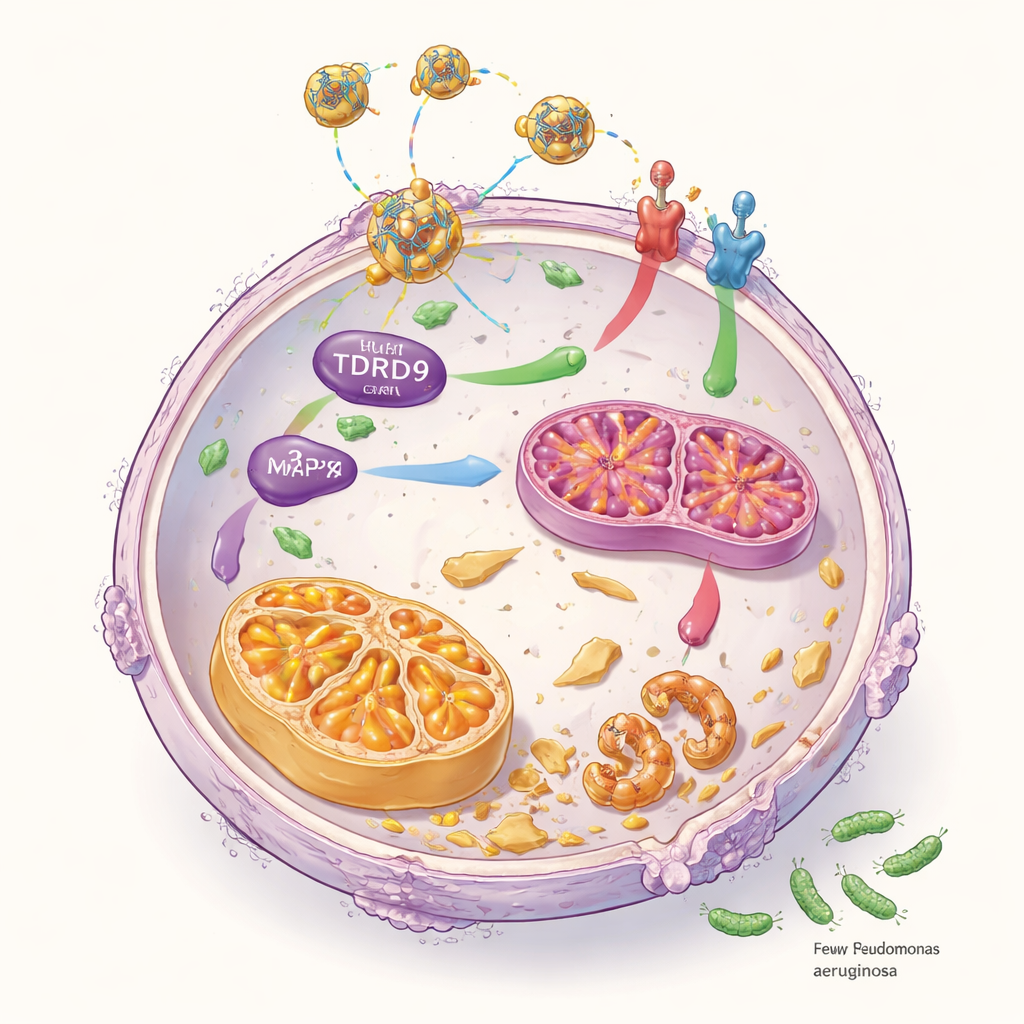
用于靶向基因沉默的智能纳米颗粒
为将这些发现转化为潜在疗法,科学家构建了一种基于透明质酸包被的纳米颗粒递送系统,透明质酸是一种可通过表面受体CD44帮助颗粒定位中性粒细胞的多糖。每个纳米颗粒内装有特异性阻断TDRD9的小干扰RNA(siRNA)。在体外实验中,这些颗粒可被人类中性粒细胞有效摄取,显著降低TDRD9水平。在感染小鼠中,经静脉注射靶向TDRD9的纳米颗粒可减少细菌负荷、肺部肿胀和炎性信号,同时未见明显的肝肾毒性。中性粒细胞表现出与增强铜致死和更平和炎症环境相一致的变化。
将类人肺带入实验室
为了弥合动物模型与人类疾病之间的差距,团队还培养了三维人类肺类器官——由非肿瘤性肺组织衍生的微小类组织结构。暴露于Pseudomonas后,这些类器官出现结构损伤、炎症和细胞死亡。用靶向TDRD9的纳米颗粒处理可抑制细菌生长、降低炎性分子并减少细胞死亡迹象,表明该方法可能有助于保护人类肺组织免受感染引发的损伤。
这对患者可能意味着什么
总体而言,这项研究表明,通过精确递送的siRNA纳米颗粒抑制中性粒细胞中的TDRD9通路,可以促进一种受控的细胞死亡形式,帮助清除过量的中性粒细胞并减轻严重Pseudomonas感染期间的肺损伤。这一策略不是单纯增加抗生素用量去消灭细菌,而是微调免疫反应本身。尽管仍需更多工作来确认在人群中的长期安全性和有效性,但研究结果指向了这样一种未来:智能纳米颗粒将过度活跃的免疫细胞从损伤源转化为愈合的伙伴。
引用: Zhang, W., Li, H., Jia, H. et al. Tudor domain-containing protein 9-targeting siRNA nanoparticles alleviate Pseudomonas aeruginosa lung injury in preclinical models by promoting neutrophil cuproptosis. Nat Commun 17, 2277 (2026). https://doi.org/10.1038/s41467-026-70349-8
关键词: 铜绿假单胞菌肺炎, 中性粒细胞, 纳米颗粒疗法, siRNA递送, 铜致死(cuproptosis)