Clear Sky Science · zh
通过GTP酶激活蛋白TBC1D9B及其结合伙伴TMEM55B对溶酶体功能的调控
细胞回收中心如何保持平衡
在我们每个细胞内都有被称为溶酶体的小囊,其既像回收中心又像生长的控制枢纽。当它们运行良好时,损耗的组件被分解并循环利用;当它们失效时,废物堆积,会引发包括神经退行性疾病和癌症在内的疾病。本研究揭示了两种鲜为人知的蛋白如何帮助在溶酶体的游走、支持生长状态与聚集、清除废物模式之间切换,阐明了细胞如何在丰饶与饥荒之间做出适应。
在细胞内移动回收中心
溶酶体并非固定不动。它们沿着细胞内部的轨道移动,由一组分子马达向外牵引,另一组向内拉拽。溶酶体在细胞中的位置很重要:当营养充足时,溶酶体向细胞外围扩散,帮助支持生长信号;当营养匮乏时,它们回撤到细胞中心,酸性增强,并加大对细胞物质的分解。一个名为ARL8的小型开关样蛋白已知能推动溶酶体向外,但此前尚未有人确定专门的刹车系统来制约它。作者推测,这样的刹车对让细胞在饥饿时迅速转入节约模式至关重要。
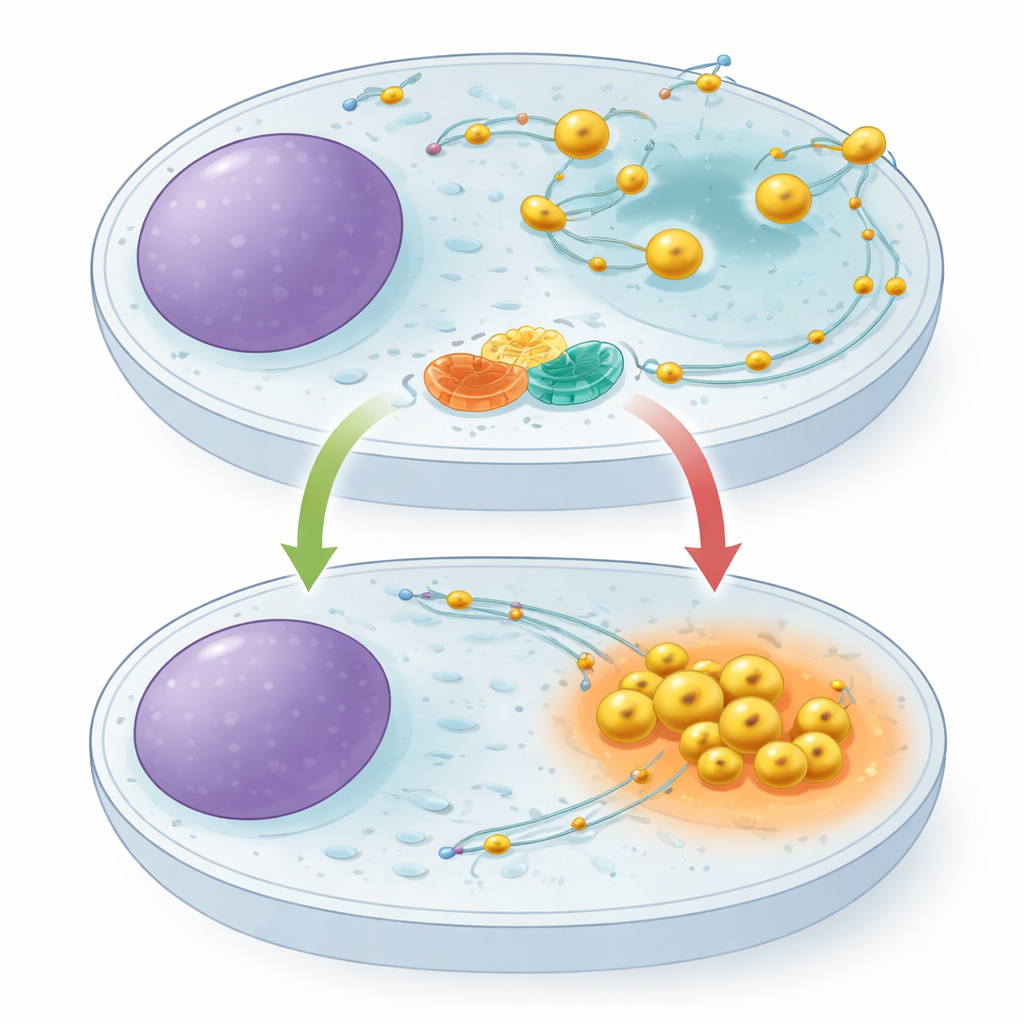
位于溶酶体表面的一种分子伙伴关系
通过蛋白质“捕捞”技术和质谱分析,研究人员发现名为TBC1D9B的蛋白可附着于一种名为TMEM55B的溶酶体膜蛋白上。TMEM55B横跨溶酶体外壳,而TBC1D9B大部分可溶并可停靠到膜上。研究组显示这两者形成直接复合物:纯化的TBC1D9B在试管中能结合TMEM55B的暴露部分,带标签的蛋白互相从细胞提取物中拉下对方。对蛋白片段的精细映射表明,TBC1D9B的若干区域与TMEM55B接触,将TBC1D9B定位到溶酶体表面,同时并不阻碍其催化活性所在的部分。
当刹车失灵,溶酶体失控
为探明这一伙伴关系的功能,作者使用CRISPR编辑从人类细胞中去除TMEM55B或TBC1D9B。在两种情况下,溶酶体不再在细胞核周围聚集,而是散布到细胞边缘并沿轨道移动得更快,模拟处于持续饱食状态的细胞。重新引入正常的TBC1D9B可恢复正确定位,而缺失催化能力的变体则不能,表明其酶学活性是必需的。饥饿处理时,对照细胞将溶酶体拉向内侧并增强其消化能力,这由关键酶活性增加和测试货物的分解增强所示。缺失TMEM55B或TBC1D9B的细胞无法做到这一点:它们的溶酶体保持在周边,且对饥饿的降解反应减弱。自噬——细胞吞噬并降解受损成分的过程——也受损,自噬报告分子的处理效率降低,并伴随适配蛋白p62的积累。
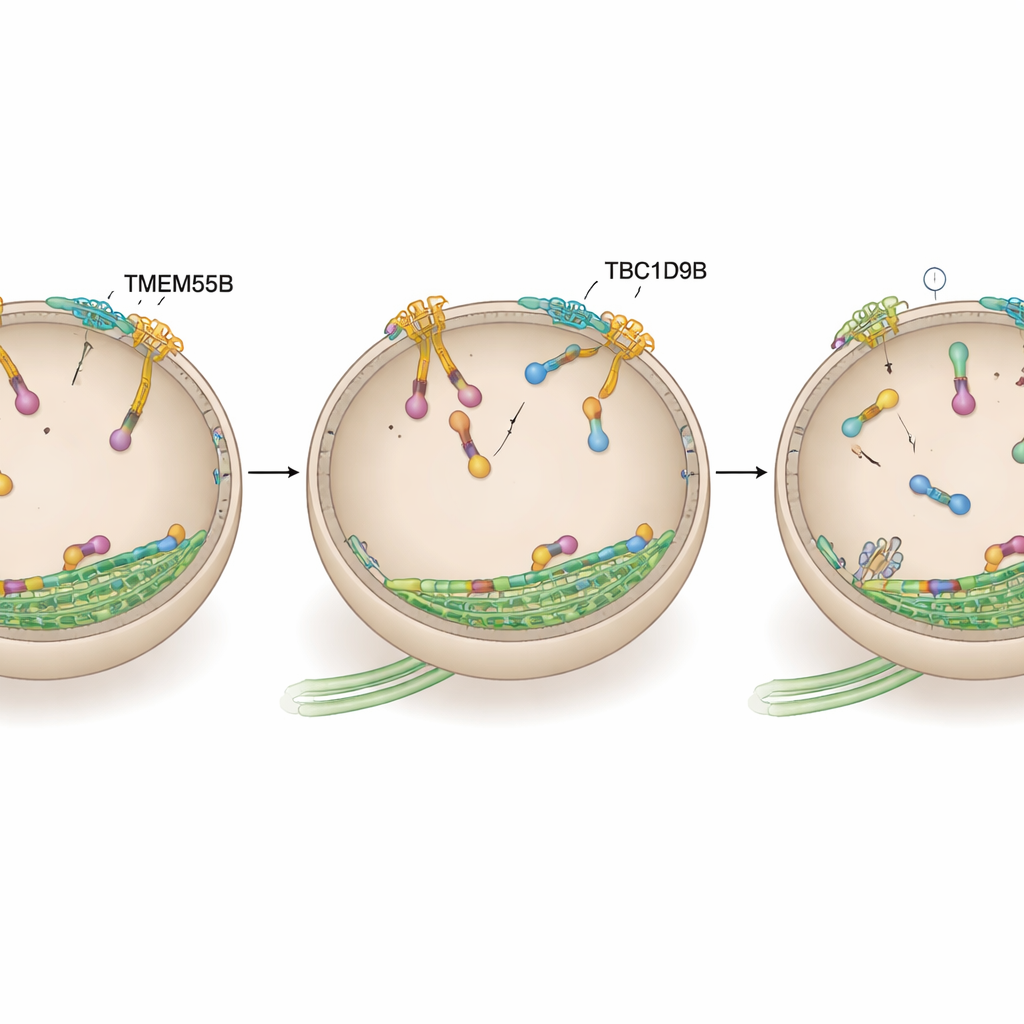
关闭溶酶体马达
研究组随后探查TBC1D9B是否通过直接作用于推动外移的马达开关ARL8起作用。利用在人类神经元中的近距离标记以及在细胞系和纯化蛋白中的结合测试,他们显示TBC1D9B选择性地结合ARL8B变体的活性(GTP结合)形式,但不结合其非活性形式或密切相关的ARL8A。结构建模预测TBC1D9B中的关键残基与ARL8B的GTP口袋接触。在生化测定中,TBC1D9B加速了ARL8B上GTP的水解,有效地将该蛋白从“开”态转换为“关”态;缺失这些残基的TBC1D9B突变体则不再具有此功能。与此一致,缺失TMEM55B或TBC1D9B的细胞在溶酶体上显示出更多的ARL8B,而过表达TBC1D9B则将溶酶体拉回中心,类似于降低ARL8B活性的效果。
细胞清洁维护的新调节旋钮
最后,作者检验这一ARL8B刹车是否解释了缺失TBC1D9B时观察到的细胞变化。当ARL8B被耗减时,溶酶体无论TMEM55B或TBC1D9B是否存在都保持靠近细胞核的聚集状态,且TBC1D9B缺失引起的自噬缺陷在很大程度上被抵消。综合数据支持这样一种模型:TMEM55B将TBC1D9B招募到溶酶体上,在那里它使ARL8B失活,从而允许溶酶体从分散的、支持生长的状态转变为集中化的、以消化为中心的状态。对非专业读者而言,这意味着该研究发现了细胞用以决定何时更积极回收的一个重要调节旋钮,这一过程与脑内废物堆积相关疾病、代谢以及癌症等有着潜在联系。
引用: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
关键词: 溶酶体, 自噬, 细胞信号, 细胞器运输, 神经退行性疾病