Clear Sky Science · zh
在雄性小鼠中,星形胶质细胞内的NF-κB激活会损害创伤性脑损伤后的伤口愈合
为什么脑挫伤并非总能干净愈合
当有人遭受头部撞击时,外部可见的伤口只是部分情形。深处脑内发生的复杂修复反应可能决定一个人是能良好康复,还是出现长期的认知、情绪或运动问题。本研究在雄性小鼠中揭示了支持细胞——星形胶质细胞内的一个关键应激通路如何将正常的愈合反应转变为在创伤性脑损伤后反而加剧损伤的过程。
大脑隐蔽的第一响应者
星形胶质细胞呈星状,围绕神经元和血管,帮助维持大脑内部环境的稳定。头部受伤后,它们会迅速改变形态与功能,围绕损伤区形成屏障并协助组织重建。研究者将注意力集中在这些细胞内的一个分子开关——NF-κB上,该分子在多种组织炎症控制中已广为人知。他们探究在类似常见人类脑震荡和挫伤的闭合头部损伤后,这一开关是帮助还是损害大脑的愈合能力。
受撞击后被点亮的应激开关
通过分析小鼠损伤后脑组织的基因活性,团队发现与炎症和NF-κB信号相关的基因在创伤后,尤其在受伤后3到7天(继发性损伤加剧的时期)显著上调。使用报告小鼠,他们显示NF-κB的激活并非在全脑弥漫,而是集中在冲击部位周围。那里,NF-κB在小胶质细胞(大脑的免疫哨兵)以及构成伤口边界的星形胶质细胞中尤其活跃。该时空分布提示星形胶质细胞内的NF-κB可能是调节大脑如何组织瘢痕和控制免疫反应的关键因子。
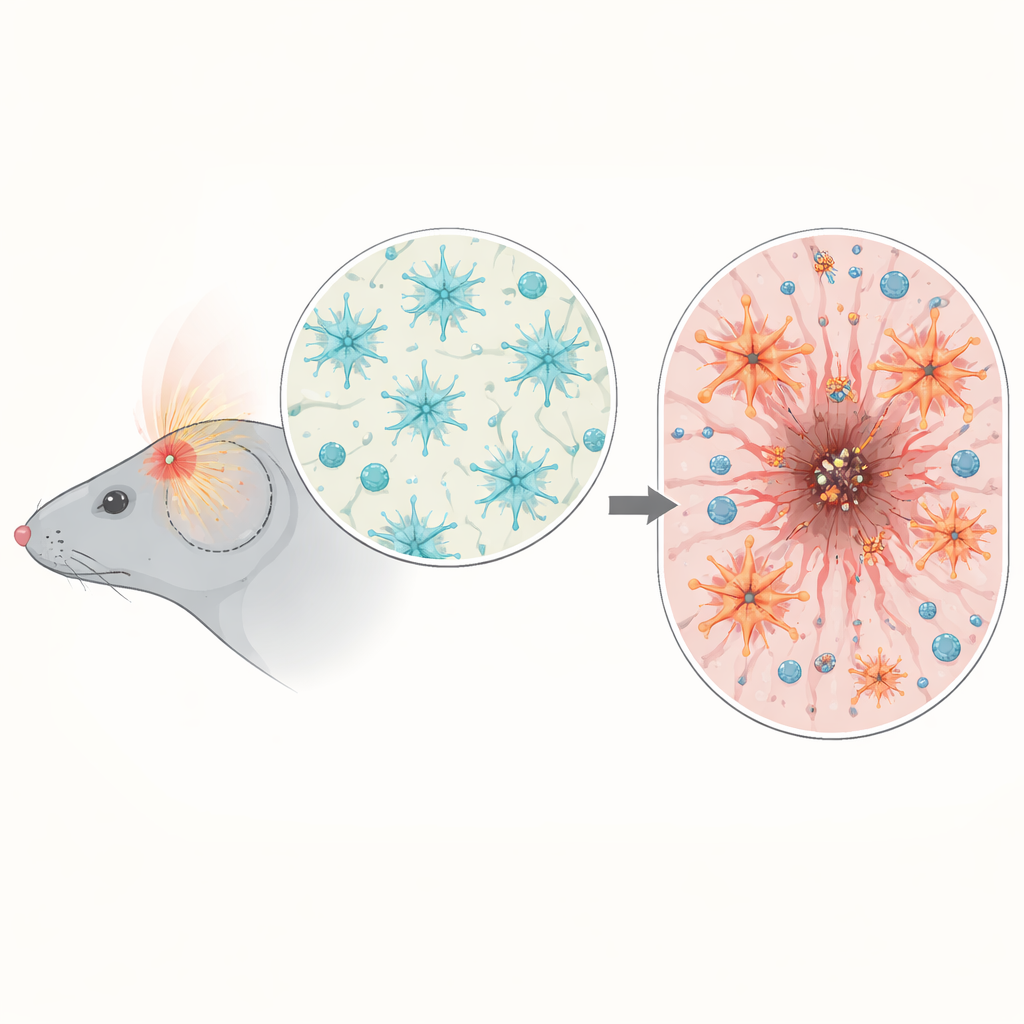
将星形胶质细胞调到过高档位
为检验因果关系,科学家制造了在脑发育完成后可使星形胶质细胞内NF-κB活性被人为增强或抑制的小鼠。当这些小鼠遭受头部创伤时,星形胶质细胞中NF-κB过度激活的那些小鼠体重下降更多,早期神经学评分更差,且在组织切片和磁共振成像上显示出更大且更持久的脑损伤区域。它们并未形成围堵损伤核心的整齐、界定清晰的瘢痕,而是产生了厚重且无序的边界,随时间未能收缩伤口。损伤周围支持性基质蛋白的正常平衡被打乱,名为胶质极限(glial limitans)的关键外层屏障结构形成不良,使周围脑组织的保护减弱。
当愈合程序偏离轨道
深入分子细节,团队分离出星形胶质细胞和邻近免疫细胞进行逐基因分析。在健康动物中,受伤通常会抑制星形胶质细胞的一些日常家务功能,同时启动支持伤口闭合和再生的基因。相反,长期处于活跃NF-κB状态的星形胶质细胞在受伤前就已显得“受损”,受伤后它们未能充分启动有益的修复程序,例如那些与受控转变、帮助细胞构建有效边界相关的程序。相反,它们强烈偏向炎症基因,呈现出与衰老和神经退行性疾病相关的有毒星形胶质细胞特征,并显示出与慢性、无法消解伤口相关的“类衰老”分泌谱的迹象。
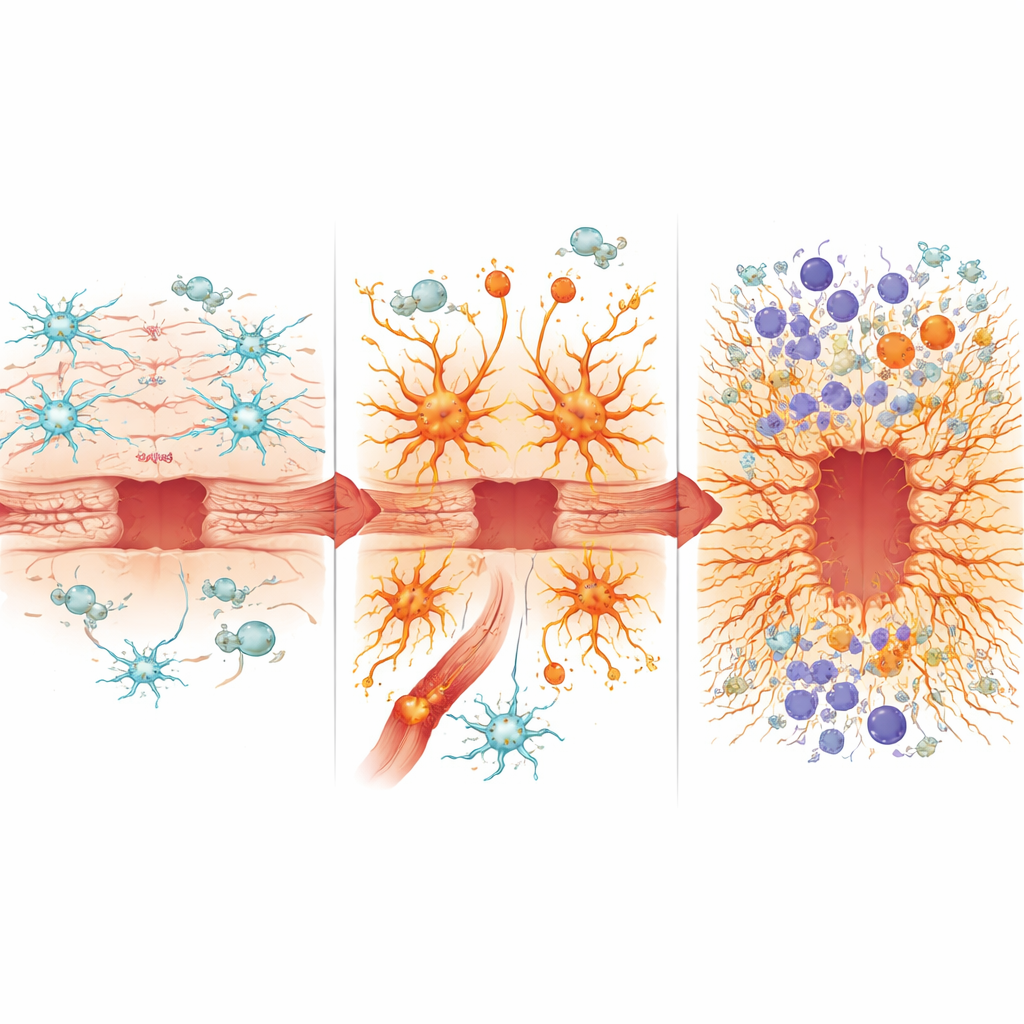
燃起免疫之火
这些被误编程的星形胶质细胞也重塑了大脑的免疫格局。血–脑屏障变得更为渗漏,允许更多外周免疫细胞进入。星形胶质细胞中NF-κB过度激活的小鼠显示炎性髓系细胞浸润加重、中性粒细胞、单核细胞和树突状细胞的组成改变,以及可进一步损伤组织的细胞毒性T细胞增加。在这种环境中,免疫细胞表达出更强的由干扰素和炎症小体通路驱动的信号,这两者都与侵袭性、可能具有神经毒性的炎症相关。与此同时,多种保护或促修复蛋白(如骨桥蛋白/osteopontin)水平降低,而与氧化应激、铁负荷和瘢痕形成相关的蛋白,包括血红素氧合酶-1和脂蛋白结合蛋白2(lipocalin-2)则升高。骨桥蛋白与脂蛋白结合蛋白2的比值成为一个简单标记,可反映不同小鼠品系间愈合好坏的关系。
这对头部损伤康复意味着什么
总体而言,结果表明当星形胶质细胞内的NF-κB应激通路长期被激活时,这些细胞会从支持有序修复转向驱动混乱的瘢痕形成和持续性炎症。它们并未建立一个能封闭损伤并允许组织重塑的干净边界,而是助长了一个渗漏、炎性的微环境,扩大了病灶并损害长期预后。尽管这项工作在雄性小鼠中完成,但它指向星形胶质细胞的NF-κB作为一个有前景的治疗目标,旨在改善创伤性脑损伤后的恢复,并提示血液中如骨桥蛋白和脂蛋白结合蛋白2等分子未来或可帮助临床医生监测患者大脑愈合的状况。
引用: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
关键词: 创伤性脑损伤, 星形胶质细胞, 神经炎症, 脑瘢痕形成, NF-κB