Clear Sky Science · zh
PfDNMT2 抑制机制与 PfATP6 介导的对疟疾候选药物 SC83288 的耐药性在恶性疟原虫中的作用机制
这对疟疾为何重要
随着疟原虫对现有药物产生抗性,医生可用于治疗这一仍然每年夺去数十万生命(主要是年轻儿童)的疾病的选择越来越少。本研究解析了一种有前景的实验性药物 SC83288 如何攻击最致命的疟原虫,以及寄生虫有时如何设法反击。理解药物的杀伤机制和寄生虫的反制策略,对于将 SC83288 转化为能尽可能长期保持疗效的未来疗法至关重要。 
对致命寄生虫的新武器
SC83288 源自改良一种老兽药的努力,现在作为一种强效的抗疟候选药脱颖而出。在体外实验和动物模型中,它能在极低浓度下迅速清除血液中的疟原虫,包括那些已对一线治疗(如基于青蒿素的联合疗法)以及较早期药物(如抗叶酸药和奎宁类)产生耐药的菌株。它还作用于可被传播给蚊子的寄生虫阶段。到目前为止,动物的广泛安全性测试尚未显示重大警示,使 SC83288 成为进入人体临床试验的现实竞争者。
药物如何终止寄生虫生长
研究人员跟踪了寄生虫在红细胞内的 48 小时周期,并在不同时间加入 SC83288。当药物在该周期的前三分之二存在时,寄生虫停止复制 DNA 并未能完成核分裂(称为有丝核分裂)。在显微镜下,受处理的寄生虫变得小而致密,这是细胞死亡的标志,而如果分裂已完成,后续步骤如分裂成子代寄生虫和破裂出红细胞则不受影响。这将 SC83288 的主要作用锁定在寄生虫为产生大量后代而复制遗传物质的关键时间窗口。
打击寄生虫的“表观遗传”控制中心
为了解 SC83288 在寄生虫内部作用的靶点,团队结合了基因表达谱、代谢测量和直接酶学测试。他们发现强烈证据表明该药物扰乱了寄生虫利用微小化学标签控制 DNA 和 RNA 的方式。作为这些标签关键供体分子之一的 S-腺苷甲硫氨酸(SAM)水平失衡,治疗后 DNA 与 RNA 的整体修饰标记显著下降。聚焦于一个核心酶 PfDNMT2——它通常向 DNA 以及某种特定的转移 RNA 添加甲基——科学家们证明 SC83288 在体外和寄生虫内都能直接抑制其活性。当寄生虫被工程化以产生大量 PfDNMT2 时,它们对药物的敏感性降低;而额外供应甲基供体分子则部分挽救了寄生虫免受 SC83288 的影响。综合这些结果支持这样一种模型:SC83288 通过破坏寄生虫的表观遗传和基因表达机制来致死,导致 DNA 复制停滞并最终细胞死亡。 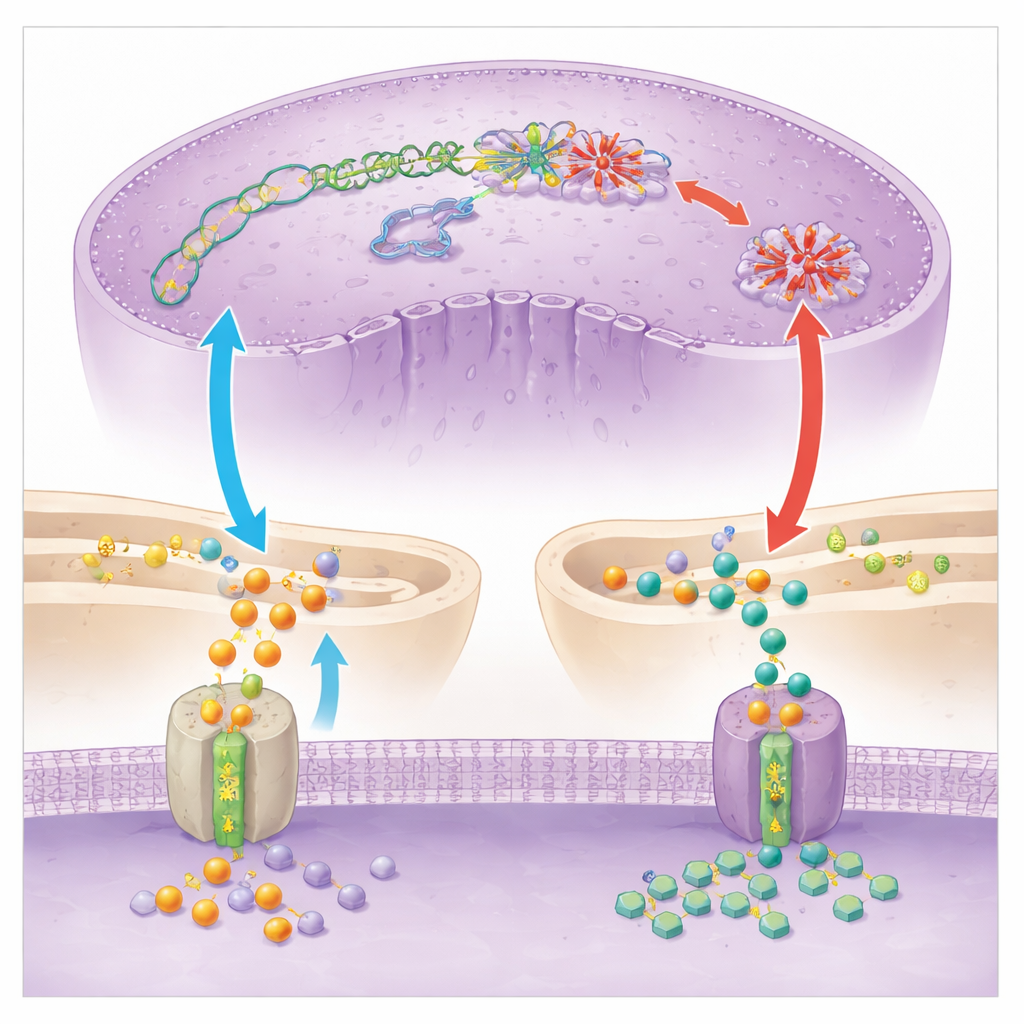
寄生虫如何躲避打击
任何有效药物都存在耐药风险,SC83288 也不例外。在长期培养暴露后,一些寄生虫系获得的变异并不在目标酶 PfDNMT2 上,而是在一种名为 PfATP6 的膜泵上发生。该泵通常有助于控制寄生虫内质网内的钙水平——内质网是细胞内的一种膜网络。通过基因工程,团队将其中一种突变导入一个标准寄生虫株,结果显示该突变使寄生虫对 SC83288 的敏感性降低约一千倍。酵母和寄生虫中的详尽运输实验,以及使用可点击荧光标记药物的成像,揭示了原因:突变的 PfATP6 像吸尘器一样,将 SC83288 从细胞核附近抽走并集中到内质网中。药物仍能进入被感染的红细胞,但现在被隔离到一个对核过程伤害较小的隔室中。
耐药的隐性代价
尽管 PfATP6 突变为寄生虫提供了对 SC83288 的保护,但这种保护代价高昂。耐药寄生虫的生长速度远低于未突变的对照株,并表现出钙平衡紊乱,表明改变后的泵在其正常功能上表现不佳。在混合培养中,在无药物存在时,适者更强的野生型寄生虫很快就会胜出并取代突变株。这表明虽然在强药物压力下此类耐药可能出现,但在野外广泛传播的可能性较低,因为在没有 SC83288 的情况下耐药寄生虫会处于劣势。从公共卫生角度看,这种高适应性代价,加上该药以新颖方式攻击寄生虫的表观遗传控制系统,使 SC83288 在与疟疾赛跑中成为一个特别有吸引力的候选药物。
引用: Sanchez, C.P., Duffey, M., Celada, R.V. et al. Mechanisms of PfDNMT2 inhibition and PfATP6-mediated resistance to the antimalarial candidate SC83288 in Plasmodium falciparum. Nat Commun 17, 2327 (2026). https://doi.org/10.1038/s41467-026-70280-y
关键词: 疟疾 药物耐药, 恶性疟原虫, 表观遗传治疗, DNA 甲基化, 抗疟药开发