Clear Sky Science · zh
NAA40 与 NAC 在人体协同进行共翻译组蛋白乙酰化
细胞如何精细调节其基因开关
在每个人体细胞内,新合成的蛋白质在从细胞的蛋白质合成机器——核糖体——刚刚伸出时会被化学修饰。这些微小的调整可以决定蛋白质的去向、寿命,甚至影响基因的开启或关闭。本文聚焦于一种高度特异的酶 NAA40 及其辅助复合体 NAC,揭示了它们如何在核糖体上协同作用,修饰组蛋白(DNA 绕其缠绕的线轴),从而影响基因活性并可能与癌症发展相关。
改变组蛋白行为的一枚微小帽子
许多人类蛋白在其起始端会被加上一个小的化学“帽子”,称为 N 端乙酰化。帮助将 DNA 打包成染色质的组蛋白 H2A 和 H4 几乎总是以这种方式被修饰。NAA40 在酶类中较为特殊,因为它几乎专门在这些组蛋白被合成时为它们添加这一乙酰帽。该乙酰标记会与同一区域上的其他化学标签(如磷酸化和甲基化)竞争,因此 NAA40 是否发挥作用会改变 DNA 的紧密包装程度及基因的调控方式。值得注意的是,NAA40 水平的异常已与多种癌症相关,使其成为潜在的药物靶点。
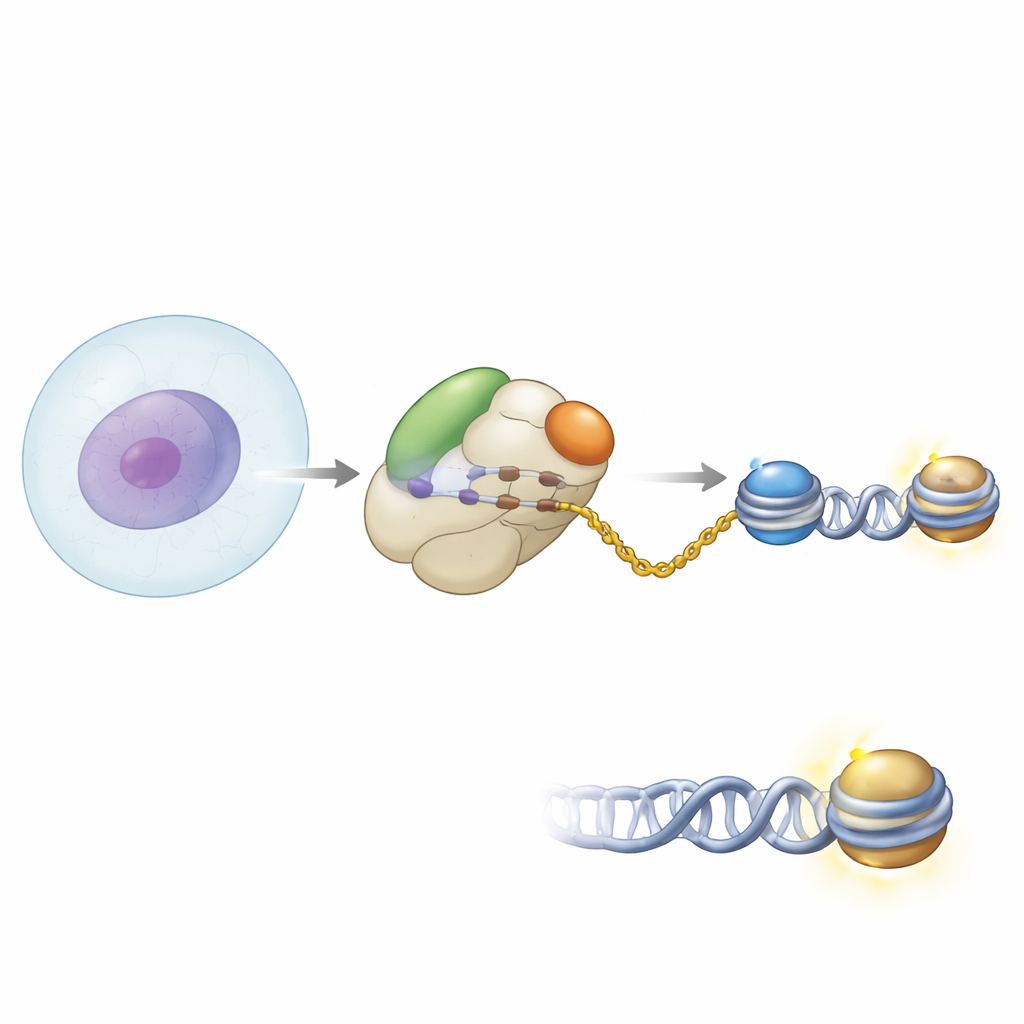
在蛋白工厂门口的合作伙伴
作者使用生化方法和高分辨率冷冻电子显微镜观测了 NAA40 在人类核糖体上的位置。他们发现 NAA40 位于新生肽链出现的通道出口处。在那里,它并非单打独斗:它与新生多肽相关复合体(NAC)并列结合,NAC 是一种常见的核糖体结合辅助因子,负责监护刚出炉的蛋白质。结构快照显示,NAA40 通过其 N 端一段带正电的独特螺旋片段锚定于核糖体,而 NAC 则通过其某一亚基与核糖体表面连接。NAC 的一个柔性结构域伸过来接触 NAA40,有效地将该酶桥接到核糖体上。
为什么 NAC 对组蛋白调节至关重要
为测试这种合作的重要性,研究者在体外用纯化组分重建了这些相互作用。他们观察到,单独的 NAA40 与核糖体结合很弱,但在 NAC 存在时,核糖体结合显著增强。如果去掉 NAC 中与 NAA40 接触的特定“UBA”区段,这种增强的结合就会消失。在人类细胞中,耗竭 NAC 会导致 NAA40 依赖的组蛋白 H4 乙酰化减少,同时同一组蛋白尾部上的竞争性磷酸化标记增加。这一变化发生时 NAA40 本身的数量或定位并未改变,表明 NAC 的主要作用是将 NAA40 招募并定位到正在翻译的核糖体上,使组蛋白在合成过程中能被高效修饰。
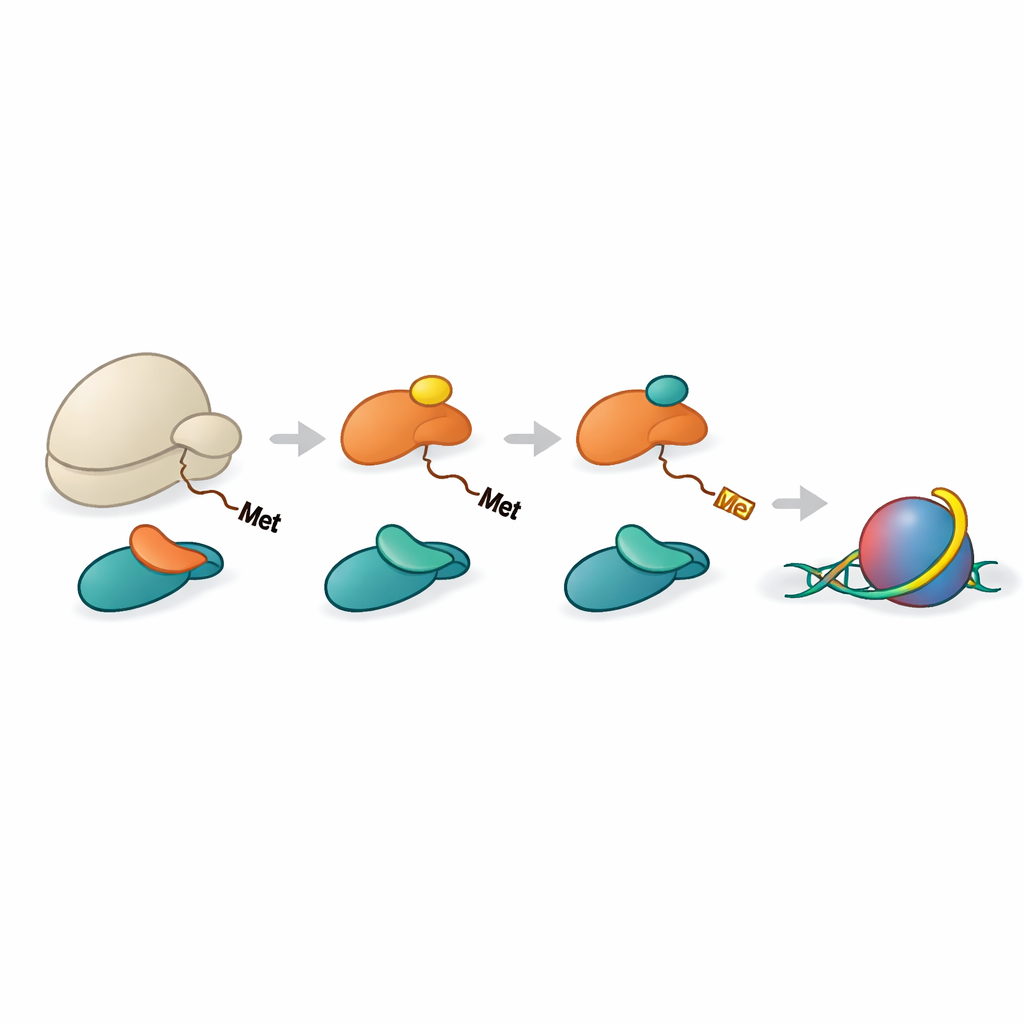
为组蛋白加工而协调的装配线
在 NAA40 识别组蛋白之前,组蛋白 H2A 和 H4 必须先失去其起始的甲硫氨酸残基。另一种酶 METAP1 负责这一剪切步骤。研究团队表明,NAC 可以帮助将 METAP1 和 NAA40 一起带到核糖体上,在肽链出口处形成一个多酶装配体。重建复合体的高分辨率结构显示,METAP1 和 NAA40 并排结合在核糖体上,它们的活性位点距出口隧道几乎等距。这种几何排列意味着,一旦组蛋白的尾部伸出核糖体大约十几个氨基酸,METAP1 就可以切掉起始甲硫氨酸,NAA40 随即添加乙酰帽,从而将两步之间的延迟降到最低。
对基因控制和癌症的启示
总体而言,这项研究表明 NAA40 并非在细胞内自由游走寻找组蛋白并修饰它们。相反,它被 NAC 停靠在核糖体上,成为一个有序加工站的一部分,能在组蛋白合成的瞬间对其进行准备。通过将甲硫氨酸去除与乙酰化紧密耦合,细胞确保组蛋白 H2A、H4 以及与 DNA 损伤相关的变体 H2A.X 能迅速获得能影响染色质结构和基因表达的乙酰标记。由于这一早期组蛋白标记步骤的失衡可能有利于肿瘤生长,理解 NAA40、NAC 与 METAP1 在核糖体上的精确排列,提供了一个结构蓝图,可用于指导旨在微调这一关键表观遗传控制点的药物设计。
引用: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
关键词: 组蛋白乙酰化, NAA40, 核糖体, 新生多肽相关复合体, 表观遗传调控