Clear Sky Science · zh
一种依赖细胞周期的乙酰化到磷酸化的转换调控中心体按时成熟
让我们的遗传货物保持正轨
每当我们体内的细胞分裂时,都必须以极高的精度分配其 DNA。这个过程出错时,细胞可能获得或丢失染色体,这是一种与癌症和其他疾病相关的危险状态。本研究揭示了一个分子定时装置,帮助细胞构建将染色体正确分离所需的小型结构,暴露出一个未来抗癌疗法可能利用的薄弱环节。
细胞的小型交通枢纽
在每个分裂的细胞中心有中心体,它们像交通枢纽一样管理牵引染色体的纤维。在细胞进入分裂之前,这些枢纽必须“成熟”:它们聚集辅助手蛋白,成为微管这个动力纤维的强大组织者,微管形成分裂纺锤体。如果这种成熟过早、过晚或根本没有发生,染色体就会分配错误,导致染色体数目异常。理解细胞如何在恰当时刻开启中心体长期以来一直是细胞生物学中的重要问题。
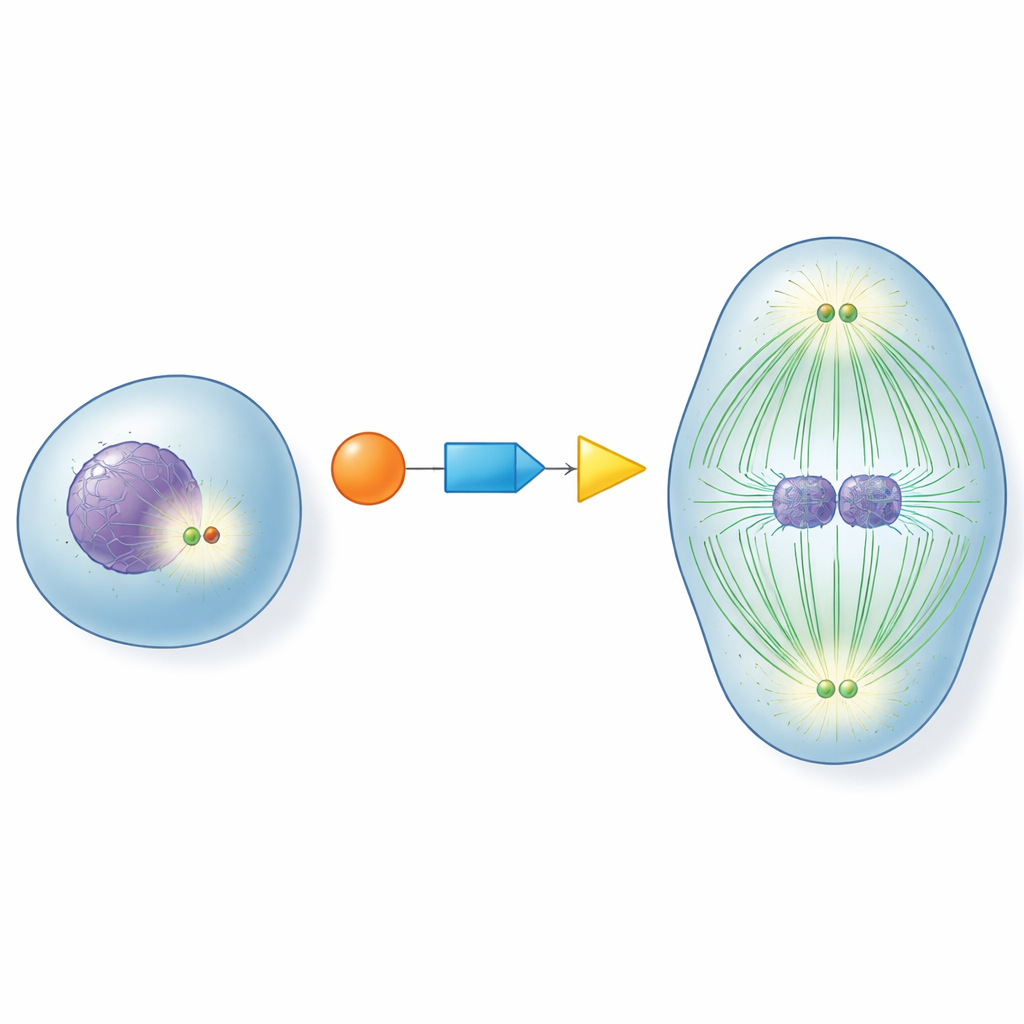
实现精确时序的分子接力
作者将注意力集中在三个协同工作的关键蛋白上:细胞周期主控 CDK1、先前主要与染色质修饰相关的 RNF40,以及推动细胞分裂的关键驱动因子 PLK1。他们发现 RNF40 在整个细胞周期中物理定位于中心体并直接结合 PLK1。当细胞接近分裂时,CDK1 在 RNF40 的两个特定位点上进行化学标记,这反过来使 RNF40 成为更好的 PLK1 停靠位点。CDK1–RNF40–PLK1 这一链条确保 PLK1 在分裂的晚期准备阶段精确地到达中心体,触发强有力的中心体成熟、微管生长以及结构良好的双极纺锤体的组装。
会形变的蛋白质开关
耐人寻味的是,RNF40 并不总是接受这些激活性标记。在非分裂期和 DNA 复制期,RNF40 在两个相邻位点带有不同的化学修饰——乙酰基。这些乙酰标记由酶 PCAF 加上,随后由去乙酰化酶伴侣 HDAC1 去除。乙酰化的 RNF40 抵抗 CDK1 的修饰,有效阻断了接力的下一步。当细胞进入最终的分裂前期时,HDAC1 逐步抹去这些乙酰标记,使 CDK1 能够改为添加磷酸基。这种从乙酰化到磷酸化的精确时序转换,将 RNF40 从“待命”状态转换为“开启”状态,准备招募 PLK1 并激活中心体。
当时序失败会发生什么
为探究该开关的重要性,研究人员构建了无法被磷酸化的 RNF40 突变体,或被迫保持模拟乙酰化状态的 RNF40。在两种情况下,PLK1 都无法在中心体正常积累。这些细胞表现出中心体微管生长减弱、纺锤体畸形和染色体未对齐。许多细胞最终出现染色体缺失或多余的情况——称为非整倍性——并且有些细胞变为双核,显示分裂严重出错。在癌症模型中,处于“乙酰化”RNF40 状态的细胞在小鼠中形成的肿瘤更小,并对用于治疗结直肠癌的常用化疗药物更敏感,表明扰乱该开关可以减缓肿瘤生长。
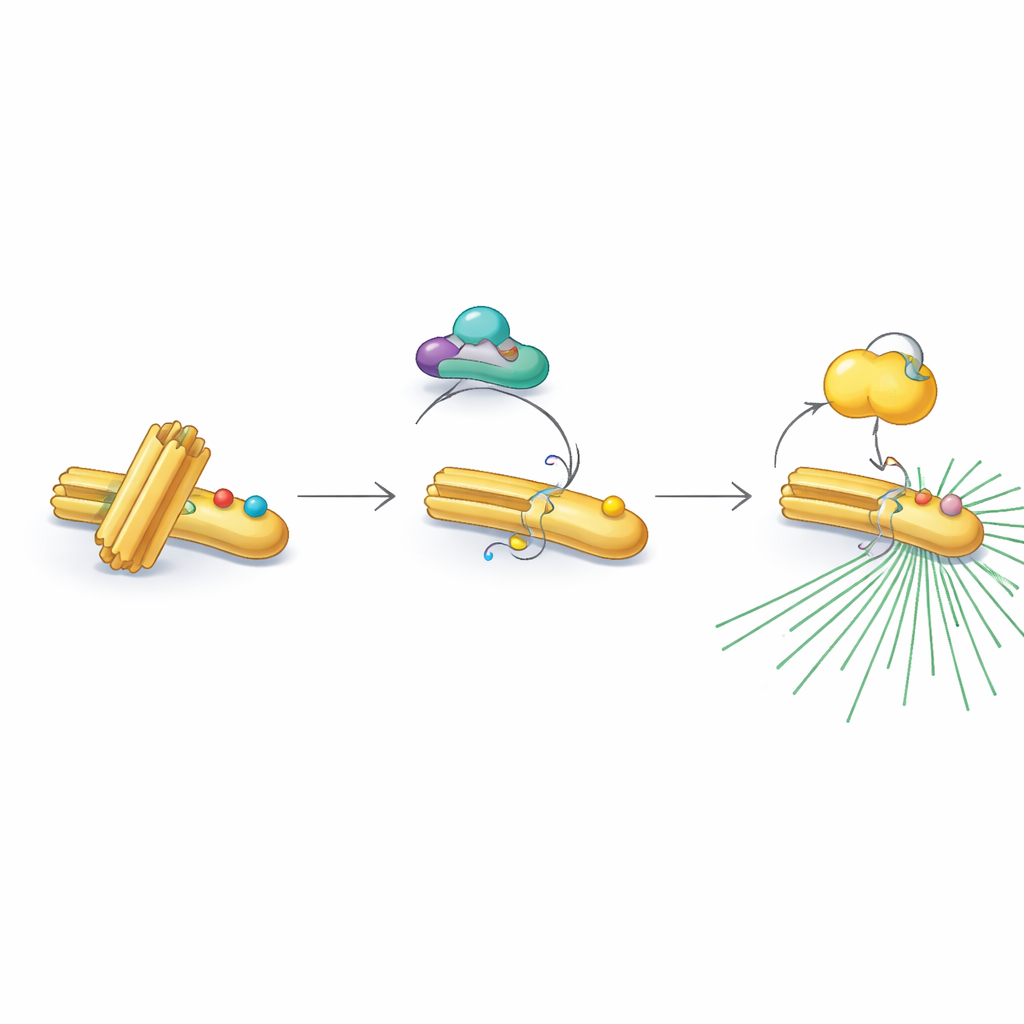
与人类癌症的关联与未来可能性
研究团队还分析了患者数据和肿瘤样本。他们发现 RNF40 在结直肠癌中常常异常增多,并且一些靠近其修饰位点的癌症相关突变会破坏其磷酸化,从而削弱中心体功能。这些观察将新描述的时序机制直接与人类疾病联系起来。通过定位一个在中心体成熟时间和染色体分离中起协调作用的特定蛋白,这项研究突出了一个信号“节点”,有望成为将快速分裂的癌细胞推向致命分裂错误的靶点,同时较少影响健康细胞。
对忠实细胞分裂的新控制手柄
对非专业读者而言,核心信息是:细胞依赖单一蛋白 RNF40 上一个精细调控的化学开关来决定何时激活分离染色体的机器。这个从乙酰化到磷酸化的转换就像繁忙路口的交通信号灯,仅在细胞真正准备好分裂时变为绿色。当信号灯失灵时,细胞在分裂过程中跌跌撞撞,积累遗传错误,可能致癌。理解并控制这一开关或许会开辟新的途径,通过破坏癌细胞干净分裂的能力来选择性地不稳定它们,从而成为潜在治疗策略。
引用: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
关键词: 中心体成熟, 细胞分裂, 染色体不稳定性, PLK1 信号, 结直肠癌