Clear Sky Science · zh
恢复早期产后突触失调可挽救脊髓延髓性肌萎缩小鼠模型的运动神经元退行性变
为什么早期微小变化会影响后期肌无力
脊髓延髓性肌萎缩(SBMA)是一种罕见的遗传性疾病,通常在成年人(多为男性)中出现,随着时间推移肢体、躯干和咽喉肌力逐渐丧失。症状在中年出现,但微妙的问题早在更早时期就已开始。本研究提出了一个令人意外的问题:出生后最初几天里的短暂事件是否会在多年后悄然为神经细胞丧失埋下伏笔——如果纠正那些早期的失调,是否能够保护运动功能?
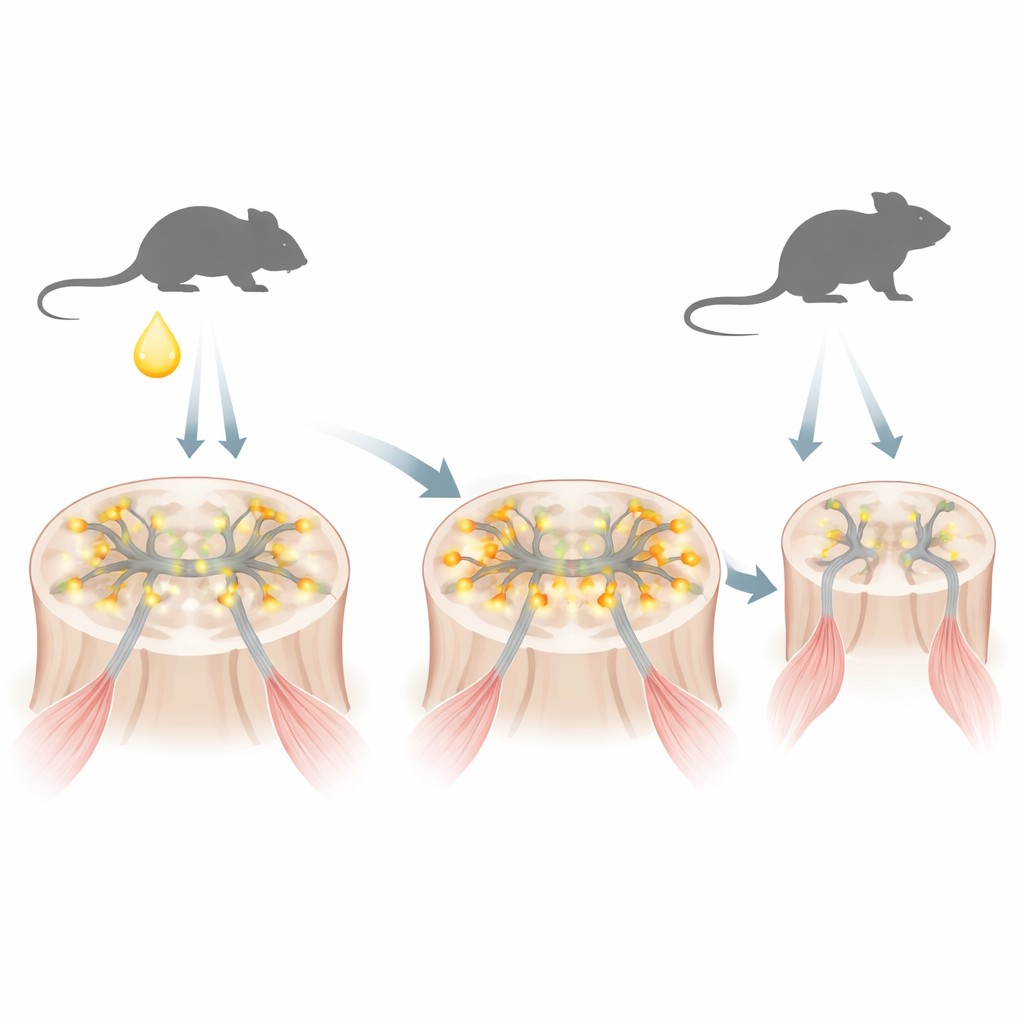
一种以激素敏感开关为根源的疾病
SBMA 由改变的雄激素受体引起,这是一种感知雄性激素(如睾酮)的蛋白。变异受体携带异常延长的谷氨酰胺序列。在模拟人类疾病的小鼠模型中,研究者发现出生后不久,当雄性幼鼠体内短暂出现睾酮高峰时,这种突变受体会迅速在运动神经元的细胞核内积聚。在这一早期阶段,蛋白尚未形成通常与神经退行性变相关的大型包涵体,但它已经开始改变基因的开启与关闭模式。
早期突触过度驱动与躁动的运动神经元
通过对新生小鼠脊髓进行全基因组 RNA 测序,研究团队发现许多参与兴奋性突触的基因——即神经细胞相互通信的接触点——异常活跃。其中许多基因编码谷氨酸受体,这类受体使神经元更容易发生放电。研究组将这一模式追溯到 REST 的功能紊乱,REST 是一个在发育过程中通常对这些突触基因实施严格抑制的“制动”蛋白。在 SBMA 小鼠和由患者诱导多能干细胞分化得到的运动神经元中,REST 的活性被削弱,并且更倾向于产生一种截短的形式称为 REST4,从而解除抑制并提升谷氨酸能突触基因的表达。与此一致的是,新生 SBMA 运动神经元显示出更高水平的 c-Fos(近期放电的标志),而来源于人类患者的运动神经元表现出更强且更频繁的钙波突发,均为过度兴奋性的特征。
短暂的早期治疗改变终生进程
研究者接着探究仅在新生期窗口内下调突变受体或恢复 REST 制动是否能改变疾病的长期进程。他们在一日龄的 SBMA 小鼠脑脊液周围注入了反义寡核苷酸——一种由修饰基因材料构成的短链分子。第一类寡核苷酸在中枢神经系统中暂时降低了突变与正常雄激素受体的水平;第二类则改变了 REST 的剪接,使其远离 REST4 而回到全长 REST,从而抑制突触基因。值得注意的是,尽管这些治疗仅给药一次并且其直接的分子效应在数周内消退,接受治疗的鼠群寿命更长、在旋转杆测试中表现更好,并在成年后仍保持较强握力。它们的运动神经元和肌纤维较少萎缩,早期神经元过度活动的标志和晚期应激相关神经肽的激增都被减弱了。
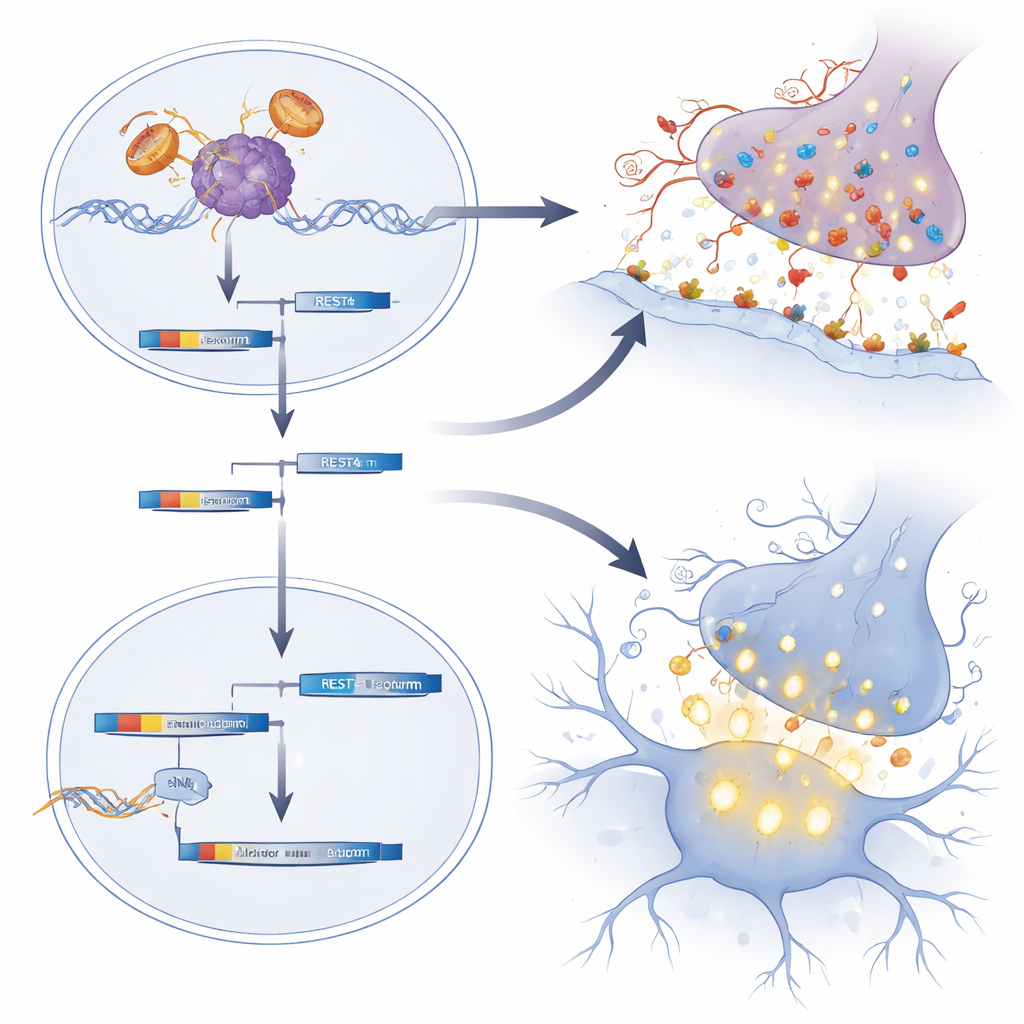
早期激素与基因调控如何塑造易感性
这项工作还突出表明,运动神经元在出生后不久出现的短暂睾酮激增期间具有特殊的易感性。当新生 SBMA 小鼠额外给予睾酮时,它们日后的无力和体重下降加剧,与健康运动神经元成熟相关的基因程序进一步被扰动。正常小鼠未见此类损伤,强调了有害效果来自突变受体与激素激增的结合。综上所述,研究结果表明在 SBMA 中,生命早期过多的兴奋性突触和过度兴奋的运动神经元会缓慢地将系统推向衰竭,尽管明显的症状要到中年才出现。
这对生活在 SBMA 患者意味着什么
对非专业读者来说,核心信息是:SBMA 在某种程度上可能是一种由出生后最初几天突触时序错误和连接异常引起的疾病。一个失常的激素感受器会将发育中的运动神经元推入过度兴奋的状态,而这种早期压力最终会在数年后促成它们的退化。令人鼓舞的是,经过精心设计的基因药物在这些关键窗口期内给药,能够重置运动神经元的信号平衡、平息其过度活动,并在动物中显著延缓或减少随后神经细胞的丧失。虽然将此类早期干预转化为对人类的治疗需要极大的谨慎和进一步研究,但这些结果为在症状出现之前就针对 SBMA 根源的全新策略指明了方向。
引用: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
关键词: 脊髓延髓性肌萎缩, 运动神经元过度兴奋性, 雄激素受体, REST 突触调控, 反义寡核苷酸疗法