Clear Sky Science · zh
通过改进的高斯混合建模在 DNA-PAINT 中的分子映射
看见分子那不可见的世界
现代生物学越来越依赖能够看到细胞内单个分子的显微镜。然而,要把这些微弱、闪烁的分子荧光信号转化为可靠的“地图”,准确标出每个分子的位置,却比想象中困难得多。本研究提出了一种新的计算方法,称为 G5M,它能显著提高这些分子地图的精确度和细节,帮助科学家在真实细胞中以纳米甚至更高精度理解蛋白质的排列与聚集。
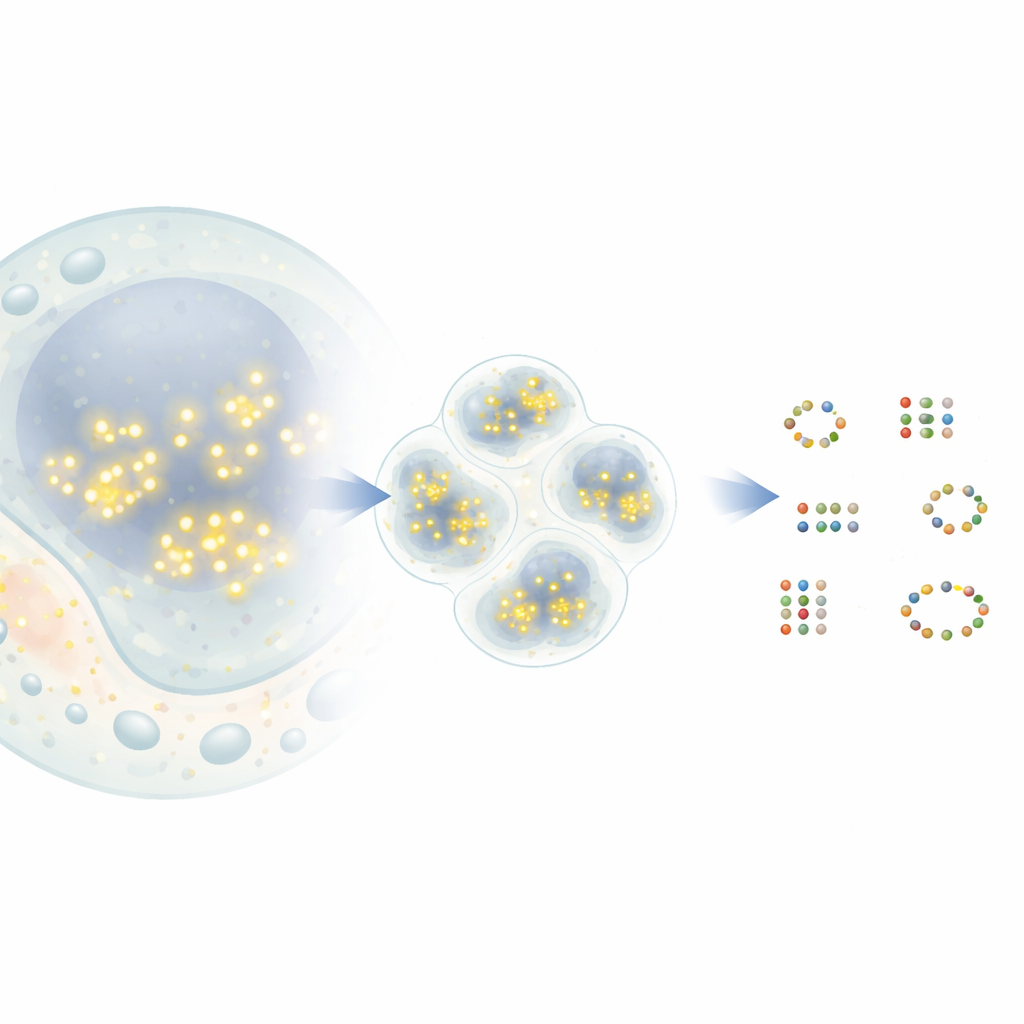
从闪烁点到分子地图
在一种流行的超分辨率技术 DNA-PAINT 中,携带荧光染料的短 DNA 链会短暂地与标记在目标蛋白上的互补 DNA 结合并解离。每次染料结合时,在显微镜下会出现一个亮点,然后再次消失。随着时间累积,许多这样的事件在每个蛋白周围形成一个点云。理论上,每个点云的中心标记了蛋白的真实位置,精度可达纳米量级。但在实际操作中,来自相邻蛋白的点可能重叠,且一些点源自随机背景信号。现有的分析工具常常将相近的邻点合并为一个蛋白,或相反地虚构不存在的蛋白,从而限制了可提取的生物学信息。
一种更智能的真实分子定位方法
新方法 G5M 将点簇视为若干简单的钟形云的混合,每个云对应一个真实分子。G5M 不仅按密度对点进行分组,而是使用一个概率模型,纳入了关于实验已知的信息:位置测量的精确度、DNA 链结合与解离的速率以及显微镜在二维或三维中对光的模糊方式。然后它测试不同的可能解释——不同数量和形状的云——并自动选择在拟合度与简洁性之间取得最佳平衡的方案。额外的保护措施会拒绝可疑解,例如基于太少点的云、过窄或过宽的云,或彼此未能清晰分离的云。
在模拟与 DNA 纳米结构中验证其实力
为测试 G5M,作者首先使用了现实的计算模拟来重建简单场景:分子对以及仅相隔数纳米的十二分子小网格。与当前的主流方法(称为梯度上升法)相比,G5M 找到了更多在理论分辨率极限下本应可见的分子,同时几乎不报告不存在的分子。在关键情形下,它恢复紧密间隔的分子对的频率比旧方法高出二十七倍,并将有效分辨率提高了超过一半。随后研究团队在实验上使用 DNA 折纸结构——在已知精确位置放置停靠位点的人工 DNA 形状——证明了这些改进,显示 G5M 在多种成像条件下都能可靠地计数并定位几乎所有预期位点。
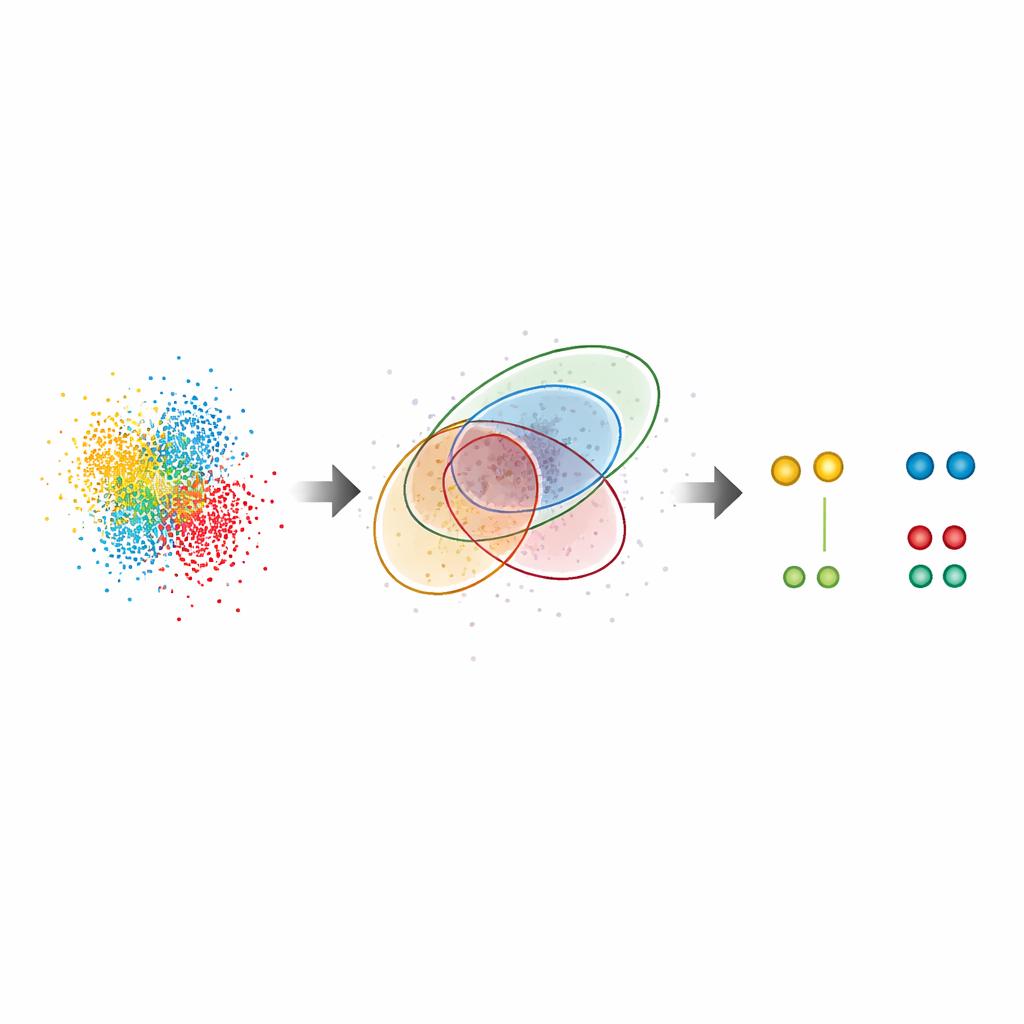
揭示真实细胞中的隐含模式
在测试样本之外,G5M 还被应用于复杂的生物系统。在细胞核中的巨大通道——核孔复合体中,该方法在蛋白质 Nup96 的环状排列上得到了已知的结构,即使其伙伴之间仅相隔约十纳米。它发现的蛋白对数量几乎是标准方法的两倍,并重现了独立的标记效率估计,表明它既不会漏掉大量分子,也不会产生虚假的分子。作者还研究了 CD20,这是一种与血液肿瘤相关、又是治疗性抗体靶点的表面受体。在这里,G5M 揭示了细胞膜上明显更多的小簇(双聚体、三聚体和四聚体),阐明了抗癌抗体及相关药物形式如何重组这些受体。它甚至提高了一种依赖多轮成像将信号分离的超高分辨率方法 RESI 的性能。
这对未来显微镜意味着什么
通过从现有的 DNA-PAINT 数据中提取更可靠的信息,G5M 表明单靠更好的软件即可解锁新的生物学细节,而无需更换显微镜或染料。该算法在保持极低误检率的同时,能分辨出几乎相互接触的分子,这对于回答复杂中包含多少蛋白、它们如何间距或药物如何改变其排列等问题至关重要。作为开源平台 Picasso 的一部分并对典型设置具备鲁棒性,G5M 有望成为将闪烁的荧光信号转化为可靠分子地图的标准工具,帮助研究者绘制细胞内部纳米级的生命组织结构。
引用: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
关键词: 超分辨率显微镜, DNA-PAINT, 分子映射, 蛋白寡聚化, 图像分析算法