Clear Sky Science · zh
单细胞多组学揭示内皮细胞力敏感的 PIEZO1–IL-33 轴驱动肺纤维化
为什么僵硬的肺很重要
肺纤维化是一种毁灭性的肺部疾病,曾经富有弹性的肺泡会逐渐被僵硬的瘢痕组织取代,使每一次呼吸都变得艰难。当前临床上只能减缓病情进展,无法完全阻止或逆转。本文提出了一个看似简单但影响深远的问题:衬于肺血管内壁的细胞如何感知周围组织异常变硬,并将这种机械感知转化为更多的瘢痕?通过将这一事件链追踪到单个细胞和具体基因,研究者们在血管中发现了一个潜在可药物干预的机械“开关”。
从肺功能检测到单细胞解析
研究团队以特发性肺纤维化患者(该病最常见的形式)和肺功能正常的供体的肺组织为起点,结合标准的肺功能测定(比如用力呼气量)与强大的单细胞 RNA 测序技术,后者可以读取成千上万单个细胞中哪些基因处于活跃状态。使用一种将总体临床数据与单细胞谱联系起来的计算工具,他们定位出与严重肺功能受损最密切相关的细胞类型。血管内皮细胞——构成血管内膜的细胞群——在肺容量低于正常一半的患者中明显富集。在这些内皮细胞中,与“机械应力”相关的基因程序持续升高,提示异常的物理力学环境是问题的一部分。
机械应力作为隐匿的驱动因子
为检验这种应力感知与疾病之间联系的普遍性,研究者转向两种小鼠肺纤维化模型:一种由化疗药物博莱霉素(bleomycin)诱发,另一种由长期硅尘暴露(职业性危害)引发。对这些实验性肺组织进行单细胞分析时,他们再次发现内皮细胞呈现出明确的机械应激标志。在两种模型中,随着周围肺组织增厚并变硬,血管内膜细胞似乎转入一种不适应的状态。人样本与动物模型间的这种一致性加强了这样一个观点:肺组织中扭曲的物理力学,而不仅仅是炎症或免疫活动,是纤维化发生和进展的核心因素。
具有关键作用的压力感受器
进一步挖掘时,研究团队寻找在受压内皮细胞中上调的特定“机械感受器”——将物理拉伸转换为生化信号的蛋白。一种名为 PIEZO1 的通道蛋白多次成为主要嫌疑。在患病的小鼠和人类样本中,血管内皮细胞中的 PIEZO1 水平明显高于健康对照。当研究者构建仅在内皮中删除 PIEZO1 的小鼠时,这些动物对博莱霉素诱导的肺纤维化表现出更强的抵抗力:胶原沉积减少,活化的成纤维细胞更少,纤维化的化学标志物水平也更低。用肽类抑制剂药理学阻断 PIEZO1 也能缓解瘢痕形成,而激活它会加重纤维化——除非该受体在内皮细胞中缺失。上述实验表明,血管内膜细胞中的 PIEZO1 不是旁观者,而是疾病发展的必要驱动之一。
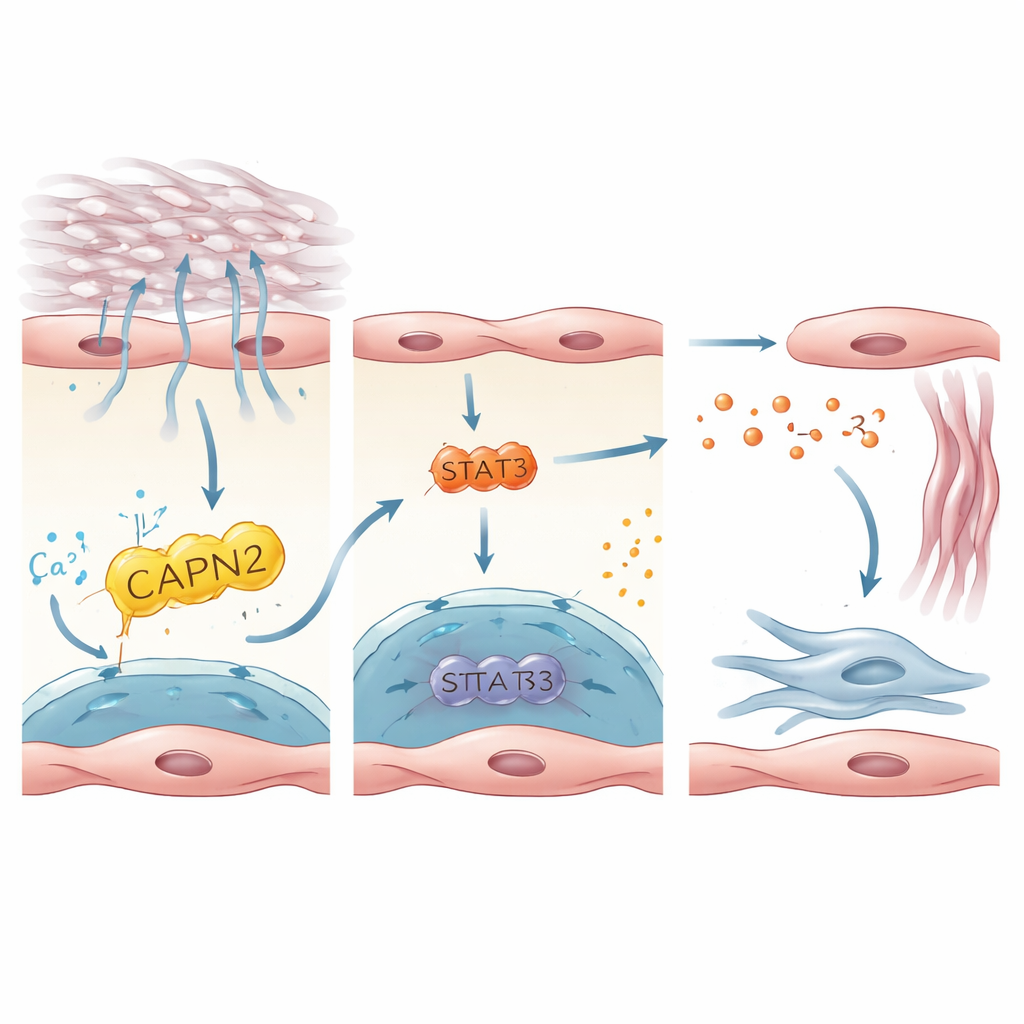
唤醒成瘢细胞的信号链
随后研究追踪了内皮细胞内 PIEZO1 激活如何被转化为唤醒成纤维细胞(即沉积瘢痕组织的细胞)的信号。通过整合人类与小鼠数据集,作者将线索集中到白细胞介素‑33(IL‑33)——一种由受压或受损细胞释放的小型信号蛋白——作为关键传递者。IL‑33 在 PIEZO1 阳性的内皮细胞中高表达,并在患病人和小鼠的肺中升高。在体外培养的人内皮细胞中,生长在刚性基底或被拉伸以模拟刚硬肺部的呼吸条件下,PIEZO1 激活促进了 IL‑33 的产生。这一过程依赖于下游酶 CAPN2 和转录因子 STAT3,它们共同调控 IL‑33 基因的活性。在小鼠中,特异性删除内皮细胞的 IL‑33 可保护动物免受纤维化,而强制使内皮细胞过表达 IL‑33 则抹消了丧失 PIEZO1 所带来的保护效应。这些结果描绘了一条线性轴:机械应力 → PIEZO1 → CAPN2/STAT3 → IL‑33 → 成纤维细胞激活与瘢痕形成。
对未来治疗的意义
对非专业读者而言,这项研究传达的信息是:肺纤维化不仅仅由失控的免疫细胞驱动;它也是一种血管“触觉”失常的疾病。内皮细胞感知到周围环境变得过于僵硬,开启 PIEZO1 开关,随后释放 IL‑33 这一危险信号,促使邻近的成纤维细胞不断沉积瘢痕。通过把机械力学信号与基因表达之间的链条解析清楚,这项工作突出了多个有前景的靶点——PIEZO1 本身、CAPN2‑STAT3 传导轴以及 IL‑33——用于中断僵硬与瘢痕自我强化循环的治疗策略。尽管仍需更多研究以安全地在人体中调节这些通路,但这一力敏感的内皮轴为应对长期难治的疾病提供了一个新的、以物理学为基础的切入点。
引用: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
关键词: 肺纤维化, 内皮细胞, 机械转导, PIEZO1, IL-33