Clear Sky Science · zh
疟原虫微管蛋白的适应性决定了不同的微管结构、力学特性和药物敏感性
为何疟疾的骨架重要
疟原虫能在人体红细胞内存活,同时又必须穿过蚊子和不同组织。为此,它们依赖一种由显微小管构成的内部支架。本文提出了一个简单却关键的问题:既然构成微管的基本单元与我们细胞中的极为相似,寄生虫的微管如何能变得如此专门化且坚固?答案不仅揭示了寄生虫如何维持形态,还为我们设计只作用于寄生虫骨架而不损害宿主的药物提供了思路。 
塑造致命寄生虫的微小管道
微管是中空的蛋白质管,帮助细胞分裂、运动并维持形状。它们由成对的蛋白单元——微管蛋白(tubulin)构成。在动物、植物和寄生虫中,微管蛋白惊人地相似,这就难以解释为何不同生物的微管外观和行为差异甚大。在疟原虫(Plasmodium falciparum)中,微管形成多样的阵列:有些动态参与细胞分裂,而另一些则是位于寄生虫外膜下的长而刚性的支撑。由于这些结构对寄生虫生长和传播至关重要,它们成为抗疟药物的有吸引力的靶点——尤其在对现有疗法耐药性不断上升的背景下。
以原子级分辨率观察寄生虫微管蛋白
研究者直接从P. falciparum中纯化出微管蛋白,使用高分辨率冷冻电子显微镜观察其组装成微管的方式。他们将这些结构与研究透彻的哺乳动物脑微管进行了比较。乍看之下,寄生虫的微管蛋白与人类版本几乎相同,整体折叠也一致。但仔细比对发现,在关键口袋周围存在一簇小的序列变化,这些口袋是能量分子(如GTP和GDP)结合的位点,也是某些药物作用的位点。这些微妙的变化改变了相邻螺旋和环状结构的位置,尤其是在微管蛋白二聚体表面上其他蛋白和药物结合的区域。研究表明,尽管总体蓝图被保留,寄生虫通过局部微调重新塑造了这些重要位点。
更强的侧向连接带来更刚的管道
微管是聚合体:许多微管蛋白二聚体端对端堆叠形成原丝(protofilaments),数条原丝并列形成管壁。团队发现,寄生虫微管中每条原丝的纵向接触与脑微管非常相似。差异出现在相邻原丝之间的侧向接触。虽然接触面积在寄生虫中实际上略小,但模拟显示这些侧向连接总体上更强,从而使晶格更刚硬。对微管壁片段进行计算建模表明,寄生虫微管蛋白较少弯曲和扭转。对真实微管末端的电子断层扫描证实,寄生虫微管的原丝卷曲更短、张开更少,这是更坚固管道的标志。 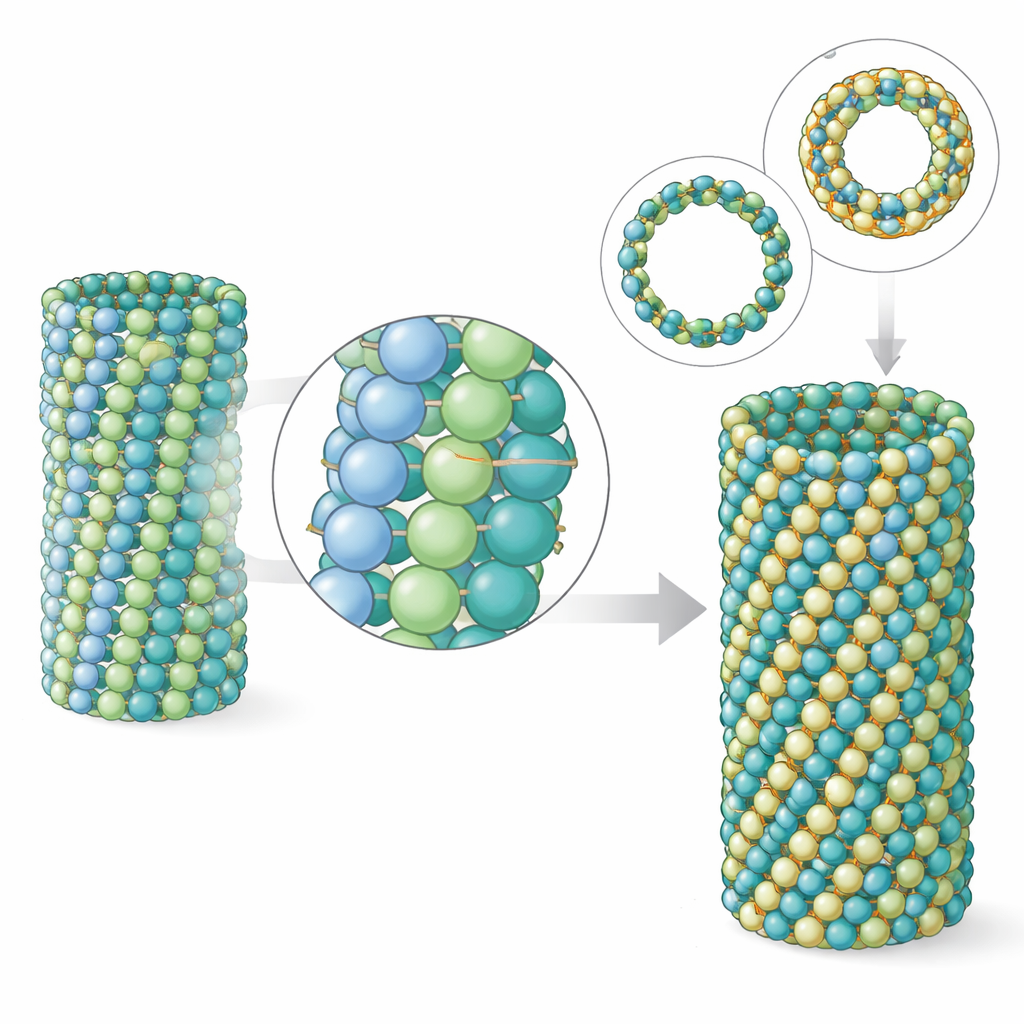
与寄生虫行为相匹配的非同寻常管径
P. falciparum的另一个显著特征是,在某些生活阶段,其微管的周向构成单元数量多于大多数动物细胞常见的13条——常见的是15条甚至17条原丝。团队通过改变组装时使用的核苷酸,在体外重现了这种行为。使用一种类似GTP并稳定生长状态的分子时,寄生虫微管自然偏好形成15原丝微管。作者解析了这些更粗微管的结构,展示了它们如何通过晶格的轻微偏斜来容纳额外的原丝,同时仍保持近乎完美的圆柱形。当他们将这些体外形成的15原丝微管与寄生虫细胞内观察到的管道比较时,形态和尺寸的匹配非常接近,表明这些独特结构主要来源于微管蛋白自身的内在性质,而非大量辅助蛋白的作用。
为未来的寄生虫特异性药物提供线索
研究结论是,进化通过零散的小序列变化调节了寄生虫的微管蛋白,这些变化共同影响微管的力学性能、结构和药物敏感性。这些微调使寄生虫的微管更刚硬,并能形成适应其复杂生活史的非标准管径,同时仍保留基本微管蛋白的可识别外形。对医学而言,某些药物结合口袋在寄生虫与宿主之间几乎相同(如抗癌药紫杉醇作用的部位),说明这些口袋可能不是选择性抗疟药的理想靶点。另一些位点,比如被认为结合类似除草剂的化合物 oryzalin 的区域,则显示出序列变化和细微的结构位移,这可能解释了为何寄生虫微管在这些位点比人类微管更易受损。描绘这些细微差别为设计能够破坏疟原虫骨架而尽量不影响我们自身细胞的未来药物提供了路线图。
引用: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
关键词: 疟疾寄生虫, 微管, 微管蛋白结构, 药物靶向, 冷冻电子显微镜