Clear Sky Science · zh
在福斯曲霉素生物合成中,共价战斗头的组装涉及由双功能硫酯酶催化的丙二酰化-内酯化和酶促去丙二酰化
自然如何构建微小的化学“战斗头”
抗癌药和抗生素的活性常常取决于少数原子以特定方式排列——一个微小的“战斗头”,能够锁定并使蛋白质失去功能。天然化合物福斯曲霉素就是这样的分子,对参与细胞生长的酶具有强效活性。但它复杂的结构使得在实验室中合成或改造十分困难。本研究一步步揭示了细菌如何组装福斯曲霉素关键战斗头,展示了可供化学家借鉴来设计新药的酶学技巧。
强效天然药物中的特殊“钩子”
许多来自土壤细菌的有前途药物属于一类称为聚酮体的家族。在该家族中,有一类携带一种反应性环,化学上称为α,β-不饱和δ-内酯,类似分子层面的鱼钩。它可以与蛋白质中的某些氨基酸形成共价键,关闭关键的生物开关。在福斯曲霉素及相关分子中,这个钩子与一个磷酸基团配对,帮助它们定位并抑制控制细胞分裂的特定酶。这些特征使它们成为有吸引力的抗癌先导物,但同样的反应性和结构复杂性也使它们难以合成并在储存中不稳定。
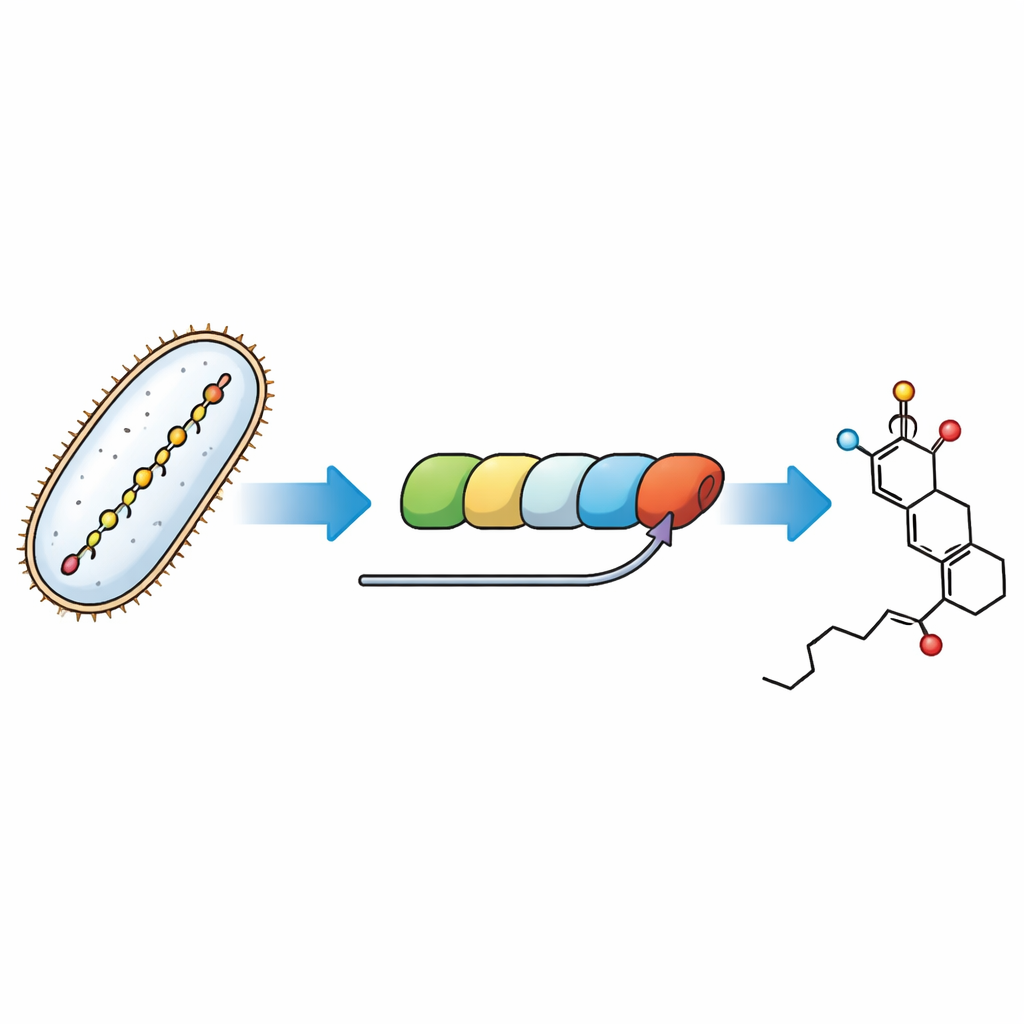
追踪分子装配线的最后几步
细菌使用一种巨大的模块化蛋白机器——聚酮体合酶来构建福斯曲霉素——这是一个装配线,每个站位延长并塑造不断增长的碳链。这里要解决的难题是,该机器的最后一个模块如何锻造战斗头环并安上一个临时的“手柄”称为丙二酰基(malonyl),而该手柄随后必须被移除。通过在试管中用纯化酶和为天然中间体精心设计的小分子替代物重构这一路径,研究人员得以观察各个步骤并将其归因于装配线的特定部位。
具有出乎意料才能的多任务酶
团队发现,装配线的最后站位——名为FosTE的结构域——表现出此前未见的行为。典型的此类结构域仅在装配线上切下完成的产物。相反,FosTE首先从一种常见的细胞构建块中夺取一个丙二酰片段并将其转移到不断增长链条的特定位点的氧原子上,然后帮助链条弯曲闭合形成战斗头环。将FosTE中的一个反应性丝氨酸氨基酸突变会同时关闭这两种活性。结构建模指出,活性位点中两个带正电的精氨酸残基托举并定位丙二酰片段以便转移——这些功能通常由另一类酶来完成。将这些精氨酸改为中性残基会抹去丙二酰转移步骤,同时基本的环形成大体保留,证实了它们的关键作用。
固化战斗头并防止物料浪费
一旦环形成并携带了临时的丙二酰基,另一种酶FosM必须去除该基团以揭示完全武装的战斗头。研究表明,只有在另一种具有广泛底物特异性的激酶FosH先向分子上邻近位置添加磷酸后,FosM才高效工作。当研究人员单独将丙二酰化的环提供给FosM时,仅观察到适度的转化。先添加FosH则几乎完全去除了丙二酰基并形成最终的活性单元。重要的是,FosH还能够对那些由侧反应产生的相关“旁路”中间体进行磷酸化,从而挽救它们,使其能被正确处理,而不是成为无法挽回的失活产物。
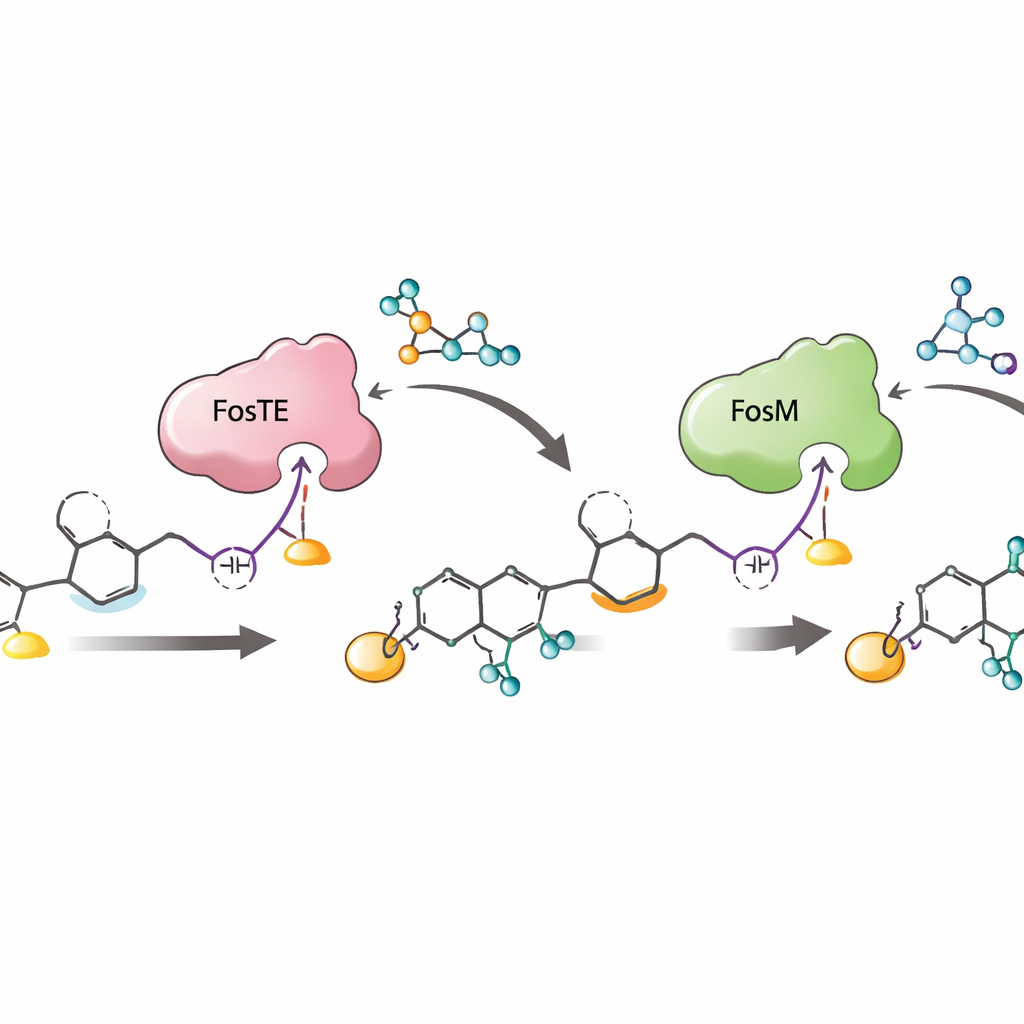
为何这种酶促协同至关重要
综上所述,这项工作展示了一个紧密编排的顺序:装配线上的链伸长、由FosTE驱动的丙二酰加入与环闭合、FosH的磷酸化,以及最终由FosM触发的丙二酰去除。这个顺序不仅高效地构建了脆弱的战斗头,还保护了不稳定的中间体免于崩解,并最大化生成以磷酸化形式存在的目标产物——这种形式作为药物先导最为活跃。通过揭示单个酶结构域如何既修饰又释放增长中的分子,以及协作酶如何微调并拯救反应性中间体,研究为工程化带有战斗头的聚酮体以及为像福斯曲霉素这样的复杂抗癌剂建立更短、更高效的合成路线提供了蓝图。
引用: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
关键词: 福斯曲霉素, 聚酮体生物合成, 酶工程, 天然产物反应基团, 化学-酶合成