Clear Sky Science · zh
通过tRNA修饰的氧化去硫作用调控翻译
细胞在压力下如何调节蛋白质产量
每个细胞都必须决定制造哪些蛋白、以多快的速度制造以及何时放慢脚步。本研究揭示了一种存在于转运RNA(tRNA)分子上的微妙化学开关,它在细胞环境变得更具氧化性时(例如在炎症或代谢应激期间)帮助细胞降低蛋白质合成速率。通过在哺乳动物细胞和体外体系中观察该开关的行为,研究者们发现了一种新的机制:看似类似损伤的RNA化学改变实际上可以充当一种调控信号。
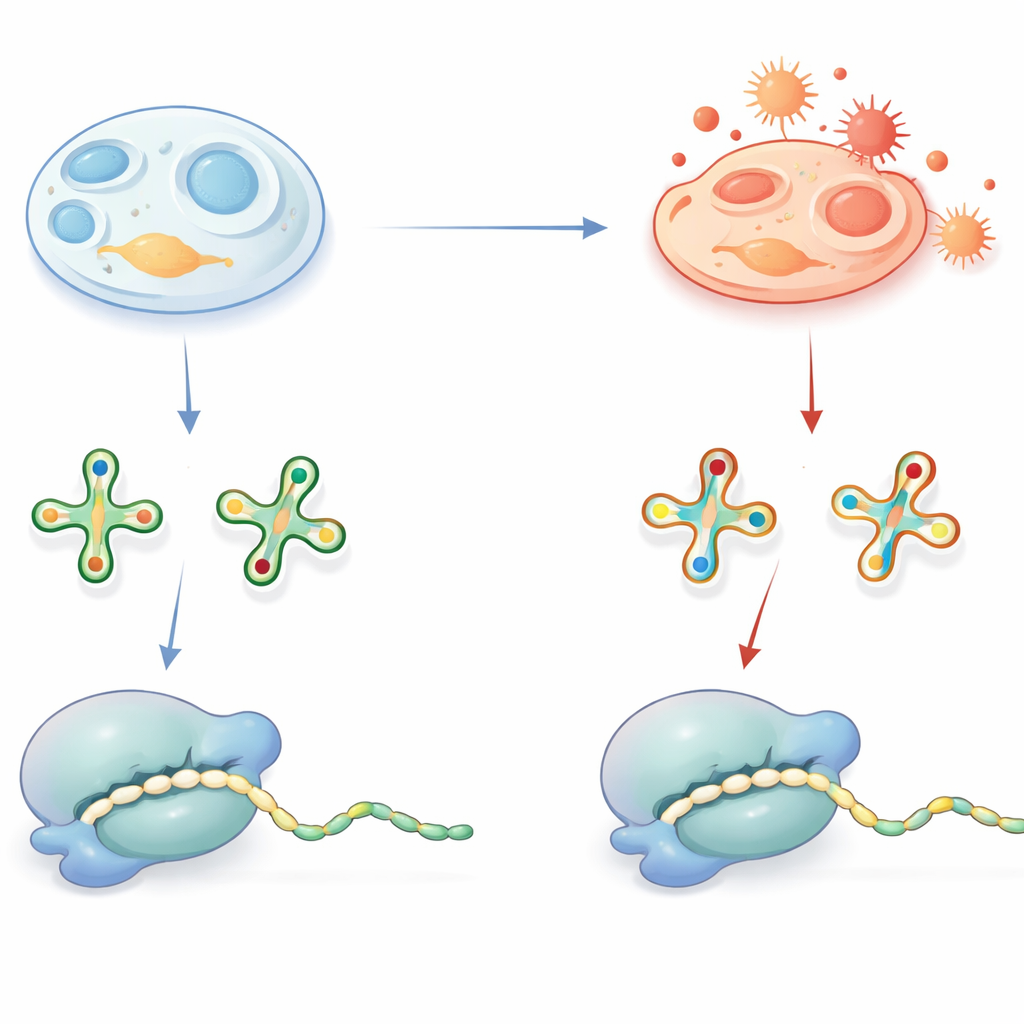
tRNA上细小的标记却有重大影响
tRNA作为适配体,读取信使RNA中的三字“词”并在蛋白质合成过程中递送对应的氨基酸。为确保这一过程准确且高效,许多tRNA携带特殊化学修饰,尤其是在与密码子第三位接触的关键位置。一个广泛存在的修饰是在尿嘧啶碱基上的含硫基团,通常记为2-硫尿苷衍生物。在健康状态下,这个硫基团有助于tRNA识别以A或G结尾的正确密码子,并支持快速且低错误率的翻译。已知这些修饰的缺陷会导致人类疾病,凸显了它们的重要性。
当氧化应激改写tRNA时
增强解码能力的硫基团也有弱点:它化学上易被氧化。研究团队探讨了在细胞内,这一基团是否在氧化条件下被剥离,以及这对蛋白质合成意味着什么。通过敏感的质谱分析,他们在小鼠组织、猪线粒体、细菌、酵母和多种人类细胞系中鉴定出了氧化的、无硫的这些tRNA碱基——称为h2U衍生物。一个巧妙的外加细菌tRNA示踪实验表明,这些h2U标记并非样品制备过程中产生的伪像,而是在活细胞内形成的。尽管氧化形式只存在于部分tRNA中,但其丰度在组织和细胞类型间有所差异,表明细胞的氧化还原状态和抗氧化能力会影响这种转化发生的频率。
氧化tRNA如何减缓合成线
研究者接着测试了这些改变后的tRNA在蛋白质合成中的表现。他们将大量tRNA中的含硫形式化学转化为氧化的h2U形式,并在完全重组的人类翻译体系中进行体外试验。一个强烈依赖这些修饰tRNA的报告蛋白在tRNA去硫化后产量显著下降,而一个回避被影响密码子的对照报告蛋白则翻译正常。生化测定揭示了原因:用于赖氨酸、谷氨酰胺和谷氨酸的氧化tRNA的氨基酰化效率大大降低,而对应的精氨酸tRNA则基本不受影响。值得注意的是,携带h2U的tRNA仍可在细胞的核糖体结合(多核糖体)分馏中被检测到,表明它们确实参与翻译,但效率较差。
削弱解码的结构视角
为了确切观察氧化如何改变解码,团队使用高分辨率冷冻电镜对携带人类赖氨酸tRNA并被特定密码子程控的细菌核糖体进行成像。在正常的含硫状态下,tRNA“摆动位点”上的修饰碱基能与以A结尾的密码子形成标准碱基配对,或与以G结尾的密码子形成特殊的摆动配对,二者均牢固嵌入核糖体的解码中心。去硫化后,同一碱基与以A结尾的密码子只能形成一个较弱的接触,并且与以G结尾的密码子形成的摆动配对也不稳定。结合实验与这些结构相一致:氧化的赖氨酸tRNA基本丧失识别AAA密码子的能力,并且识别AAG密码子的效率也大幅下降。总体来看,这些发现表明,一个看似微小的化学调整可以导致对特定密码子的翻译减速。
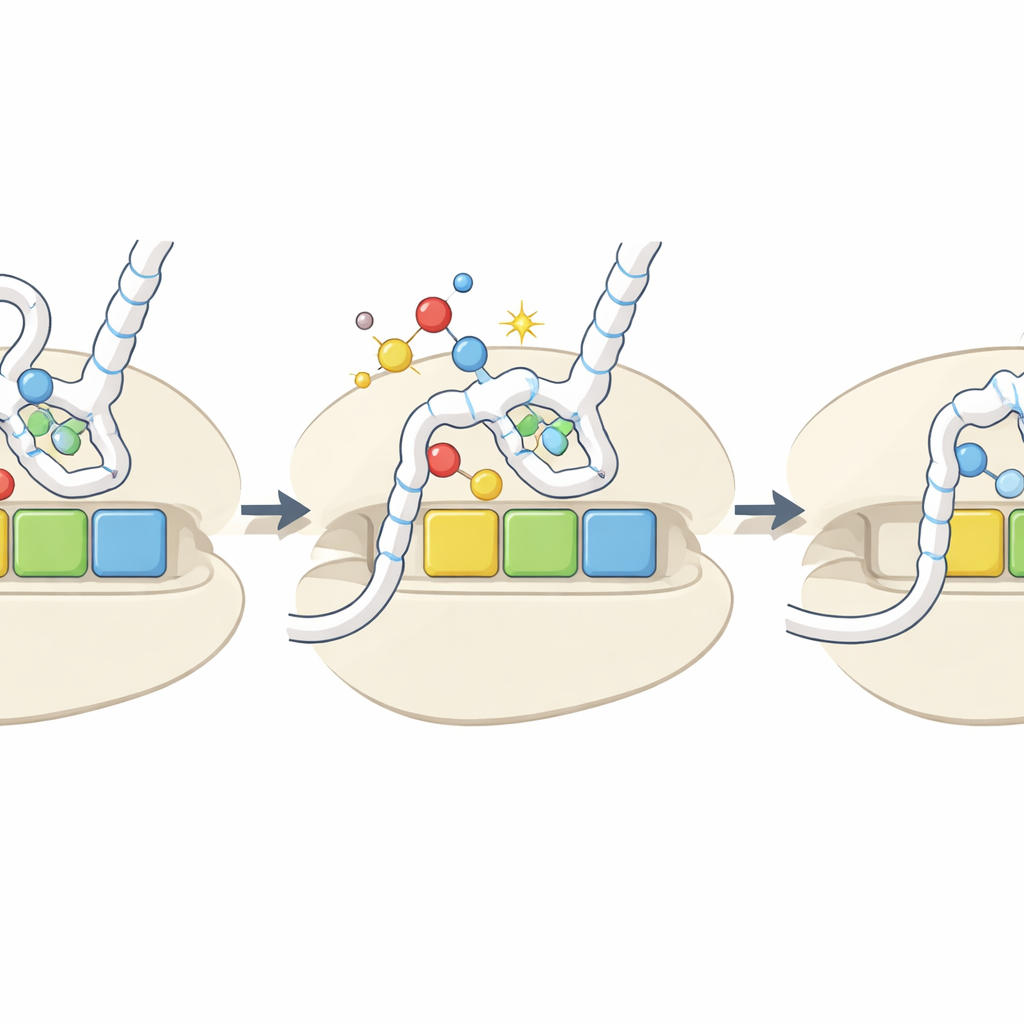
由损伤信号转为调控旋钮
总体而言,该研究提出:在关键tRNA碱基上氧化性地去除硫是细胞氧化还原环境的内置感应器。在氧化应激下,更多tRNA被转化为h2U形式,这些tRNA氨基酰化效率低并且与某些密码子结合较弱。这种选择性减慢这些密码子的翻译,可能改变受影响mRNA的稳定性、改变蛋白质折叠方式,并在核糖体停滞时触发应激反应通路。尽管这些氧化标记相对罕见且在实验性应激下并不总是显著上升,但它们具有密码子和氨基酸特异性的效应,这意味着即使是适度的变化也可能重塑在困难条件下哪些蛋白被合成以及合成的速率。
引用: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
关键词: tRNA修饰, 氧化应激, 蛋白质合成, 翻译调控, RNA损伤