Clear Sky Science · zh
靶向tRNA依赖的酪氨酸使用揭示肝细胞癌的代谢脆弱性
剥夺癌细胞一种常见构件
像所有快速分裂的细胞一样,肝癌细胞需要稳定供应的氨基酸——蛋白质的小型构件。该研究揭示,最常见的肝癌类型肝细胞癌有一个意想不到的弱点:它在能量产生和存活上高度依赖氨基酸酪氨酸。通过选择性限制癌细胞使用酪氨酸的方式,研究人员能够减缓肿瘤生长、破坏癌细胞的能量工厂,并触发一种可用于新疗法的细胞死亡形式。
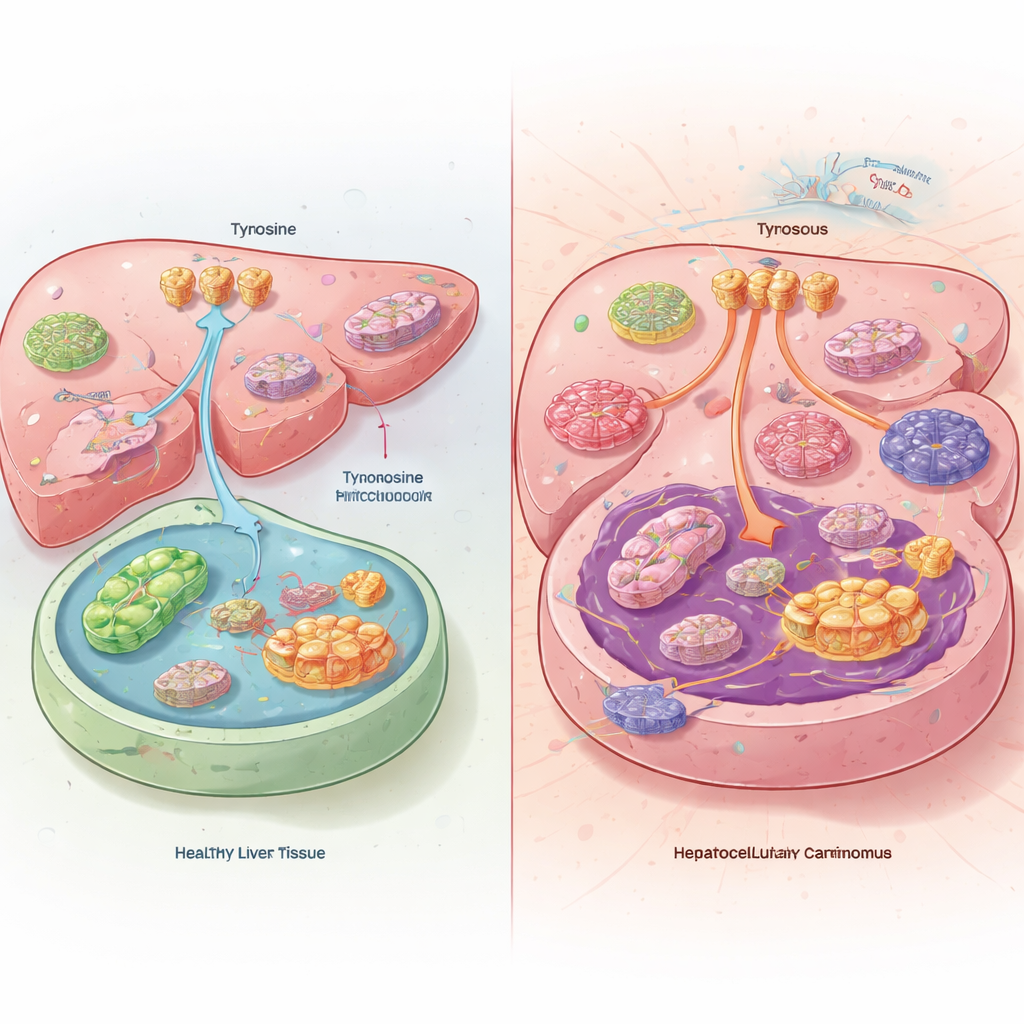
肝肿瘤中隐藏的不平衡
当研究团队将患者和小鼠的肝肿瘤与健康肝组织比较时,发现了一些令人困惑的现象。在癌细胞内,酪氨酸水平实际上偏低,尽管肿瘤从血液中摄取更多酪氨酸并减少其分解。肝肿瘤并没有将酪氨酸作为燃料燃烧,而是将其改道用于蛋白质合成。癌细胞通过增加细胞表面酪氨酸转运蛋白的活性并抑制肝脏中通常降解酪氨酸的酶来实现这一点。食用无酪氨酸饮食的小鼠肿瘤更小、寿命更长,而饮食中额外的酪氨酸则使其肿瘤生长更快。
癌细胞如何重编蛋白质合成
研究人员将这种对酪氨酸的“饥渴”追溯到一个强效的癌基因MYC。在肝肿瘤中,MYC开启了一种名为YARS1的蛋白,它将酪氨酸连接到特定的转运RNA(tRNA‑TyrGUA)上。被载入的tRNA正是核糖体构建富含酪氨酸蛋白所需的物质。研究显示,肝癌同时提升了YARS1及其对应tRNA的水平,确保了一条将酪氨酸优先输送到蛋白质合成中的通道。干扰这条通道——无论是降低酪氨酸水平、敲低YARS1或tRNA‑TyrGUA,还是阻断酪氨酸的加载——都会使肝癌细胞在细胞培养和小鼠体内明显失去活性,揭示出与其高蛋白质合成需求紧密相关的代谢脆弱性。
削弱能量工厂与脂质平衡
通过结合全基因组的RNA、蛋白质合成和代谢物测量,团队确定了两种对酪氨酸限制尤为敏感的靶点。一种是NDUFB8,它是线粒体复合体I的组成部分,复合体I是细胞能量生成机器的核心。另一种是SCD1,它有助于将饱和脂肪转换为更易于在细胞膜和脂滴中安全储存的单不饱和脂肪。当用于翻译的酪氨酸受限时,NDUFB8和SCD1的产量下降,而它们的RNA水平基本保持不变——这清楚表明受影响的是翻译而非基因表达。这导致复合体I装配不良、细胞呼吸下降、活性氧增多,以及脂质从单不饱和向更易氧化的多不饱和形式转变。
将癌细胞推向一种铁依赖的死亡
线粒体损伤与不稳定脂质的叠加促使肝癌细胞走向铁死亡,这是一种由脂质过氧化驱动的铁依赖性细胞死亡方式。肿瘤试图通过上调天然的铁死亡阻断因子(如GPX4及相关分子)进行反击,但一项大规模CRISPR基因编辑筛选显示,禁用这些保护者会使酪氨酸限制变得更加致命。在细胞和小鼠模型中,将限制酪氨酸的策略与抑制GPX4或BCL2的药物——或与现有的肝癌药物如索拉非尼和维奈托克斯联合使用——能够产生更强的肿瘤控制、更小的肿瘤负担和更长的生存期。
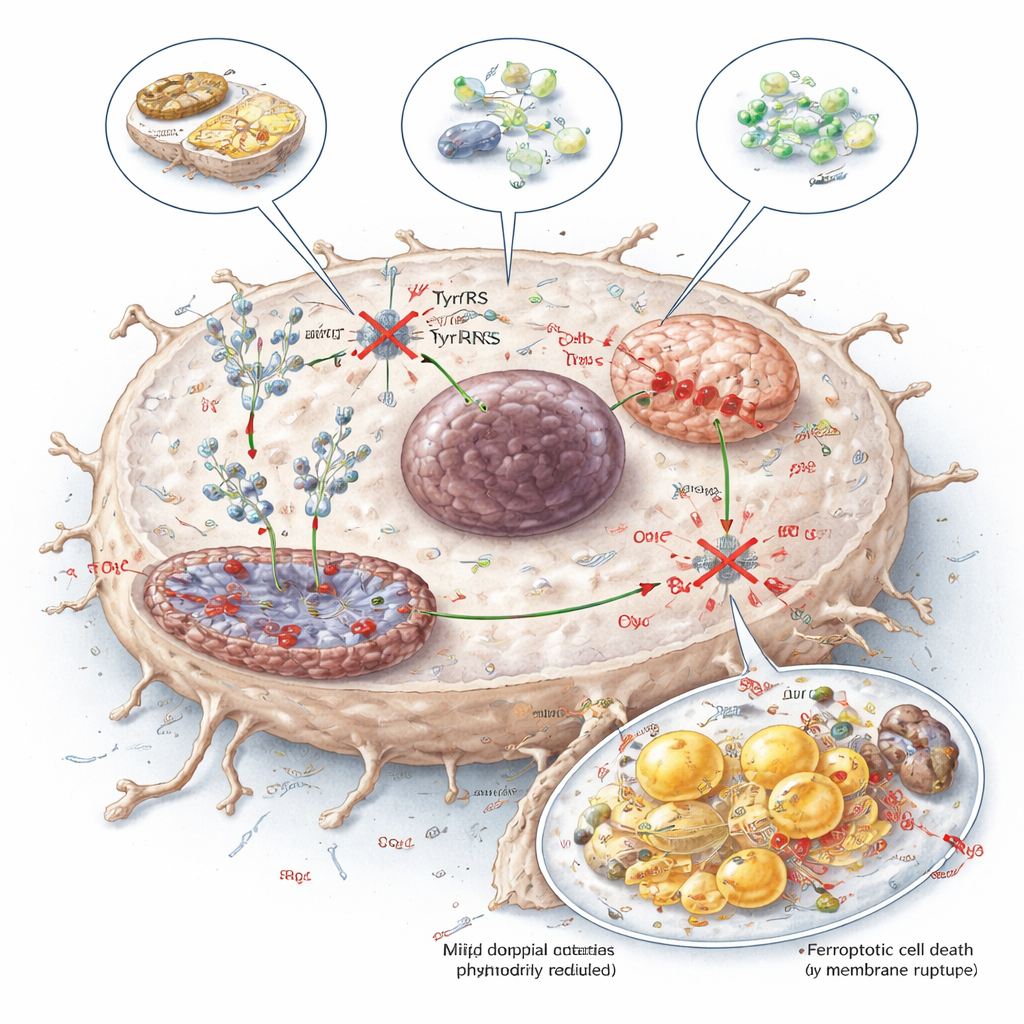
把代谢弱点变成治疗策略
为探索利用这一弱点的可行方法,研究团队测试了三种途径:酪氨酸受限饮食、一种能酶解酪氨酸的酶(TAL),以及一种名为酪氨醇的小分子,它与酪氨酸竞争结合YARS1。这三种方法都减少了用于蛋白质合成的酪氨酸可用性,降低了NDUFB8和SCD1水平,损害了线粒体功能,并在肝肿瘤中增加了铁死亡,同时在小鼠的正常组织中显示出可控的影响。对非专业读者来说,结论是肝癌似乎不仅把酪氨酸当作营养物质,而是将其作为其蛋白质制造机器的精确燃料。通过饮食、酶或药物靶向这种依赖,为削弱肿瘤并增强现有治疗的效果提供了一条有希望的新途径。
引用: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
关键词: 肝癌, 氨基酸代谢, 酪氨酸, 线粒体, 铁死亡