Clear Sky Science · zh
通过系统识别变体特异性RNA结构-小分子相互作用,以RNA G-四链体为例
微小的RNA变化为何对未来药物至关重要
我们大多数人都继承了使个体独特的小小DNA差异。这些微小变化会细微地重塑细胞内RNA分子的折叠。新研究提出了一种方法,用以观察这些遗传微调如何改变靶向RNA的实验性药物的结合方式。之所以重要,是因为同一种药物在不同人身上可能表现大相径庭,尤其是在癌症或遗传性疾病中。
一种新的方法来观测药物与RNA的接触点
许多药物开发者现在把目标从仅限蛋白质扩展到RNA。小分子可以附着在特殊的RNA构象上并影响基因的解读,但直到现在大多数方法仅能在单一“参考”RNA序列上工作,基本忽略了真实患者中存在的无数单字母变异。作者建立了一种高通量方法,称为BIVID-MaP,能够同时测试成千上万的RNA变体,并以单核苷酸分辨率定位每个变体上小分子的结合位点。 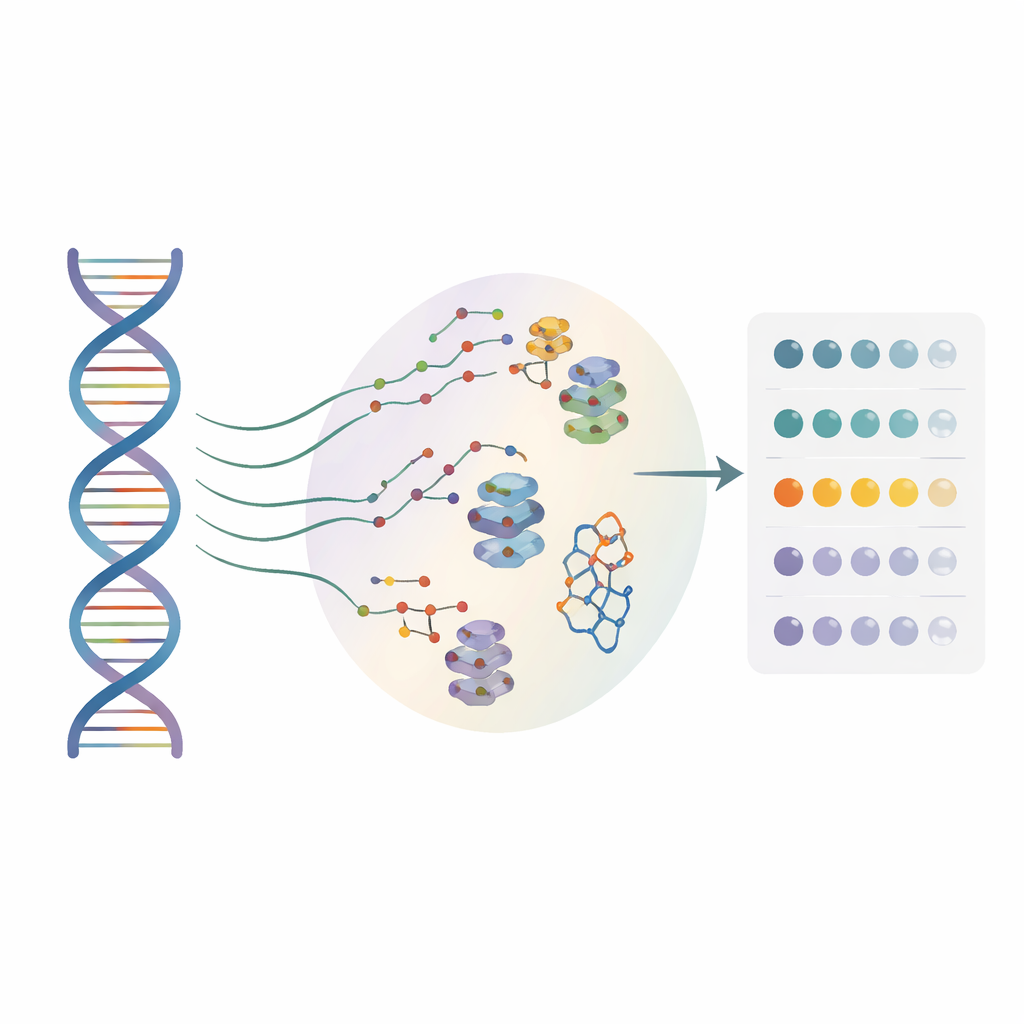
将化学标记转成可读信号
BIVID-MaP由三大步构成。首先,团队把一个反应性标记连接到能结合RNA的小分子。当该带标记的化合物嵌入其偏好的RNA结构(例如由富含鸟嘌呤的序列形成的紧凑G-四链体)时,标记会与附近的RNA碱基形成永久的化学键。其次,一种特殊酶将被修饰的RNA复制为DNA。当遇到这些化学标记时,酶往往会“跳过”一个碱基,在拷贝中产生微小缺失。第三,深度测序读出数百万分子上的这些缺失特征。由于周围的大部分序列得以保留,这些缺失可以被准确地分配到混合池中的特定遗传变体上。
在受控范例上验证该方法
为确认BIVID-MaP确实能检测到变体特异性结合,研究者研究了来自CD44基因的一段RNA,该段通常形成G-四链体。一个G到A的单核苷酸替换会破坏该结构。在同时包含两种版本的混合物中,只有完整构象在暴露于基于小檗碱的探针时,在折叠区域附近显示出强烈的缺失信号,独立实验也证实了该处更强的结合。不能形成相同构象的突变体则产生明显更少的缺失和更弱的结合。其他常用的映射技术要么错过了这一差异,要么产生混淆的背景噪声,凸显了新方法在敏感性和特异性上的改进。
扫描与癌症相关的多基因突变
随后团队进行了放大实验。他们构建了一个由283个与癌症相关基因的5′非翻译区(5′ UTR)组成的RNA文库,每个序列都配对包含肿瘤中报道的真实体细胞突变。使用识别类似G-四链体结构的探针,BIVID-MaP发现了大量突变,这些突变要么强化要么削弱了小分子的结合。在诸如DAXX和ING2等基因中,富含鸟嘌呤片段中的单字母变化显著改变了结合,这与关于G-四链体形成的独立生物物理学测试以及通过质谱进行的直接结合测量结果一致。在某些情况下,位于显性G序列之外的突变仍通过微妙改变邻近碱基配对的可能性来改变结合,从而重塑结构“集合体”,而不必对预测的整体折叠进行显著改变。 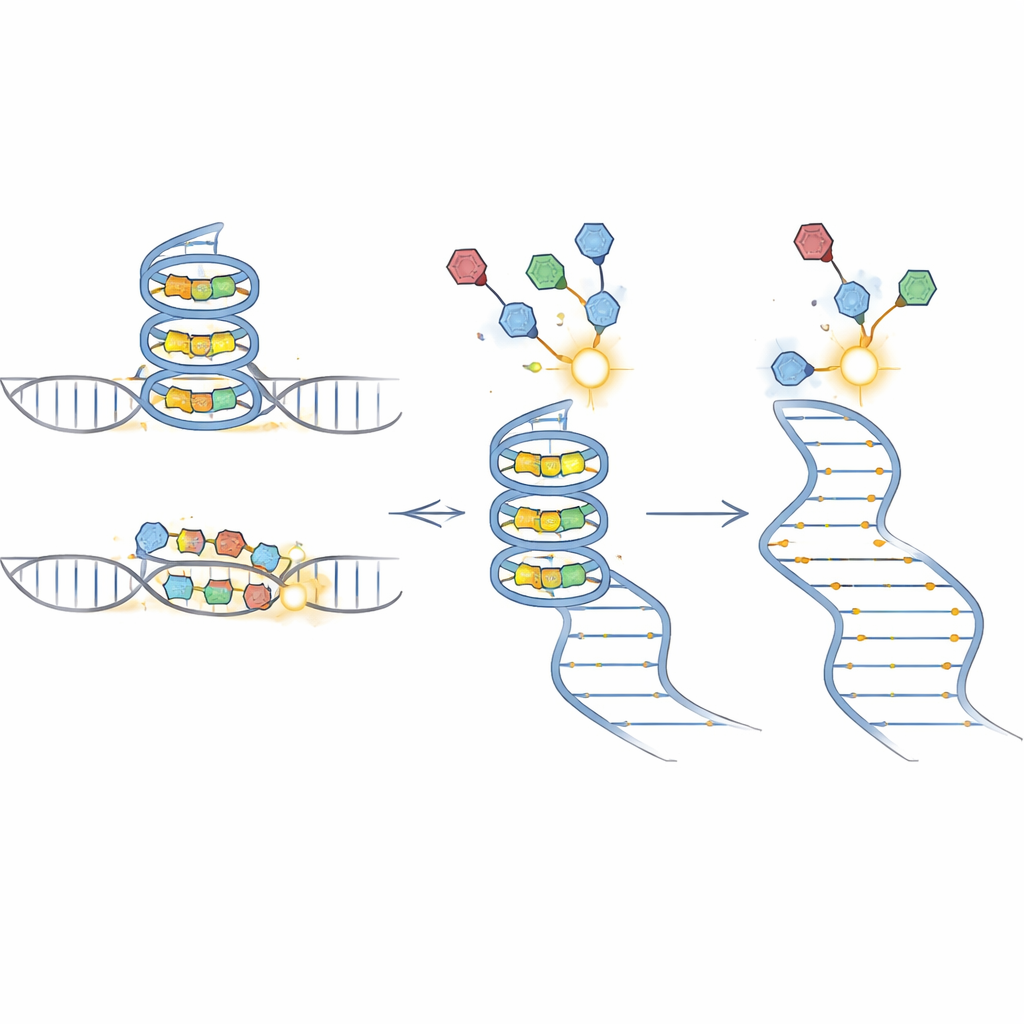
弥补计算预测的盲点
重要的是,现有的RNA结构和G-四链体预测工具经常无法预见BIVID-MaP揭示的变化。一些在计算评分上几乎无显著变化的变体,在现实中却引起了大的结合差异。另一些变体似乎影响了一类针对G-四链体的小分子结合,而某些突变则具有药物特异性的效应。这表明单核苷酸变体可以以难以单从序列推断的方式调节RNA折叠和药物接触的景观。
对个性化RNA药物的意义
作者总结称,BIVID-MaP为绘制个体遗传差异如何重塑RNA结构及其与小分子药物相互作用提供了强有力的途径。通过将局部化学修饰转化为精确的缺失特征,该方法可并行筛查数千个变体并突出那些显著改变药物结合的变体。从长远看,这类图谱可以指导更有效、更安全且适用于多样化患者群体的靶向RNA药物设计,并揭示先前隐藏的可能作为新药物靶点的RNA结构。
引用: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
关键词: 针对RNA的药物, G-四链体, 遗传变体, 小分子结合, 癌症突变