Clear Sky Science · zh
亚细胞蛋白质组学揭示锥虫类动物 Angomonas deanei 中内共生体整合的蓝图
单细胞生命中的隐秘伙伴
许多单细胞生物实际上并不真正独处。一些宿主细胞内长期寄居着细菌,彼此交换营养和服务,这种关系回响着我们线粒体起源的情形。本文研究了昆虫微小寄生菌 Angomonas deanei 中这种伙伴关系,揭示了曾经的自由生活细菌如何深度嵌入宿主细胞的内在运作。
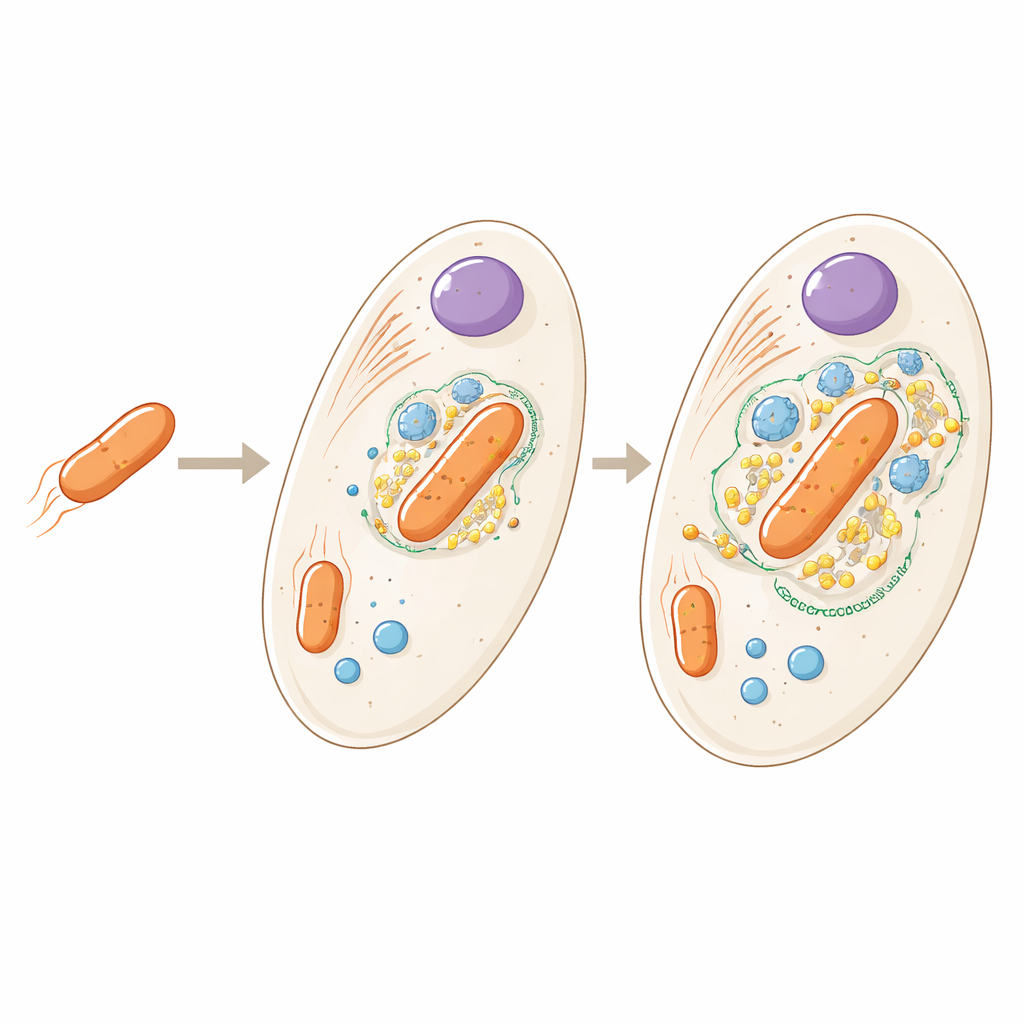
从住客到内置部件
生活在 Angomonas deanei 细胞内的细菌与自由生活的土壤微生物有较远的亲缘关系,但在宿主中以每个细胞仅一份的形式存在,已不再能独立生存。早期研究显示,宿主会合成特定蛋白质并导入该细菌,甚至参与控制其分裂。新研究提出了更广泛的问题:把整个细胞放在一起看,所有宿主和细菌的蛋白质究竟分布在哪里?这些分布又能告诉我们双方融合得有多紧密?
绘制细胞内部的城市地图
为了解答这一问题,研究者以极其温和的方式破碎大量细胞,使内部结构大致保持完整。随后通过不同速度的离心将这些片段分离,并用高分辨率质谱鉴定每个组分中的数千种蛋白质。通过比较蛋白质在各组分间的聚类情况,并与已知标志物和荧光显微镜成像交叉验证,他们建立了一个详尽的“地址簿”,将近 3,000 种蛋白质分配到 21 个不同区室,例如细胞核、线粒体、专门的储存体以及细菌内共生体本身。
宿主工具指向共栖细菌
在这份图谱中,团队发现了一组始终与内共生体共同出现的宿主产物蛋白,扩充了已知的“靶向内共生体蛋白”名单。其中一个新确认的例子,命名为 ETP10,像先前发现的某蛋白一样覆盖在细菌表面,暗示宿主因子可能在微生物周围形成支架。另一小类蛋白在物理行为上与已知在细菌分裂时起夹紧作用的动力蛋白样蛋白类似。总体而言,这些发现提示存在一套专门的宿主构建的机械装置,用于定位、塑形并复制细胞内的内共生体。
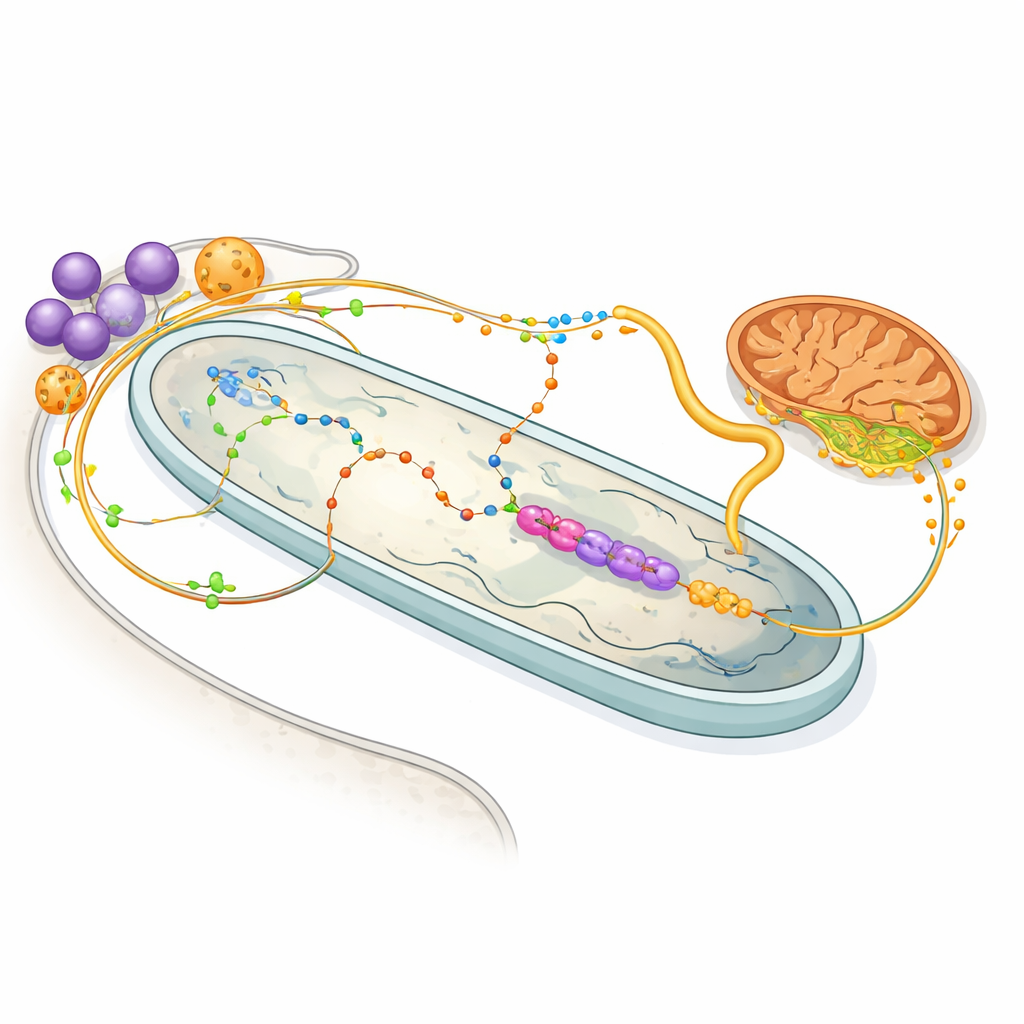
能量共享与化学贸易路线
蛋白质图谱还揭示了宿主与细菌之间繁忙的分子交换。宿主的糖体(glycosome)——负责糖类和氨基酸代谢的细胞器——中的酶似乎被调整为向细菌提供脯氨酸和 2-氧代戊二酸(2‑oxoglutarate),两者都是重要的能量来源。细菌内部则保留了一套精简的酶系,利用 2‑氧代戊二酸生成 NADH,驱动简化的呼吸链,然后将延胡索酸(succinate)传回宿主的线粒体。其他途径显示细菌承担了合成血红素的大部分步骤——血红素是宿主所需的重要色素——同时为核苷酸合成提供关键构件。实际上,双方各自将特定代谢任务外包给对方,共同形成了一个共享且相互依赖的体系。
细胞内的新型交流通道
除了代谢层面,研究还揭示了内共生体与其他细胞器之间的物理联系和可能的信号联络。一组独特的宿主蛋白形成了作者所称的“接触位点”簇,这些簇富集了核包膜和内质网成分,并在离心分布上与细菌共同沉降。两类储存细胞器——糖体和酸性多磷酸体(acidocalcisome)——出现了两种群体:一部分独立分布于胞质,另一部分则始终随同细菌。显微镜证实这些细胞器的子集紧贴内共生体排列。酸性多磷酸体是已知的钙和磷酸盐储库,其紧密接触暗示存在双向的信号与离子交通路线,将细菌、这些储存体和邻近的内质网连接起来。
生命内融合的蓝图
综合来看,这项工作提供了一个丰富的细胞级蓝图,说明细菌如何在功能上与宿主融合,而尚未演化为像线粒体那样的完全部分化细胞器。Angomonas deanei 依赖其内共生体提供关键营养,而细菌反过来依赖宿主合成的蛋白质和富能分子,并通过与宿主细胞器的连接获得通信与调控。对非专业读者而言,结论是:进化可以逐步将不同生命形态的合作硬化为不可分割的体系,一步步走向无法分离。该系统提供了这一过程的活体快照,帮助科学家更好地理解像我们细胞这样的复杂细胞如何从更简单的起点逐渐出现。
引用: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
关键词: 内共生, 细胞代谢, 细胞器进化, 原生生物学, 宿主-微生物相互作用