Clear Sky Science · zh
通过超深度长读长测序揭示异质耐药大肠杆菌群体中遗传串联扩增的动态分布
隐藏的生存口袋
当医生用抗生素治疗细菌感染时,通常假定整群微生物会有相同反应。但有时,极小的一部分群体会悄然耐受、在治疗中幸存,并为治疗失败或复发埋下伏笔。本研究揭示了在大肠杆菌中这些稀有幸存者如何产生并随时间变化,并引入了一种能够逐个细胞观察这些遗传变化展开的强大方法。
小的基因重复,巨大的后果
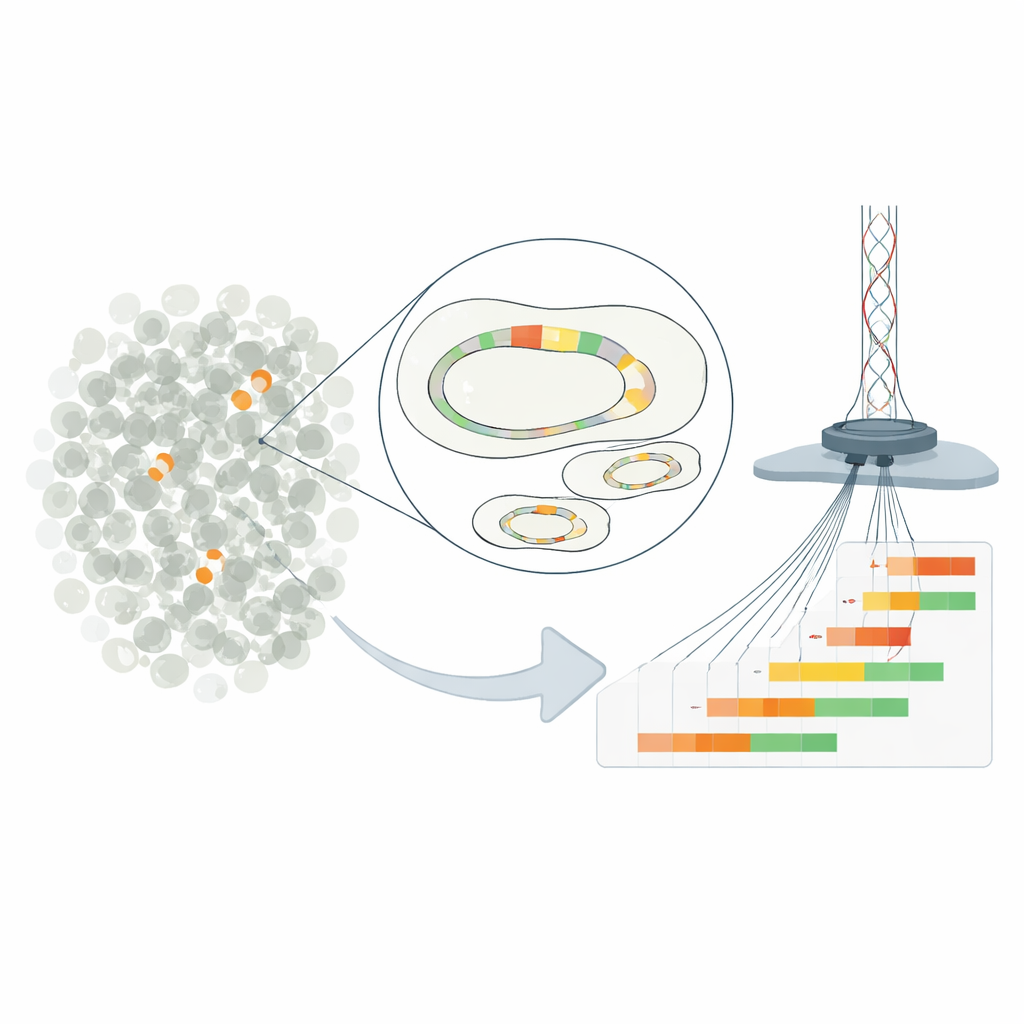
研究聚焦于“异质耐药性”,即样本中大多数细菌看似对药物敏感,但一小部分个体可承受远高于常规剂量的情况。在所研究的大肠杆菌菌株中,这种行为源于位于质粒上的耐药基因重复拷贝——质粒是独立于主染色体的小型环状DNA。通过重复包含β‑内酰胺酶基因的短片段,细菌能够增加分解抗生素哌拉西林‑他唑巴坦的酶的产量。单个细胞携带的重复次数越多,产生的酶越多,在药物存在下的存活几率也越高。
前所未有地读取DNA环
传统方法只能估算整个细菌群体的平均基因拷贝数,从而掩盖了单个细胞间的丰富多样性。为了解决这一问题,研究者对临床质粒进行了工程化改造,使其可以在精确位置被切割并从染色体中分离出来。他们使用超深度的纳米孔长读长测序读取完整质粒分子,从头到尾精确计算每个质粒包含的耐药单元重复次数。该方法的分辨率达到十万分之一,发现同一培养物中共存着从零拷贝到十几拷贝的质粒。与其他技术的比对验证了该新方法在平均拷贝数报告上的准确性。
抗生素如何重塑群体
利用这一工具,团队追踪了将大肠杆菌培养物暴露于不断升高的哌拉西林‑他唑巴坦剂量随后撤药时的变化。随着抗生素浓度上升,整体分布向携带更多耐药基因拷贝的质粒移动,但携带较少拷贝的细胞从未完全消失。当撤去药物并让细菌在数百代内生长时,群体仅缓慢回漂向较低拷贝数,并且从未完全回到初始状态。单独的生长测试显示,每增加一个基因拷贝就会使药物耐受性出现可测的阶梯式提升,将观察到的遗传分布与标准实验室检测中可见的异质耐药模式紧密关联。

邻居的保护与隐秘代价
为了解释为何低拷贝细胞在强烈药物作用下仍能存续,作者构建了一个结合细菌生长、抗生素降解及随机增加或减少基因拷贝事件的数学模型。模拟显示,“间接耐药”发挥了关键作用:高抗性的细胞分泌足量的β‑内酰胺酶,降低共享环境中的药物浓度,顺带保护了耐药性较低的邻居。只要额外基因拷贝在无药物条件下仅带来很小的生长代价,这种保护效应就能维持宽广的拷贝数分布,减缓群体回归到完全敏感状态的速度。模型还显示,对培养基的常规适应——即与耐药无关但提高生长的突变——可以使某些亚群体更适应,从而锁定特定的拷贝数状态。
这对患者及更广泛领域的意义
对非专业读者而言,结论是细菌培养物并非一个单一、均质的敌人:它是一个不断变化的个体集合,个体间在生存抗药能力上存在差异。通过直接在数千条单一DNA分子上计数基因拷贝,本研究以定量方式将这种隐匿多样性与临床相关的耐药性联系起来。这些见解可改进基因组测序在预测难以检测的异质耐药性时的应用,帮助识别更可能导致治疗失败的细菌菌株,并指导更好的诊断测试。由于串联基因扩增也驱动病毒、肿瘤及其他生物的快速适应,同样的策略可超越大肠杆菌被推广应用,为理解重复DNA片段如何帮助生命体规避威胁提供新的视角。
引用: Jonsson, S., Guliaev, A., Berryhill, B.A. et al. The dynamic distribution of genetic tandem amplifications in a heteroresistant Escherichia coli population revealed by ultra-deep long read sequencing. Nat Commun 17, 2113 (2026). https://doi.org/10.1038/s41467-026-70044-8
关键词: 抗生素异质耐药性, 基因扩增, 大肠杆菌, 长读长测序, β‑内酰胺酶