Clear Sky Science · zh
单分子动力学显示仅ATP结合就能驱动ABC转运蛋白的底物易位
为何这些微小的细胞泵重要
你体内的每个细胞都依赖将分子穿膜搬运的微观机械,这些机械决定了从营养物质摄取到免疫防御等诸多过程。一类主要的机器称为ABC转运蛋白,它利用细胞的化学燃料ATP将货物往高势能方向推动,即逆着自然梯度运输。然而几十年来,科学家们对一个基本问题存在争论:仅ATP的结合动作是否就能为转运步骤提供动力,还是必须等到ATP被水解才释放能量?本研究通过分子层面的观察,一步步解决了这一争论。
逐个观察转运蛋白
研究者没有去测量数百万分子的集体行为,而是搭建了一个能实时追踪单次转运事件的系统。他们聚焦于TmrAB——一种与人类TAP转运蛋白同源的细菌蛋白,后者负责将免疫肽传送以供杀手T细胞识别。TmrAB镶嵌在膜中,利用ATP将短肽段从一侧运输到另一侧。为了看到每一次转运步骤,团队将单个TmrAB分子困在人工膜泡(脂质囊泡)中,并在囊泡内封入一款经过工程改造的“传感器”蛋白,该蛋白在捕获肽时会改变其荧光信号。借助高灵敏显微镜,他们能够通过光信号的短时跃变,精确看到一个接一个肽分子进入囊泡的瞬间。
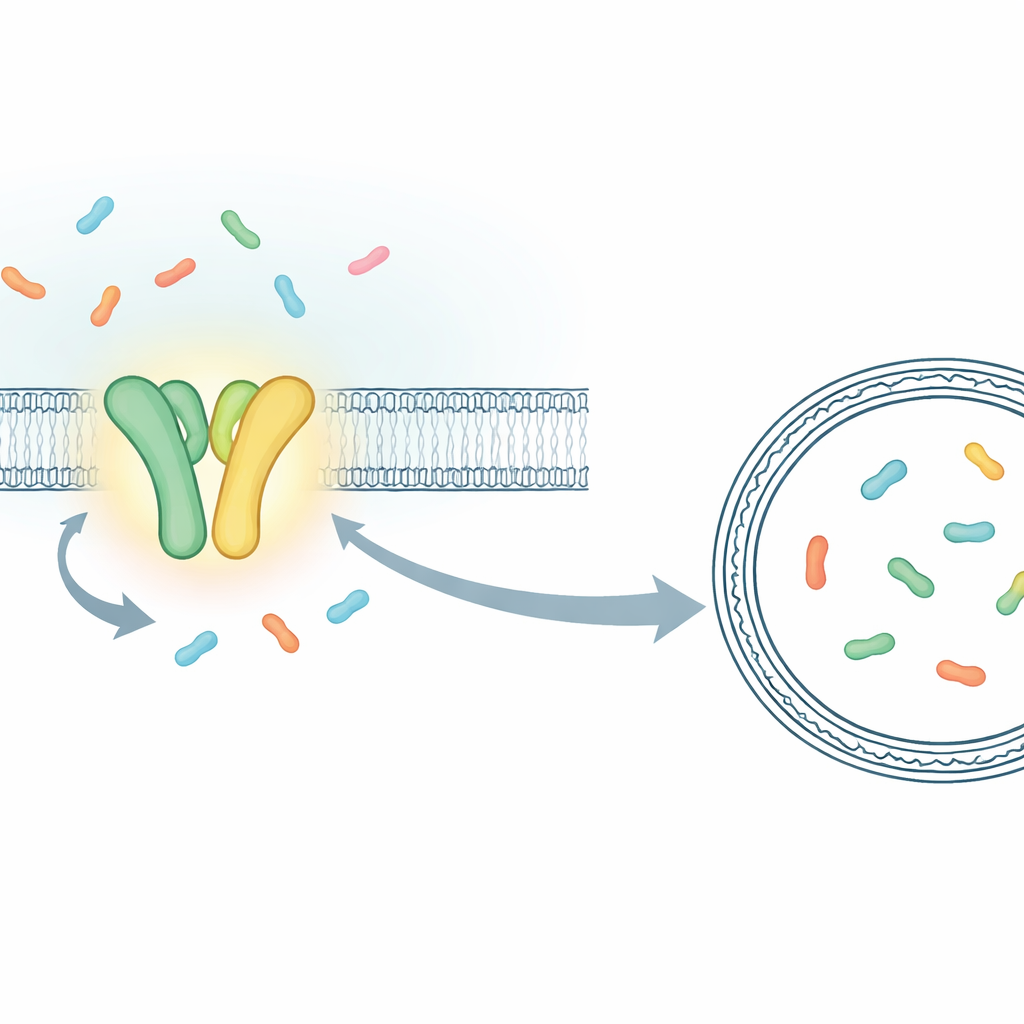
证明一次ATP结合移动一个肽
利用这个单分子测定法,研究者将正常TmrAB与一种改造的、反应较慢的变体进行比较,后者的循环被拉长便于分辨单个事件。慢速变体使得原本会相互遮盖的事件可以被区分开来。他们发现当ATP和肽同时存在时,囊泡内的传感器会以离散步骤从“空”态转为“装载”态,每一步均与单个肽的转运相符。通过分析传感器围合肽的速率并估算每个囊泡内的微小体积,他们甚至能将这些光学变化换算为近似的肽浓度。所得数值与在约100纳米直径的囊泡中先后积累一、二个肽的预期相符,从而证实他们确实是在逐一计数转运事件。
仅ATP结合即可触发分子开关
关键争议集中在镁离子(Mg2+)上:在细胞中镁通常伴随ATP存在,并且已知对ATP高效水解是必要的。有些模型提出镁可能也参与ATP结合或帮助转运蛋白闭合。为了解析这些作用,研究者用螯合剂去除了Mg2+,但仍提供ATP。在这些条件下,正常型和慢速转运蛋白都能完成且仅完成每个分子一次肽的转运,随后停止。这种行为表明即便没有Mg2+,ATP仍然可以结合并将转运蛋白从朝内构象切换到朝外构象,从而移动肽。然而没有Mg2+时转运蛋白无法高效水解ATP,因此不能复位进行下一轮工作。
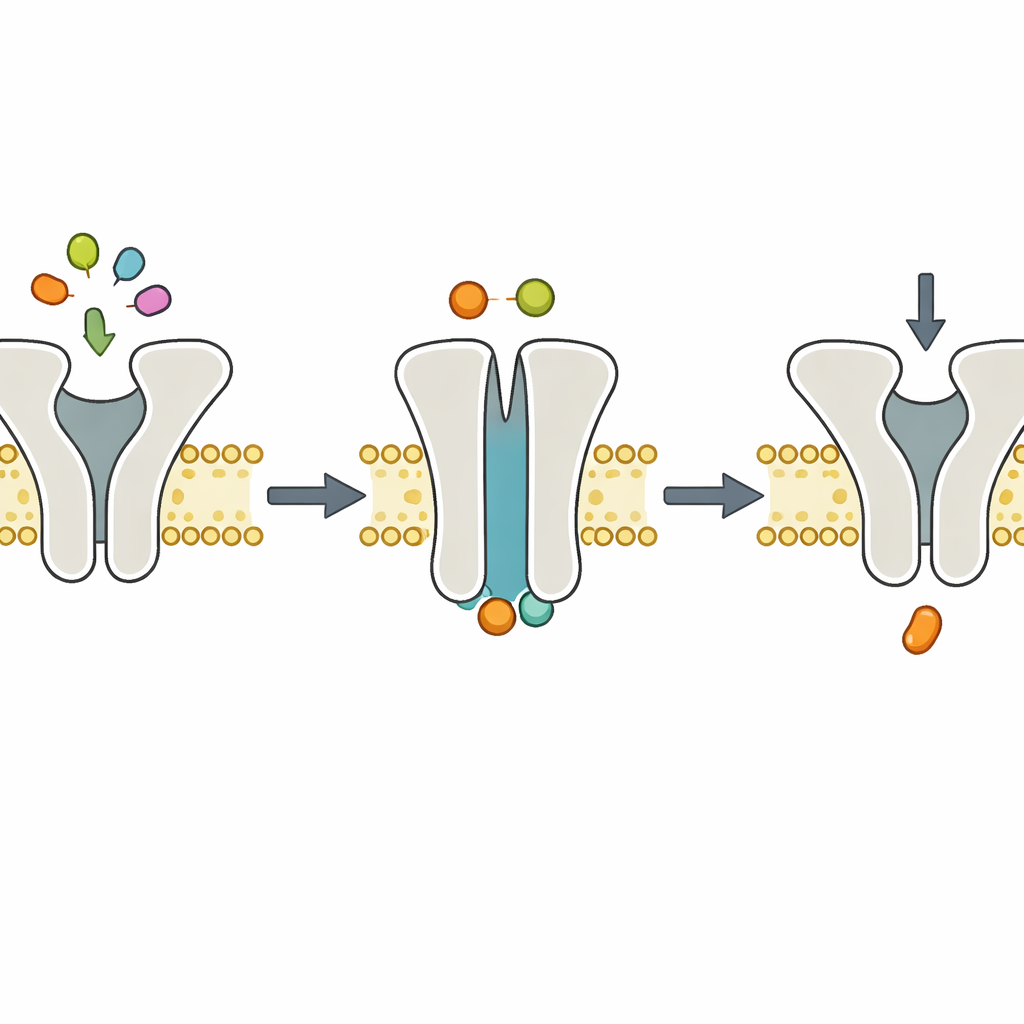
结构快照支持动力学观察
为观察在无Mg2+条件下机器的构象,团队采用了冷冻电子显微镜,对闪冻的分子进行近原子解析。他们在脂质纳米片中重建TmrAB,加入不含Mg2+的ATP并冷冻复合物。得到的结构显示TmrAB处于朝外、被“封闭”住的构象,ATP嵌入其两个内部结合口袋,但看不到任何Mg2+。这些构象几乎与早前含有ATP和Mg2+时获得的结构无异。再结合生化测定显示无Mg2+时ATP水解完全停滞,图像与动力学数据共同支持这样一个分工明确的机制:ATP结合驱动构象变化移动肽,而Mg2+依赖的ATP水解则负责复位步骤。
更清晰的细胞泵工作图景
通过观察单个转运蛋白并解析其结构,这项工作解决了关于ABC转运蛋白的长期疑问:推动肽移动的机械“冲程”由ATP结合本身触发,而非随后对ATP的化学分解。Mg2+的作用主要在于允许ATP被切开,从而使转运蛋白得以复位并继续工作。除了解释一项细胞生物学的基本原理,这种单分子方法也为剖析其他决定免疫、药物抗性以及多种疾病的膜机器提供了蓝图——逐个分子、逐次转运地加以研究。
引用: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
关键词: ABC转运蛋白, ATP结合, 单分子FRET, 膜转运, TAP与TmrAB