Clear Sky Science · zh
以多靶向PANoptosome介导的PANoptosis为目标的普鲁士蓝纳米颗粒用于心肌缺血-再灌注损伤治疗
为何保护正在愈合的心脏至关重要
当一个人发生心肌梗死时,医生会迅速疏通被堵塞的动脉以恢复血流。这一挽救生命的步骤却有一个隐性代价:氧气的突然回流本身会损伤心脏,导致细胞死亡并为心力衰竭奠定基础。本研究探讨了一种创新的纳米药物,旨在在这一脆弱窗期内通过同时阻断多条相互关联的细胞死亡途径来保护心脏,有望使心肌梗死后的恢复更为温和。
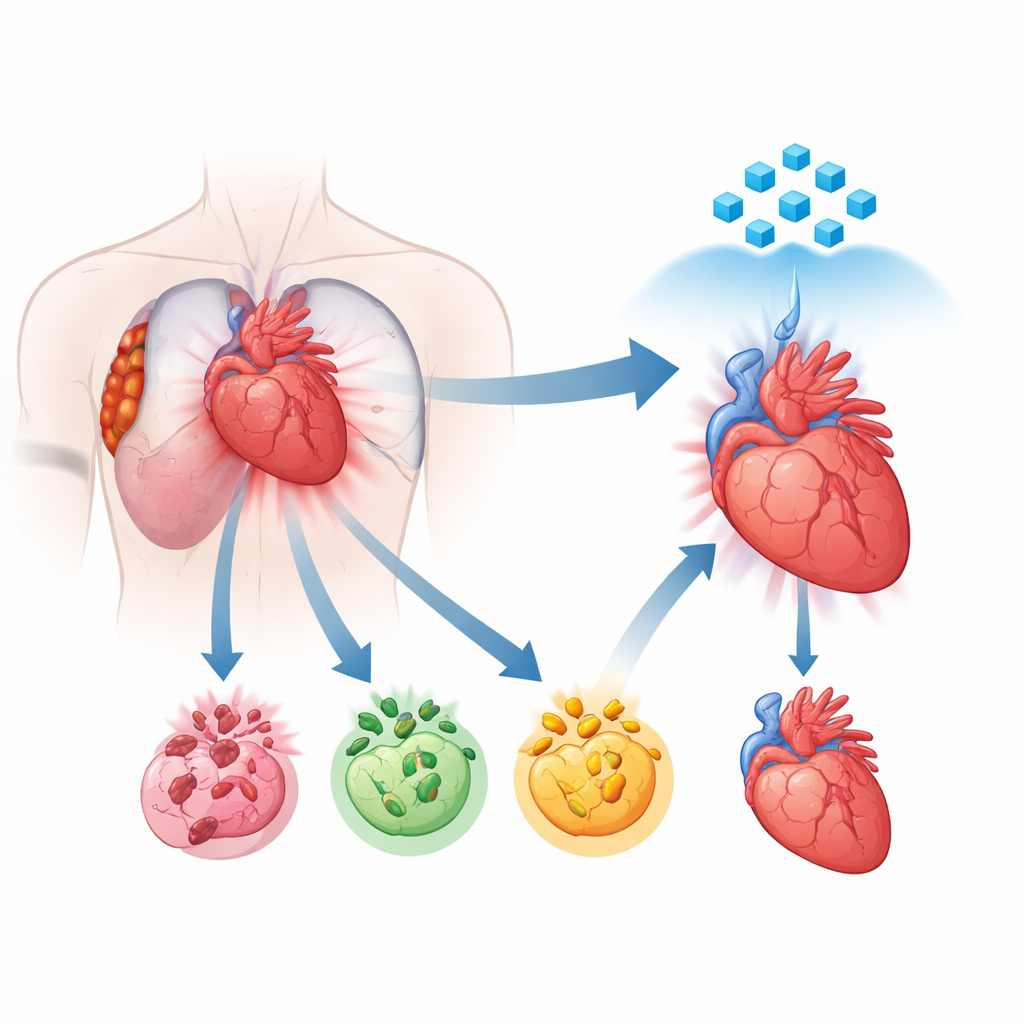
关于心肌细胞如何死亡的新视角
多年来,科学家已知受损的心肌细胞可通过不同的程序性路线死亡,包括凋亡、坏死性凋亡和焦亡学。每条路径有其独立的分子程序,但越来越多的证据表明这些路径并非独立运行。相反,它们相互对话并可融合为一种联合且失控的过程,称为PANoptosis。在这种状态下,多种细胞死亡程序同时被激活,使得仅阻断单一路径的治疗往往效果有限。作者对来自近期心肌梗死患者的人体心脏组织进行了单细胞核RNA测序,以描绘这些死亡程序在何处及多大程度上被开启。他们发现,在损伤最严重的区域,心肌细胞明显转向这种联合死亡模式,表明PANoptosis是损伤的核心驱动因素。
为受损心脏设计的小型多功能工具
为应对如此复杂的过程,研究团队转向了普鲁士蓝——一种已长期获批的医用化合物,最为人所知的是用于某些金属中毒的解毒剂。在纳米尺度下,普鲁士蓝颗粒表现得像微小的催化机器人,能够清除有害分子并影响细胞行为。通过计算机模拟,研究人员表明这些纳米颗粒可以直接附着于三个关键蛋白枢纽——RIPK1、ZBP1 和 AIM2——这些枢纽有助于组装PANoptosis的分子机械。通过以不同方式与这些枢纽结合,颗粒被预测能干扰协调三条细胞死亡通路的促死复合体的构建。
将纳米颗粒直接引导至受损心脏组织
纳米颗粒只有到达正确位置才有效,因此团队用来源于血小板的天然膜包裹普鲁士蓝颗粒,血小板具有趋向受损血管的能力。这层包膜形成了PB@PM,一种仿生载体,能像血小板一样循环并传递治疗负载。在接受可控性心肌梗死及动脉再通的小鼠模型中,成像显示PB@PM在受损心脏区域的富集远高于未包膜颗粒,同时在健康器官中基本避免积累。重要的是,这种包膜颗粒耐受性良好:血液检测和组织检查未显示明显毒性,支持其进一步开发的潜力。
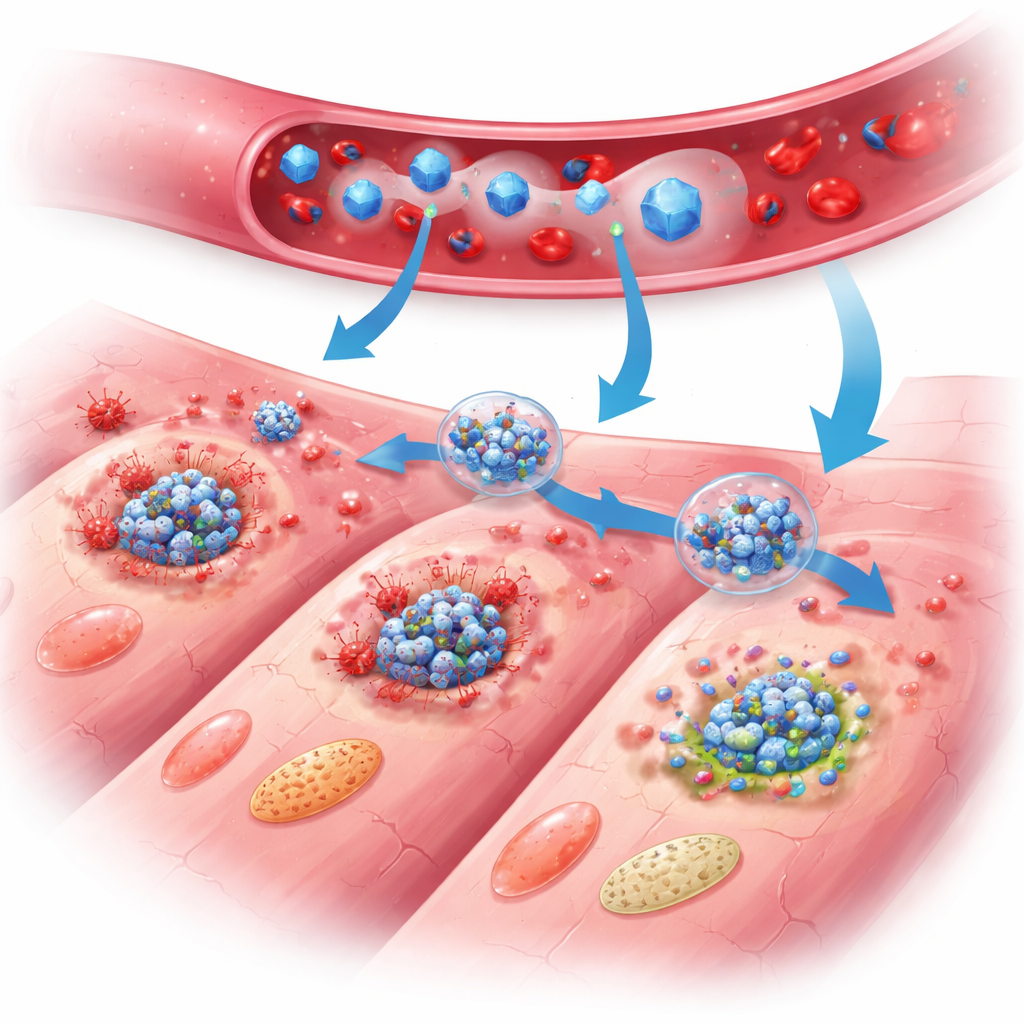
纳米防护如何保护心脏
在经治疗的小鼠中,PB@PM的益处在数日到数周内变得显著。心脏泵血功能改善,瘢痕面积缩小,与未治疗动物相比心壁变薄程度较轻。详细组织学研究显示,死亡的心肌细胞更少,炎症细胞更为平静,修复组织结构更好,血管生成更健康,并且存活细胞的异常肥大减少。在分子水平上,广泛的基因表达谱和蛋白测量表明PB@PM同时抑制了三条主要的程序性死亡通路,破坏了多蛋白PANoptosis复合体的组装,并降低了助长炎症的信号分子水平。颗粒还清除有害的活性氧,稳定线粒体——细胞的能量工厂——并恢复更正常的能量代谢,去除了会将细胞推向自我毁灭的关键触发因素。
这对未来心肌梗死护理意味着什么
简而言之,这项工作表明,经过巧妙设计的纳米颗粒可以像多面盾牌一样保护心脏,抑制错综复杂的致死信号网络,而非逐一追逐单一路径。通过靶向受损心肌组织、结合核心控制蛋白并缓解氧化与炎性应激,PB@PM显著减少了在动脉再通后常见的细胞丧失和瘢痕形成的连锁反应。尽管在将此策略推向临床之前仍需大量测试,该研究提供了一个概念验证:整体靶向PANoptosis——并以智能且受生物启发的颗粒实现——可能为心肌梗死后保护心脏开启新篇章。
引用: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
关键词: 心肌缺血 再灌注, 纳米颗粒治疗, 程序性细胞死亡, 心脏炎症, 线粒体保护