Clear Sky Science · zh
磷硫代修饰反义寡核苷酸对DNA损伤反应的失调
当有益的基因疗法误导细胞的修复队伍
反义寡核苷酸(ASO)是一类新兴的精准药物,旨在开关或调节单个基因的表达。它们已用于治疗某些罕见遗传疾病,并正在用于更多疾病的临床研究。本研究揭示了用于提高这些药物稳定性的常见化学修饰意想不到的一面:在特定条件下,它会误导细胞,使其误以为DNA受损,从而阻塞修复机械并对基因组造成长期风险。
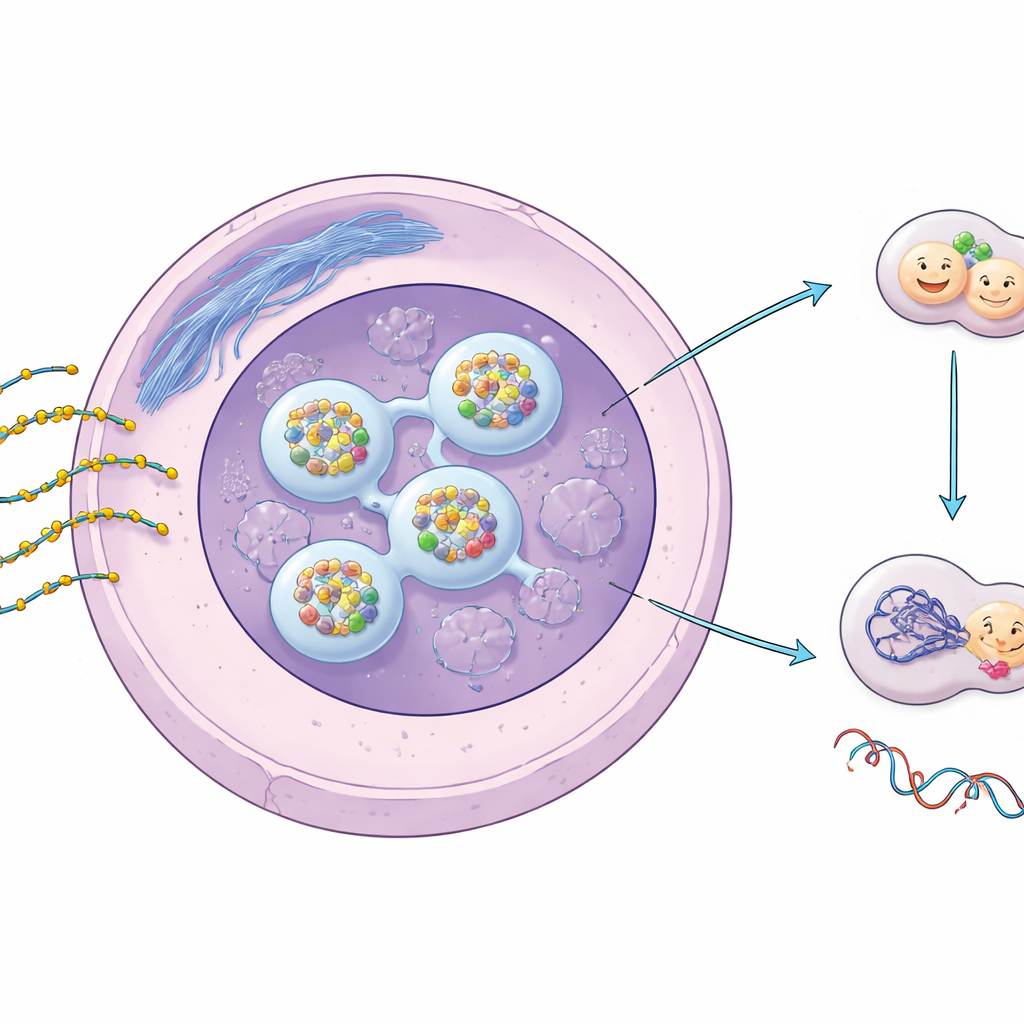
设计师基因开关及其化学升级
ASO是短而单链的遗传物质,设计用来识别并结合细胞内的特定RNA信息,从而沉默或改变这些信息。为了在体内存活并高效进入细胞,大多数治疗性ASO都带有磷硫代(PS)修饰,即在链的骨架中用硫原子替代一个氧原子。这个微小变化显著提高了它们的稳定性和与蛋白质相互作用的倾向。先前工作表明,PS‑ASO会在细胞核内聚集成特定斑点并可能对某些核结构造成压力,但这对DNA修复和长期安全性的意义尚不清楚。
模拟真实DNA修复位点的人工液滴
作者追踪了带荧光标记的PS‑ASO在人体细胞中的行为,发现在常用的实验剂量下,它们会迅速在细胞核内积累并孕育出新的球形结构,称为PS体。这些体以浓度依赖的方式形成,表现出像液滴一样的行为——会融合、溶解,并依赖弱的分子作用力,都是液-液相分离的典型特征。关键的是,这些结构并不位于实际DNA断裂发生的位置,也不含有断裂DNA的常见标记。相反,研究显示关键的DNA修复酶,包括DNA‑PKcs、ATM、ATR和PARP1,直接与PS‑ASO结合并在这些人工液滴中高度富集,即便基底DNA仍然完好无损。
激活细胞损伤信号的错误警报
一旦形成,ASO诱导的液滴并不只是被动捕获蛋白:它们会激活修复酶。在ASO进入后一小时内,这些液滴中的酶被激活并开始修饰邻近的染色质,在组蛋白上留下通常在真实DNA损伤后才见到的化学标记。这引发了完整的DNA损伤反应——招募更多修复因子、启动检查点信号,并降低称为CDK的细胞周期驱动器的活性。因此,细胞在关键的细胞周期阶段放慢或停止进程,尤其是在通常检查DNA完整性以准备分裂的点。在以临床相关ASO给药处理的小鼠脑组织中,研究者也观察到在ASO摄取较高的区域DNA损伤信号增强,表明这些效应并不限于细胞培养。
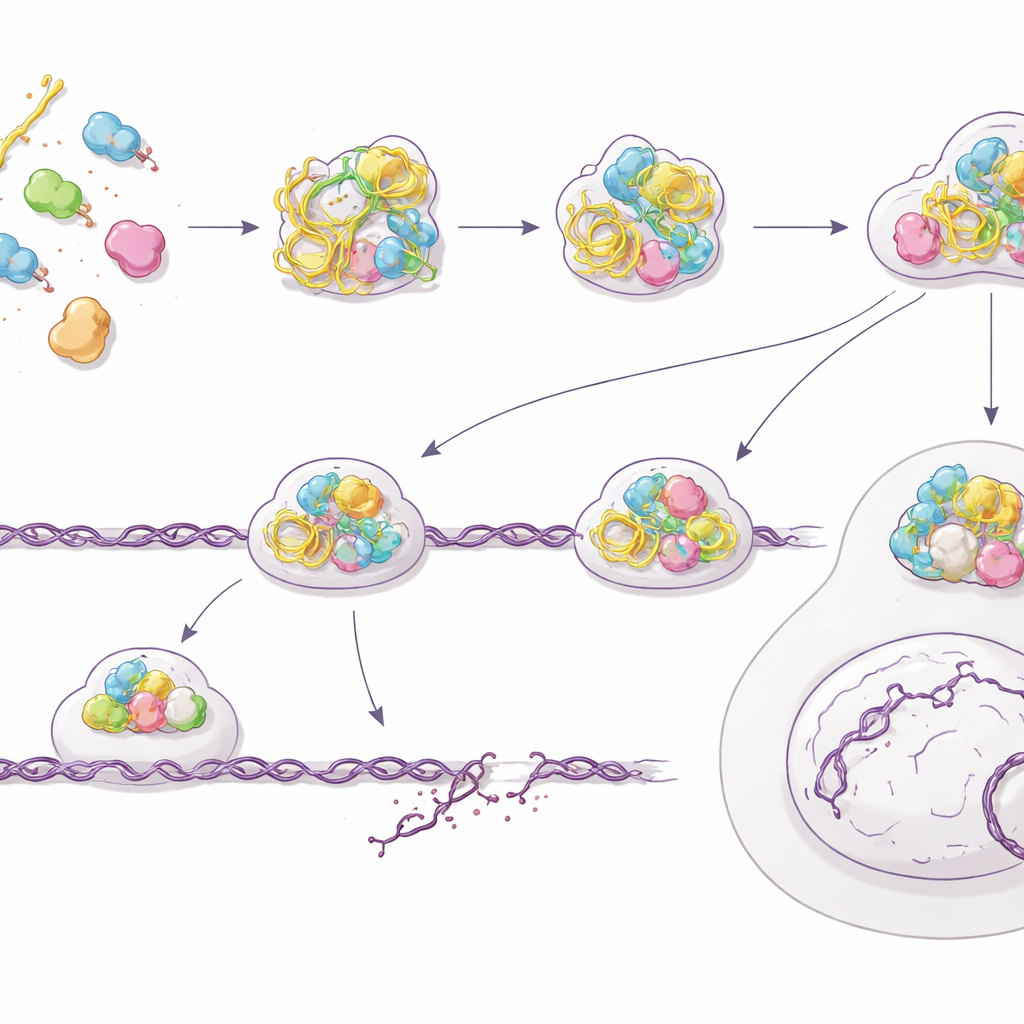
修复出错与日益增多的DNA断裂负担
矛盾的是,尽管细胞的报警系统响个不停,其实际修复危险DNA断裂的能力却变差。团队显示,经PS‑ASO预处理的细胞在照射后难以清除损伤,甚至积累更多自发断裂——通过彗星实验和持续存在的修复焦点可以测得这一点。细看细胞最精确的修复途径之一——同源重组,揭示了问题所在:像BRCA2和RAD51这样的关键因子无法在断裂的DNA末端正确组装,而对这些末端的早期处理标记仍可见。利用遗传报告系统,作者量化出在PS‑ASO暴露后同源重组效率约下降60%。细胞总体存活能力下降,对辐射的敏感性明显增加,这与一个被错误激活但未正确部署的修复系统一致。
对未来基因靶向药物的意义
综上所述,研究表明PS修饰的ASO可以在细胞核内诱导人工液滴,这些液滴在没有真实损伤需要修复的情况下,浓缩并激活DNA修复酶。这种长期的错误警报扰乱了正常的修复选择,尤其是准确的同源重组,导致持久的DNA病灶、检查点激活和细胞死亡。虽然最强的效应在核内ASO水平较高、常见于转染实验的情况下最明显,但在较低、更接近药物剂量的情况下也可检测到损伤信号的微妙激活。对患者和药物开发者而言,结论明确:正是那些使ASO成为有效药物的化学特征,在某些情况下可能干扰细胞最基本的防护机制——维持基因组稳定性的能力——强调了设计更安全骨架和在治疗期间监测DNA修复通路的必要性。
引用: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
关键词: 反义寡核苷酸, DNA损伤反应, 液相分离, 同源重组, 基因组稳定性