Clear Sky Science · zh
手性肽聚糖模拟物靶向细菌细胞壁生物合成以干预病原体
一种追踪有害微生物的新方法
抗生素耐药性感染在全球范围内上升,但医生仍然缺乏能精确识别并攻击危险细菌而不伤害自身细胞的工具。这项研究提出了一种巧妙的分子“诱饵”,模仿细菌细胞壁的关键构件。这些设计分子既能用于成像显现感染,也能将抗生素直接运送到微生物体内,为应对难治病原体提供了新的策略。
模仿细菌的铠甲
细菌被一种由糖类和不寻常的镜像氨基酸构成的坚韧网格包裹,这些氨基酸在我们自身细胞中很少使用。研究者利用这一差异,合成了以糖为主链并装饰有特定镜像形式丙氨酸的长链。这些链被称为手性肽聚糖模拟物,旨在尽量接近细菌用于构建细胞壁的天然成分,但在哺乳动物组织中并不存在。通过微调所接入的D-型丙氨酸含量,团队制备出更偏向识别细菌而非人类细胞的版本。
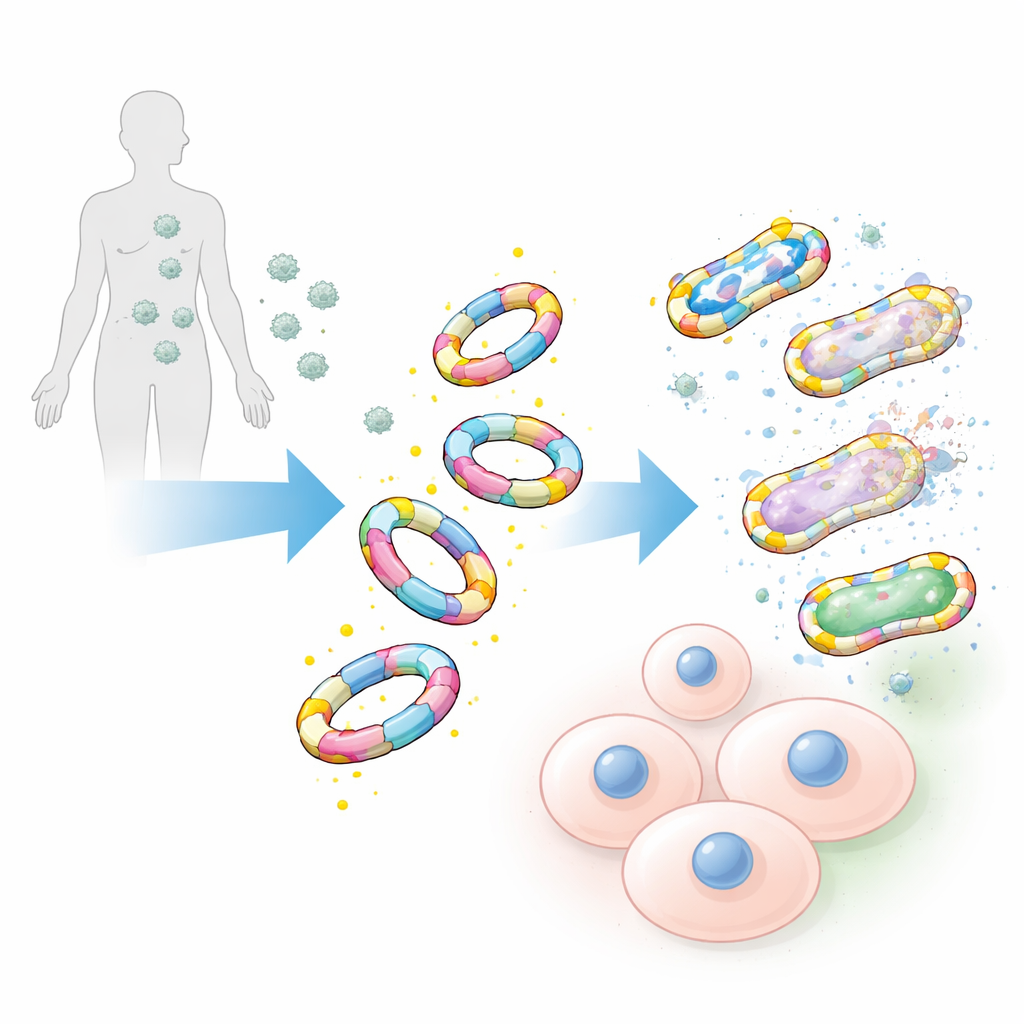
锁定细菌,而非我们的细胞
在包括耐甲氧西林金黄色葡萄球菌等医院内常见菌株及其他ESKAPE病原体在内的广谱病原体测试中,装饰有D-丙氨酸的模拟物以惊人的效率结合到细菌表面。由L-型丙氨酸构成的镜像对照体以及仅有原始糖链的样品则表现出较弱或可忽略的结合力。团队还将这些大分子模拟物与基于单个D-丙氨酸的小分子化学探针进行了比较。即便小探针被制成极其明亮,它们标记到的细菌仍远少于大型、更加逼真设计的模拟物,信号也更弱,凸显了大型仿生设计的优势。
劫持细胞壁装配线
为理解识别为何如此强烈,科学家检查了这些模拟物与细菌细胞壁合成机器的相互作用。他们发现,D-丙氨酸为基础的链不仅仅是附着在外表;它们被当作真正的构建模块摄取,并进入通常连接细胞壁组分的相同酶促步骤。化学分析检测到仅在存在这些模拟物时才出现的新中间体分子,计算机模拟显示关键的壁构建酶对这些模拟物的结合力甚至超过天然底物。在几轮细菌生长过程中,模拟物在细胞壁中积累,逐渐扭曲其结构并使其变得渗漏。
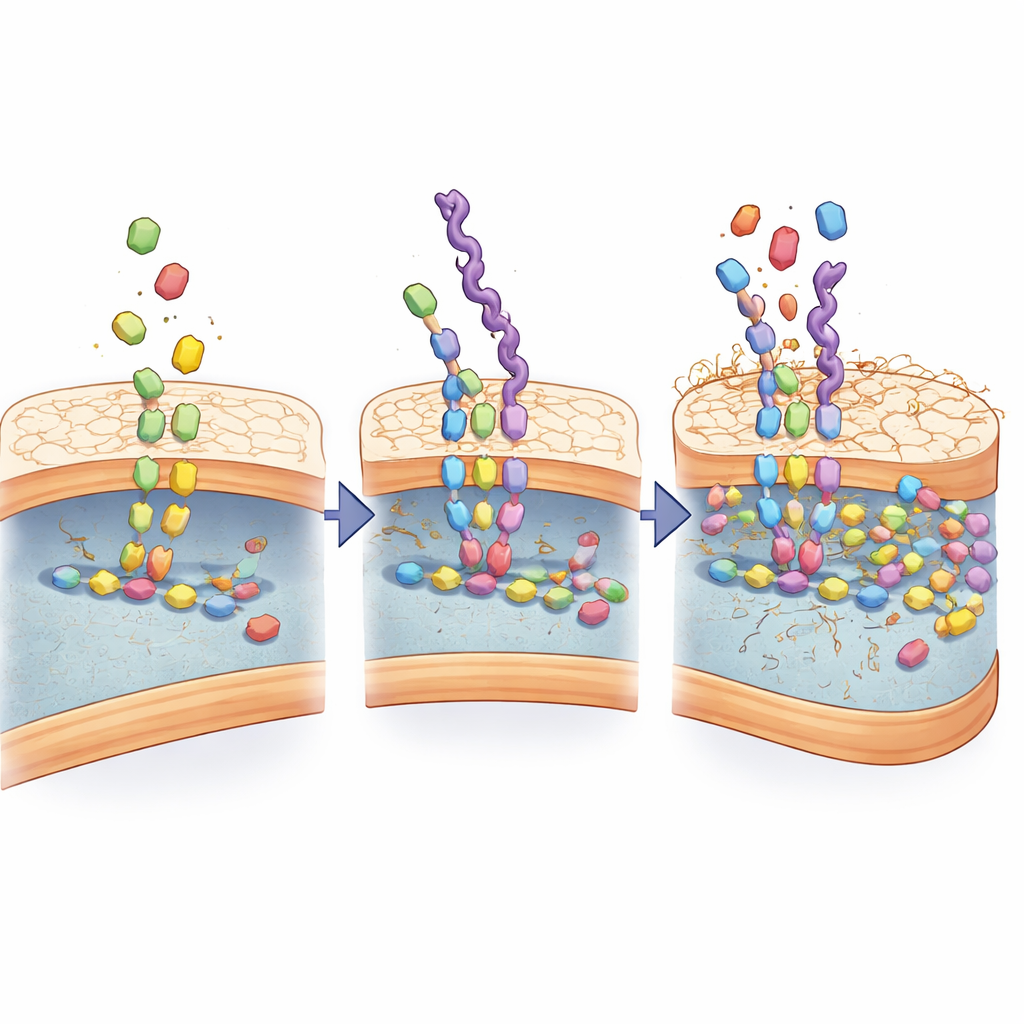
将模拟物转化为智能药物载体
由于这些链在水中天然聚集成微小颗粒并携带许多化学活性位点,团队将其用作成像染料和抗生素的支架。荧光化版本在细胞培养中清晰描绘出细菌轮廓,同时几乎不与并培养的哺乳动物细胞相互作用。研究者随后将四环素装载到基于模拟物的颗粒中。在体外试验中,这种包装使四环素的效力提高了数倍,甚至在远低于游离药物的剂量下也能杀灭耐药菌株。显微镜观察显示,载药的模拟物在细菌表面聚集、穿透其包膜,并比非靶向制剂引发更广泛的细胞死亡。
在体内对抗感染
最严苛的测试在小鼠局部皮肤伤口和危及生命的腹腔感染模型中进行。在感染伤口中,荧光模拟物能够深入组织定位细菌,并在携带四环素时几乎完全清除微生物。这带来了更快的愈合、更厚的新生皮肤、更有序的胶原沉积和更多毛细血管生长。在系统性感染模型中,模拟物特异性地在脾脏和肺等感染器官中积累,且在载药时显著降低细菌数量。重要的是,高剂量的模拟物单独使用显示出良好的安全性,未见主要器官或血液化学指标的明显损害。
这对未来治疗的潜在意义
通过构建与细菌细胞壁自身成分高度相似的化学仿制品,这项工作展示了一种“混入”病原体代谢体系的新方法,而不仅仅是从外部发起攻击。这些手性模拟物既可作为用于成像的高精度信标,也可作为将抗生素引导至微生物目标(包括耐药菌株)的智能载体,同时尽量避免伤及哺乳动物细胞。如果能转化为临床工具,这类仿生平台可帮助医生精确定位感染位置,并以更低的药物剂量更有效地治疗感染,为应对日益严峻的抗微生物耐药性挑战提供有前景的武器。
引用: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
关键词: 抗生素耐药性, 细菌细胞壁, 靶向药物递送, 分子成像, 纳米医学