Clear Sky Science · zh
对运动皮层中细胞类型特异性TDP-43病理的多模态剖析
这项研究对人们的重要性
肌萎缩侧索硬化(ALS)和额颞叶痴呆(FTD)是毁灭性的脑疾病,会剥夺人的运动、语言和个性。大多数ALS患者以及许多FTD患者在显微镜下有一个共同的特征:称为TDP-43的蛋白异常聚集并出现在不该出现的地方。本研究提出两个与未来治疗有重大意义的实用问题:究竟哪些脑细胞最受TDP-43影响,以及这些细胞在DNA调控和基因活性层面上具体发生了什么故障?
追踪损伤到大脑的运动中心
研究者将注意力集中在初级运动皮层——控制随意运动的那条脑组织带上。利用来自ALS、ALS-FTD患者和神经学正常对照者的尸体捐献脑样本,他们分离出单个细胞核,并同时读取基因表达状态与局部DNA开放程度。这种“多组学”方法在超过18万枚细胞核上实施,使他们能够将细胞精确分型:若干类兴奋性和抑制性神经元,以及星形胶质细胞、少突胶质细胞和小胶质细胞等支持细胞。随后他们将这些结果与另一份人体脑数据集的空间基因图谱整合,以将这些细胞类型重新置回大脑皮层熟悉的分层结构中。
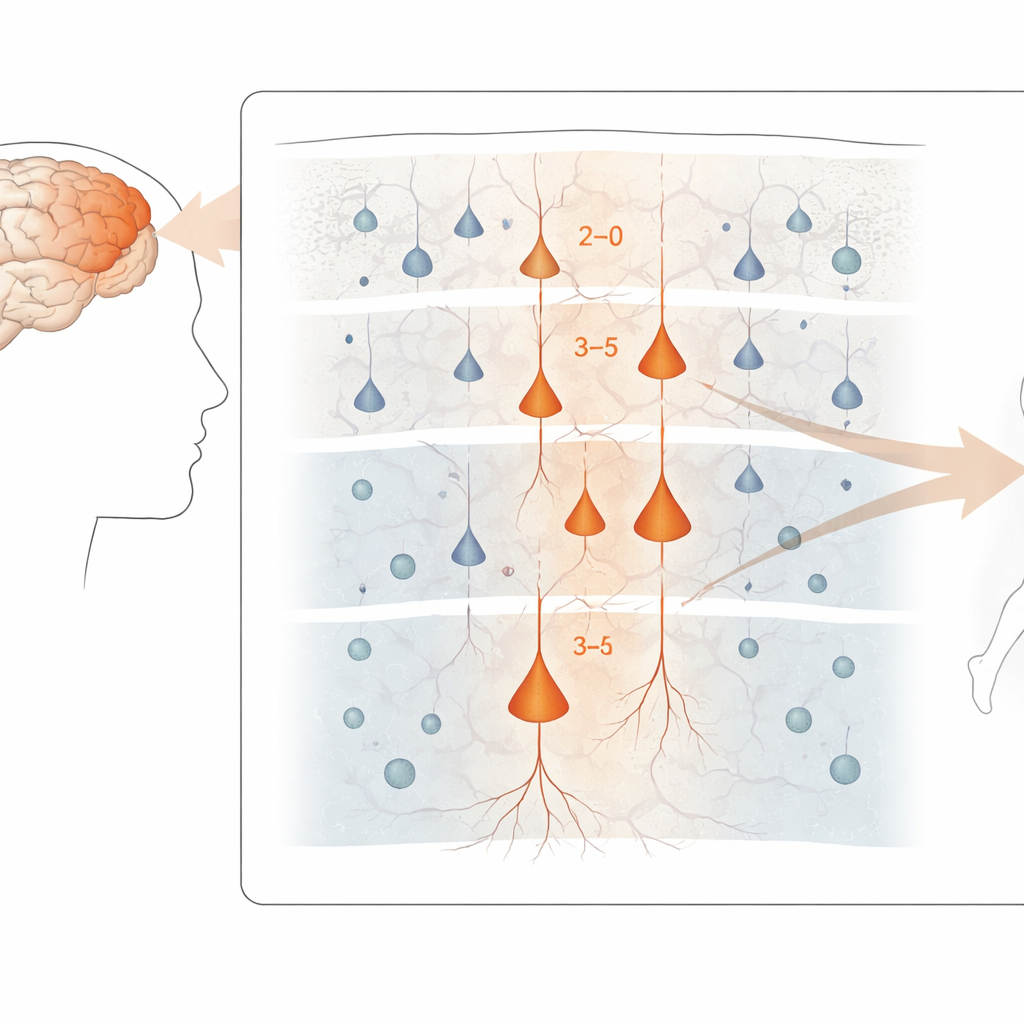
精准定位最脆弱的神经元
在整个运动皮层中,病相关的基因变化最为显著地出现在兴奋性神经元——这些细胞推动脑回路的活动。特别是皮层上层和中间层的连接皮层内的神经元,以及将信号发出皮层外的某些深层细胞——包括控制脊髓运动神经元的大型“贝茨”细胞——显示出最明显的变化。相比之下,抑制性中间神经元和许多胶质细胞在基因表达层面受影响较小,虽然其中一些确实表现出更为微妙的变化。尽管存在这种分子层面的动荡,组织中主要细胞类型的总体比例在患者与对照之间出人意料地相似,这提示损伤更多与细胞功能改变有关,而不仅仅是细胞数量的丧失。
TDP-43如何从内部重塑基因活动
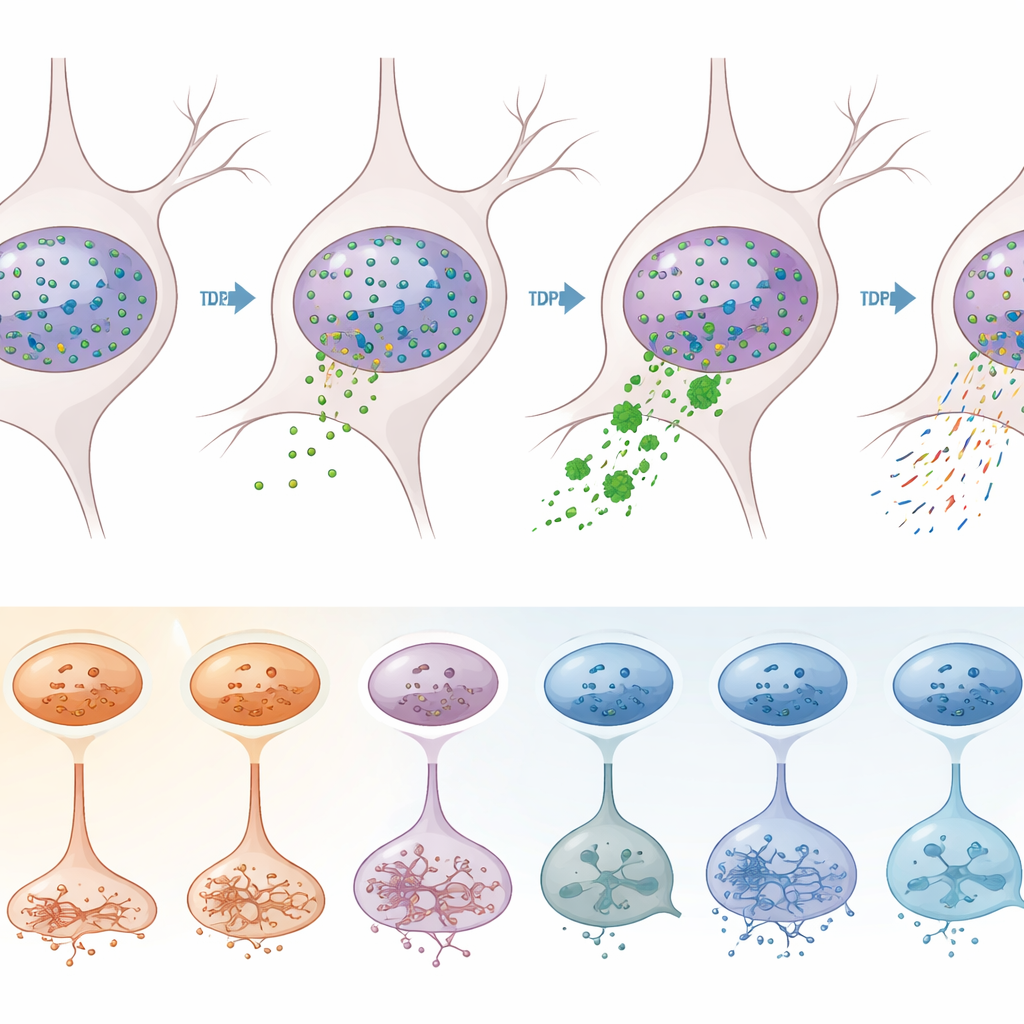
为将由TDP-43直接驱动的效应与其他疾病过程区分开,团队采用了一种巧妙的分选策略。他们用针对TDP-43和神经元标志的抗体标记细胞核,然后利用流式细胞术将那些核内丢失TDP-43(病理标志)与保留TDP-43的神经元分离开来。对超过1.2万枚此类细胞核的测序显示,TDP-43的丢失在兴奋性神经元中占主导地位,尤其是皮层2–3层、3–5层、5层和6层的特定亚型。在这些脆弱的神经元中,数百个基因表达失调,其中包括许多已与ALS相关的基因。TDP-43功能失常的经典分子特征——如STMN2和KALRN基因转录本中出现的“隐匿”额外片段,以及RNA分子在末端剪接和加尾位点的改变——在缺失TDP-43的细胞核中明显富集。
表观遗传重塑:并非所有变化都源于TDP-43
由于他们在同一细胞核中同时测量了基因活性和染色质开放性,作者可以探究哪些变化与DNA包装的转变相关。他们发现基因组中存在数以万计的位点,其局部染色质可及性与基因表达变化呈一致性。许多在ALS和ALS-FTD中改变的基因位于此类区域,表明疾病特征部分反映了更广泛的表观遗传重塑,而非TDP-43丧失的直接后果。有趣的是,这些与染色质相关的变化常常会汇聚到参与细胞通信和轴突引导的信号通路上,且在某些兴奋性神经元和少突胶质细胞中尤为显著。当团队将与TDP-43病理相关的基因变化与与染色质转变相关的变化进行比较时,发现二者部分重叠但在很大程度上是不同的两层破坏。
这对未来疗法的意义
对于普通读者,关键信息是ALS和ALS-FTD并不会均匀地损害运动皮层。相反,它们攻击特定的兴奋性神经元类型以及在较小程度上某些支持细胞,以依赖于TDP-43异常行为和更广泛的DNA包装与读取改变的方式改变它们的基因程序。这些发现表明,有效的治疗可能需要既具细胞类型特异性又具通路特异性——例如在最脆弱的神经元中恢复TDP-43功能或纠正其剪接错误,同时另行针对跨多种细胞类型共同存在的表观遗传和信号学改变。通过以高分辨率绘制这一复杂景观,该研究为设计更精确的干预方案提供了蓝图,旨在减缓或预防ALS和ALS-FTD中运动控制的丧失。
引用: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
关键词: ALS, 额颞叶痴呆, TDP-43, 运动皮层神经元, 单核多组学