Clear Sky Science · zh
依赖情境的翻译抑制作为癌症治疗方式
将细胞的蛋白质工厂变成对抗癌症的武器
癌细胞通过不断合成大量短寿命的“驱动”蛋白维持增殖和分裂。本研究探索了一种新途径:在核糖体制造特定蛋白序列时进行微妙阻断——尤其是那些存在于像 MYC 这样的难以药物化的致癌基因中的序列。这样的选择性干预有望杀死肿瘤细胞,同时尽量保留正常蛋白质的合成。
细胞如何合成蛋白——以及可能出错的地方
每个细胞都依赖核糖体,这种微小的分子工厂读取遗传信息(mRNA)并将氨基酸连接成蛋白质。现有多数靶向核糖体的药物(如抗生素或较早期的抗癌药)更像是粗暴的工具:它们广泛地关闭蛋白质合成,会损伤健康细胞并引起严重副作用。作者的推理是:由于每条新生肽链都有独特的序列和化学特性,或可设计出仅在特定序列进入核糖体时阻断翻译的小分子,而对细胞其余的蛋白质合成影响甚微。
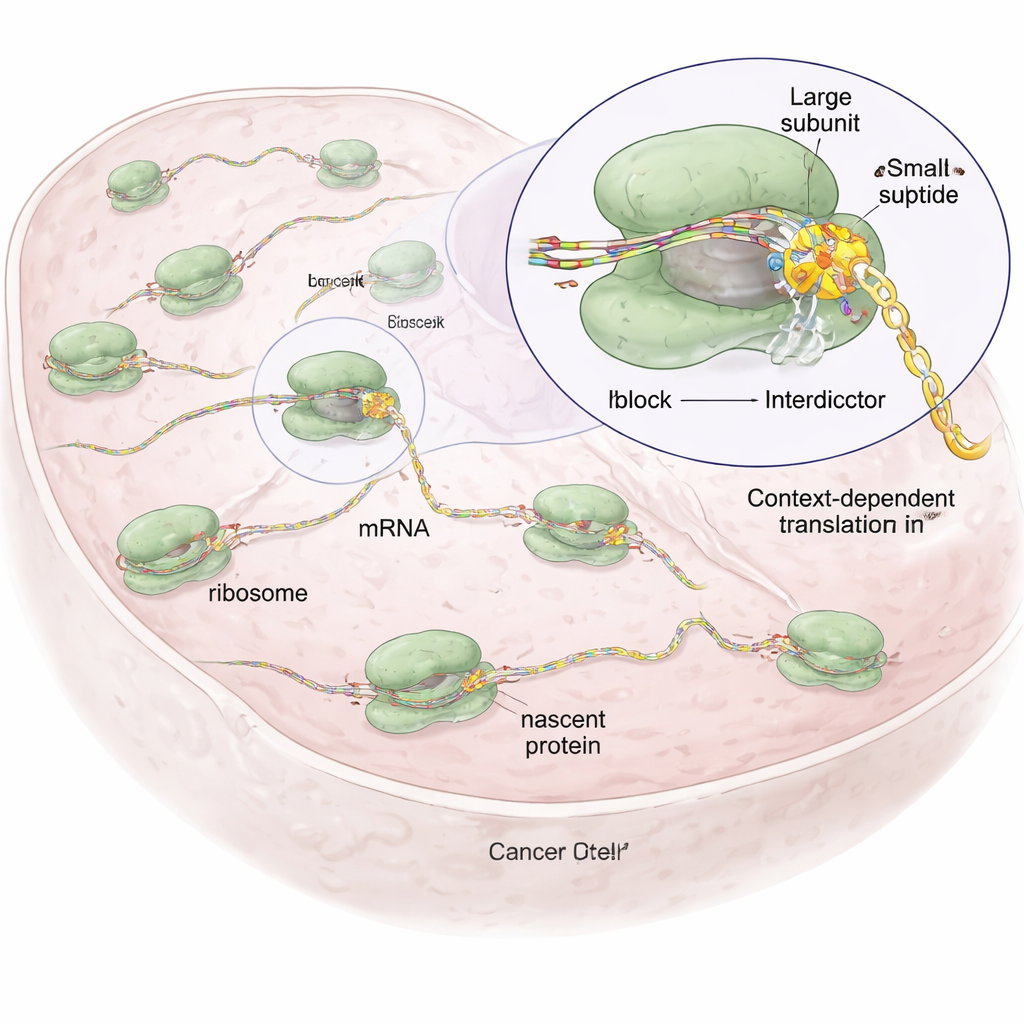
专门使某些蛋白序列停滞的设计分子
研究人员以天然化合物阿尼索霉素为起点——它能结合核糖体催化中心,即肽键形成处——构建了一类称为“拦截剂(interdictors)”的合成分子家族。所有分子共享一个将其锚定在核糖体内的核心骨架,但在朝向新生肽链的侧基上有所不同。这些侧基被调整以偏好特定类型的氨基酸——例如,一种拦截剂(IDB‑001)倾向结合带负电的残基,而另一种(IDB‑002)偏好小的疏水残基。通过核糖体足迹测序等技术(能在细胞内全局绘制核糖体在 mRNA 上的停滞位点),团队展示了每种化合物在新生肽链的特定短序列处引发停滞,常发生在倒数第二位(−1)氨基酸处,说明其作用依赖于序列而非不加区分的关闭。
原子级观察药物与核糖体的相互作用
为揭示这种选择性的物理基础,作者在翻译设计肽序列的过程中冷冻人源核糖体,并通过低温电子显微镜得到了近原子分辨率的图像。他们观察到拦截剂嵌入核糖体活性位点,与新生肽链的最后几种氨基酸形成精确接触。在一个结构中,IDB‑002 的疏水侧基被肽链中小而不笨重的残基包裹,这解释了为何较大的侧链不被接受。在另一个结构中,来源于 MYC 的酸性侧链摆动形成了与 IDB‑001 上正电基团的盐桥。药物的存在还促使邻近的核糖体 RNA 碱基移动到新的位置,收窄了活性位点并部分阻挡下一个 tRNA 的进入,有助于在这些有利序列处冻结延伸过程。
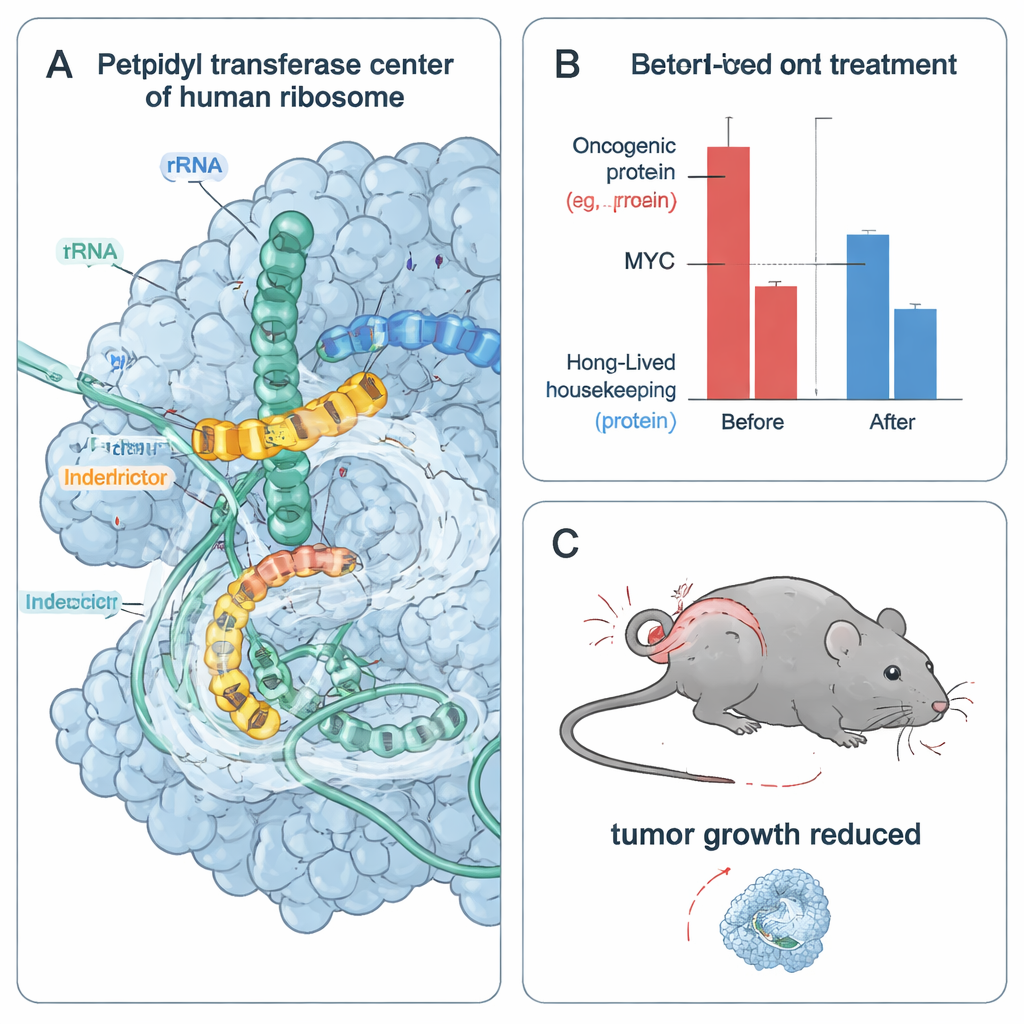
从停滞的核糖体到受压并死亡的肿瘤细胞
因快速分裂的癌细胞严重依赖短寿命的致癌蛋白(如 MYC 和 CCND1),团队测试了拦截剂对肿瘤细胞存活的影响。在多种依赖 MYC 的癌细胞系中,IDB‑001 和 IDB‑002 在纳摩尔到低微摩尔浓度范围内降低细胞活力。进一步优化的类似物 IDB‑003 效力更强且适合口服给药。在细胞内,这些化合物能迅速耗竭 MYC 及其他快速周转的致癌蛋白,而在相同时间窗口内对寿命更长的家务蛋白影响较小。药物还触发了与核糖体碰撞相关的细胞应激反应,但阻断这些应激信号通路并未消除活力丧失,这表明直接剥夺关键致癌蛋白是肿瘤细胞死亡的主要驱动因素。
在难治性乳腺癌模型中的概念验证
为测试该方法在动物体内的有效性,作者对携带人源三阴性乳腺癌肿瘤的小鼠进行口服给药 IDB‑003。在 28 天内,受治疗的肿瘤生长显著放慢,与对照组相比高剂量时肿瘤生长抑制可达 80%,本研究中未报告严重毒性。肿瘤的基因表达分析显示 MYC 靶基因程序显著下调,与体内 MYC 活性降低相符。综合来看,这些结果表明有选择性地在特定蛋白序列上使核糖体停滞,可削弱依赖不稳定致癌驱动因子的肿瘤,同时可能避免传统翻译抑制剂的广泛毒性。
这对未来癌症治疗意味着什么
该研究引入了一类新型小分子药物:它们不是通过结合成熟蛋白起效,而是在蛋白被合成时拦截它,且仅在存在短小的“地址标签”序列时发生作用。由于许多致癌蛋白结构松散、寿命短或缺乏传统药物可靶向的口袋,直接在核糖体水平靶向其合成,或为治疗由诸如 MYC 等目前“难以成药”基因驱动的肿瘤开辟新途径。研究还提示,通过调整拦截剂的化学性质,未来有望设计出针对不同序列基元和疾病靶点的药物,将这一策略扩展到肿瘤学之外的其他需要下调特定蛋白以恢复健康的情况。
引用: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
关键词: 靶向核糖体的癌症疗法, 翻译抑制, MYC 驱动的肿瘤, 依赖情境的小分子, 三阴性乳腺癌