Clear Sky Science · zh
将ephrin-A1–EphA2信号鉴定为潜在的骨折预防靶点
为何保护脆弱的骨骼至关重要
随着年龄增长,骨骼会变薄变脆,以至于像被地毯绊倒这样的日常小事故也可能导致严重骨折。骨质疏松性骨折不仅令人疼痛,还给医疗体系带来沉重开销,并可能夺走多年的健康寿命。现有药物有效,但通常仅用于确诊的骨质疏松患者,且可能伴随罕见但令人担忧的副作用。本研究提出了一个前瞻性问题:能否利用大规模人群中的遗传学和血浆蛋白测量,发现全新方式来强化骨骼并在骨折发生前加以预防?
在血液中寻找骨折线索
研究人员首先把体内循环蛋白视为一本巨大的线索书。许多药物正是通过作用于血中蛋白起效,因此找到真正影响骨折风险的蛋白可能直接指向新疗法。利用UK Biobank的样本,他们考察了会提高或降低1615种不同血浆蛋白水平的遗传变异,然后将这些遗传“蛋白指纹”与来自超过5万例前臂骨折的大型基因研究数据相连。一种名为孟德尔随机化的统计方法帮助他们提出问题:当人们天生携带使某种蛋白水平升高或降低的基因时,他们终生的骨折风险是否以一致的方式变化?
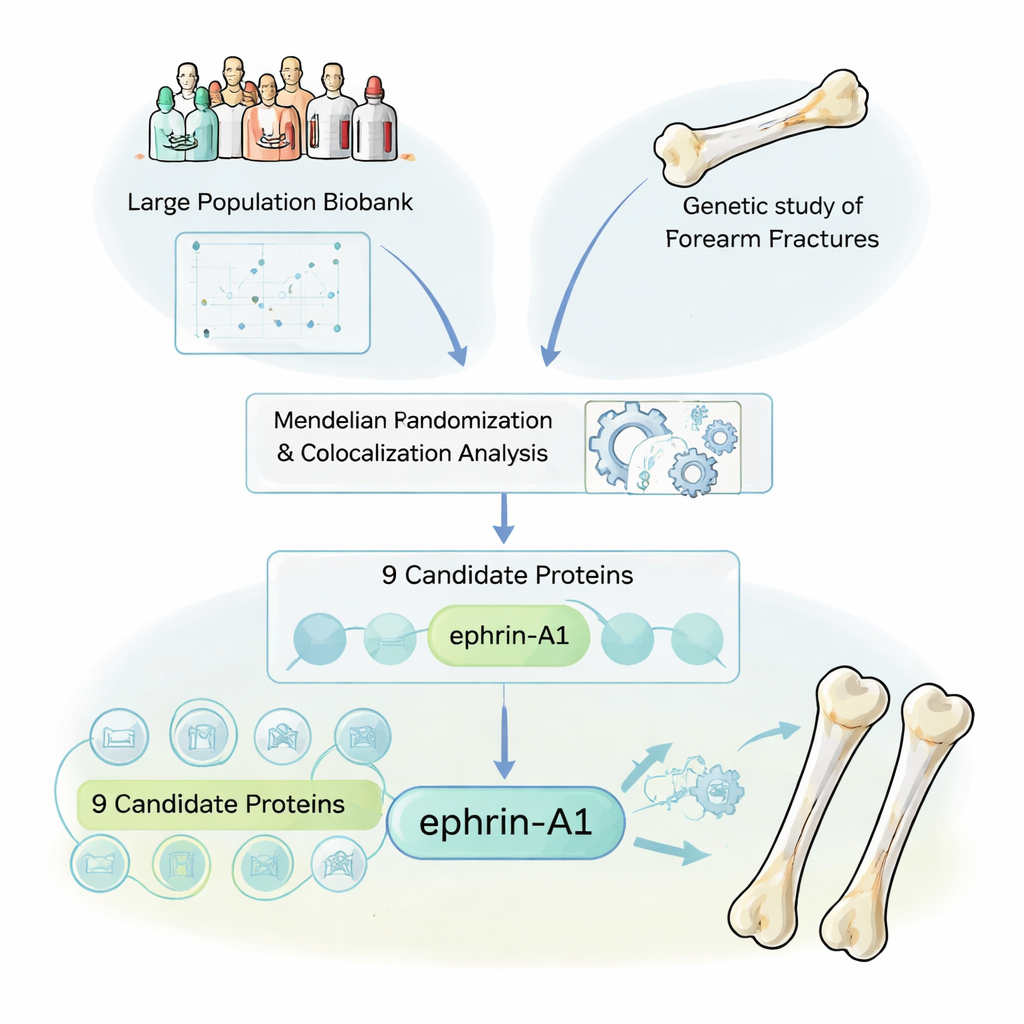
将真实信号与遗传噪声区分开来
由于邻近基因常常一起遗传,团队使用了第二层分析——共定位(colocalization),以确保所见是真正的因果关系,而非误导性的基因邻居效应。在1615种蛋白中,有九种被凸显为与前臂骨折因果相关。重要的是,其中几种已知参与骨骼代谢:硬化蛋白(sclerostin)和骨保护素(osteoprotegerin),它们是现有抗骨质疏松药物的靶点,以及若干长期与骨密度相关的蛋白。它们的再次被发现为方法管线提供了关键的质量检验——表明该流程既能可靠地重新发现已验证的药物靶点,也能带来新的候选目标。
一个令人意外的新保护因子:ephrin-A1
在新提出的蛋白中,有一种尤其引人注意:ephrin‑A1。遗传上倾向于具有更高血浆ephrin‑A1水平的人群,骨密度更大、前臂骨折更少。ephrin‑A1通常附着在细胞表面,能够被剪切进入血液循环。它与一种称为EphA2的受体结合,而团队发现该受体在成骨细胞(osteoblasts)上高表达。通过对人类与小鼠组织进行单细胞测序、原位RNA成像以及先进的三维“DeepBone”透明化技术的检查,他们看到一致的模式:ephrin‑A1位于骨内血管的内膜细胞上,而EphA2则位于沿骨表面的成骨细胞上,常常相距仅几个细胞直径。这种布局使血管细胞与成骨细胞之间的直接细胞间通信不仅可行而且很可能发生。
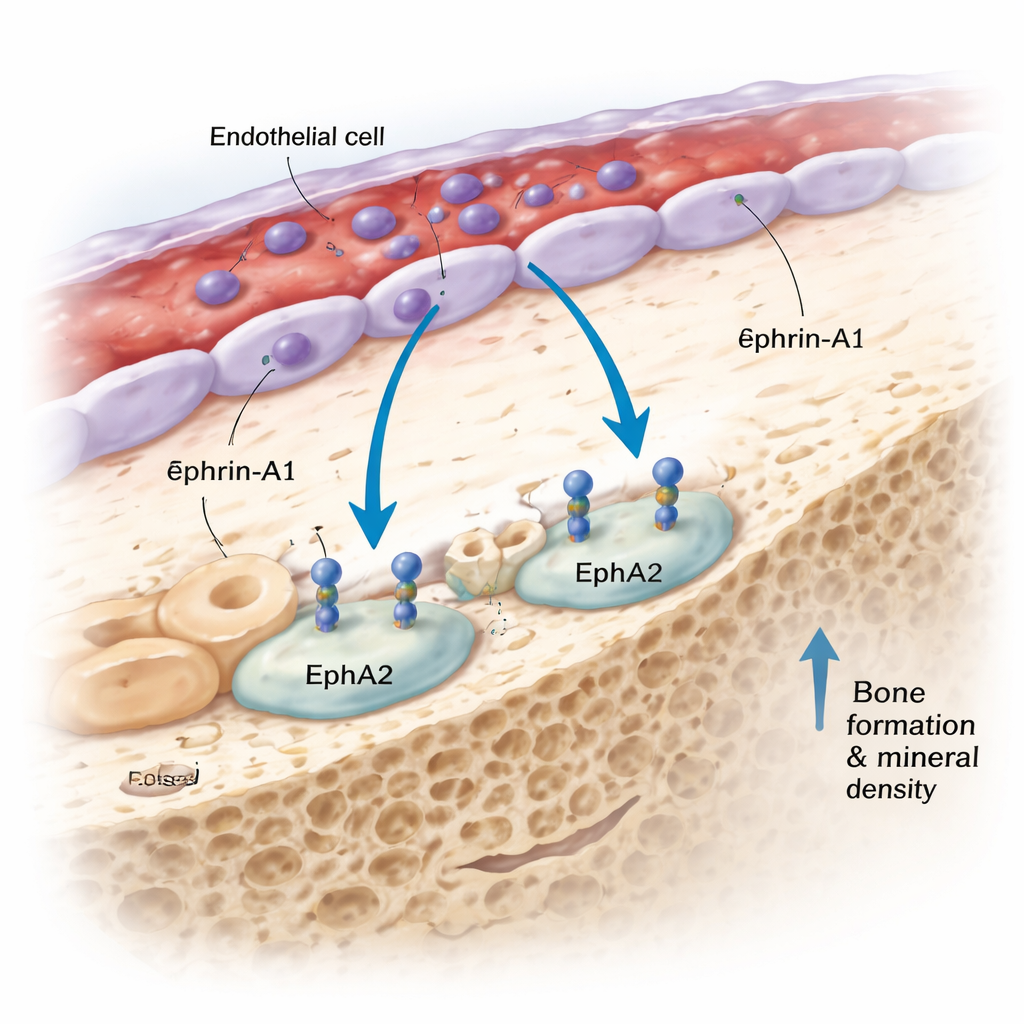
在活体骨骼中检验这一信号
为了弄清ephrin‑A1–EphA2的对话是否确实影响骨强度,研究人员转向小鼠遗传学实验。缺失ephrin‑A1或其受体EphA2的基因工程小鼠,其全身骨密度显著低于正常同窝对照,且在两性中均为如此。团队随后观察了这一信号对在不同小鼠模型中模拟人类骨质流失与骨量增加的行为如何变化。炎症、衰老以及高剂量维生素A——这些已知会削弱骨骼的因素——都与骨组织中ephrin‑A1和/或EphA2表达的降低相关。相比之下,模拟负重运动益处的机械负荷则提高了ephrin‑A1的表达。值得注意的是,这些变化并不完全与现有抗骨质疏松药物下看到的模式相同,暗示ephrin‑A1–EphA2可能通过一条不同的途径起作用,能够与现有疗法互补。
这对未来骨折预防意味着什么
总的来说,这项研究表明一种将遗传学与蛋白质数据相结合的复杂方法,既能重新发现已知的骨骼药物靶点,也能揭示新的靶点。研究指向ephrin‑A1与成骨细胞上的EphA2相互作用,作为维持骨密度和韧性的关键信号。对普通读者来说,结论是:我们的血液与基因中蕴含着关于骨骼如何保持强壮的详细蓝图——而ephrin‑A1现在成为该蓝图中一个有前景的新开关。如果未来的研究能够以安全的方式增强这一开关,例如开发能够增强ephrin‑A1–EphA2信号的药物,或许可以为预防骨折提供一种新的、潜在更安全的途径,尤其是对于目前尚未获治疗的众多群体。
引用: Movérare-Skrtic, S., Nethander, M., Li, L. et al. Identification of ephrin-A1–EphA2 signalling as a potential target for fracture prevention. Nat Commun 17, 1988 (2026). https://doi.org/10.1038/s41467-026-69863-6
关键词: 骨质疏松, 骨密度, 骨折预防, ephrin-A1 EphA2, 孟德尔随机化