Clear Sky Science · zh
在水性缓冲液中通过选择性氢同位素交换用氘和氚对寡肽进行放射性标记
在原子层面追踪药物
现代药物越来越多地包含复杂的生物分子,例如肽和小型蛋白。为了了解这些药物在体内的分布和持续时间,科学家常常将一些普通原子替换为可以被追踪的稀有或放射性原子。本文提出了一种在水性溶液中直接“标记”肽类药物的方法,比早期大多数方法更接近真实的生物环境。
为何微小的原子替换至关重要
将普通氢替换为更重的同位素如氘或氚,会把普通分子变成强有力的科学示踪物。这些标记体的行为与原始药物几乎相同,但可被检测质量或辐射的灵敏仪器追踪。对于小分子药物,化学家已建立了广泛的工具箱来制备此类标记化合物。相比之下,用于标记更大、更易损的生物制剂(如肽和蛋白)的办法稀缺、常常复杂,并且不适合类似血液或细胞液的水性环境。作者旨在弥补这一空白:提出一种在水性缓冲液中直接、简便且可选择地将氘或氚插入肽组成单位的方法。
在水中一步完成的标记策略
团队关注一种称为氢同位素交换的反应,其中分子上的氢原子被来自氘气(D2)或氚气(T2)的重同位素替换。他们原位构建了基于铱金属的催化剂,并配以特定选择的膦配体作为助剂。在温和碱性缓冲液中加热时,该体系能活化氨基酸和短肽上的特定碳–氢键,并用来自气体的氘或氚置换这些氢。关键在于,这在一步完成、富水介质中进行,所需金属含量极低——这些条件对脆弱的肽类药物和实际实验室流程更为友好。 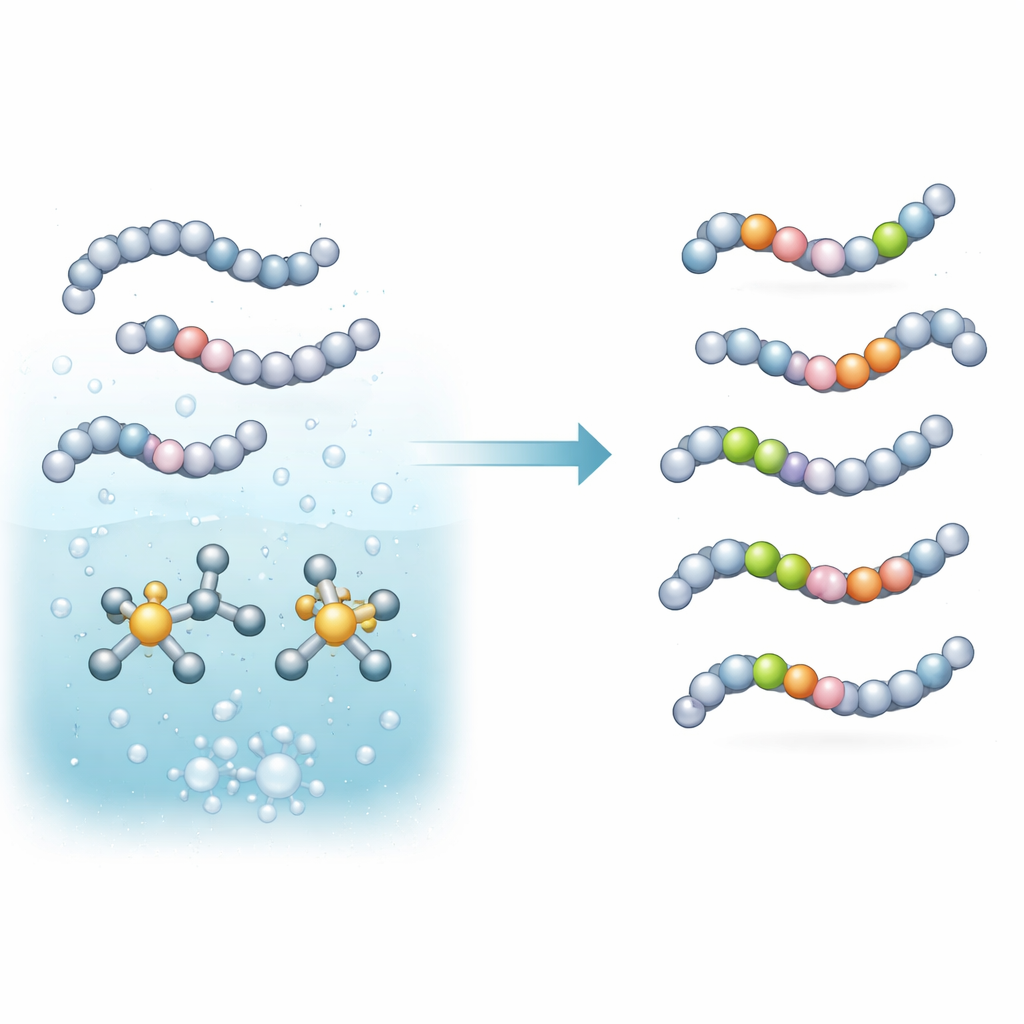
精确选择肽上的标记位点
并非肽中所有的氢原子都同样适合作为标记。有些在代谢过程中容易丢失,这会抹去放射性标记。作者仔细探究了催化剂偏好作用的位置。他们发现未保护的氨基酸如赖氨酸和精氨酸特别适合。在赖氨酸中,该方法选择性地标记侧链上的一个碳(所谓的γ位点),这是被认为“非活化”的位点,更有可能在体内保持稳定。精氨酸在其侧链的相邻位置也显示出类似行为。通过测试一系列相关分子,包括具有两个氨基的短链,团队发现当两个氮位点恰好定位时,有助于金属催化剂钳制分子并到达目标碳–氢键。
深入了解催化剂的工作机理
为理解这种选择性的来源,研究者将实验与使用密度泛函理论的详细计算机模拟相结合。这些计算描绘了从二聚体起始物形成铱配合物、与水结合、随后与氨基酸结合并最终插入特定碳–氢键的能量路径。模型显示,在水相中打破原始铱二聚体对一种前驱体来说在能量上是可行的,而对一类密切相关的前体则不可行,这解释了为何只有某些起始配合物有效。模型还揭示,底物本身有助于稳定活性金属中心并防止其凝聚成不活性的颗粒。最有利的途径涉及氨基酸通过两个氮原子配位,形成类似“钳子”的握持,使单个碳–氢键处于适合与氘或氚交换的位置。
从简单构件到真实肽药物
掌握机理后,团队将该方法从单个氨基酸扩展到含有多达七个残基的短肽,随后推广到多达13个氨基酸的更复杂类治疗序列。在所有案例中,标记发生在肽末端赖氨酸或精氨酸的侧链上,并且肽在反应条件下基本保持完整。针对氚标记,他们在低气压下优化了反应以安全实现高比活度,意味着大量分子至少携带一个氚原子。这些氚标记肽在一步反应中制得,可作为体外及潜在体内研究的示踪物使用。 
对未来药物的意义
这项工作表明,可以在简单的、基于水的步骤中选择性地将氘或氚连接到现实可行的肽药物上,同时针对关键氨基酸上代谢稳定的位置。对药物开发者而言,这意味着更容易获得精确标记的肽类示踪物,这对测量吸收、分布和代谢至关重要。除示踪物生产外,关于铱催化剂如何与氨基酸相互作用的机理见解,可能激发出新的方法来微调复杂生物分子的修饰位置与方式,从而为未来生物药物的更精确化学控制开辟道路。
引用: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
关键词: 放射性标记肽, 氢同位素交换, 氘和氚标记, 肽类治疗药物, 铱催化