Clear Sky Science · zh
ERCC6L2 确保交错末端DNA双链断裂的修复准确性
这项发现为何对我们的DNA重要
你体内的每个细胞都不断遭受DNA损伤,尤其是最危险的一类:切断双螺旋两股的断裂。如果这些断裂未被正确修复,可能导致癌症、遗传性疾病,或使医疗性基因编辑失败。本研究揭示了一种此前被低估的“守护”蛋白ERCC6L2,它专门保护一种棘手类型的断裂,防止其演变成大片缺失和混乱的染色体。理解这一守护机制有助于解释一种罕见的人类骨髓疾病,也提醒我们某些基因编辑工具在易感患者中可能引发严重后果。
不同类型的DNA断裂,不同的风险
并非所有DNA断裂都相同。有些切口很整齐,两股在同一点断开,就像把绳子平直切断。另一些则是交错的,留下短的悬垂末端,不能完美对齐。现代基因组编辑器如Cas9通常产生整齐的钝端切口,而像Cas12a、TALEN和一些成对切割的nickase系统则产生交错的、带突出端的断裂。研究人员通过敲低数千个基因,系统比较了人体细胞如何应对这两种断裂类型,以找出对每种切口特别重要的基因。
针对交错断裂的隐秘守护者
在这些全基因组筛选中,ERCC6L2 被发现是保护交错断裂的关键因子,但对钝端断裂大多并非必需。缺失ERCC6L2 的细胞仍能修复Cas9产生的钝端断裂,通常只产生小的插入或缺失,这是常见的DNA修复指纹。形成鲜明对比的是,当交错断裂由Cas12a、TALEN或双nickase Cas9 引入时,缺乏ERCC6L2 的细胞会产生更多成千上万碱基的大片缺失以及广泛分布的染色体重排(称为易位)。这些效应不仅在工程化细胞系中观察到,也出现在携带遗传性ERCC6L2 突变的患者骨髓细胞中,突显了该发现的临床相关性。 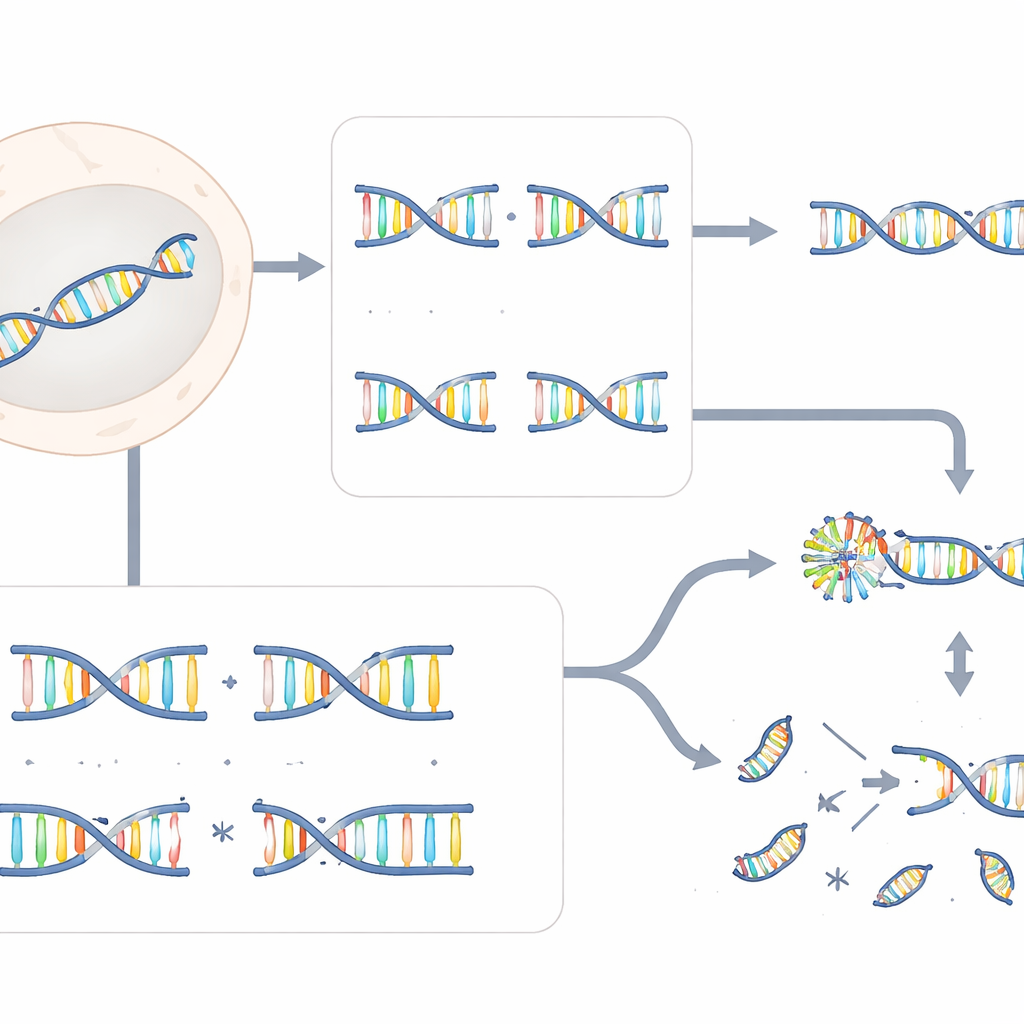
当大量断裂累积时,细胞开始失效
当团队同时在基因组中诱导多个交错断裂时,失去ERCC6L2 的危害更加明显。在这些实验中,缺乏ERCC6L2 的细胞生存困难,并且经常形成微核——这些小的、位置异常的含DNA小体表明染色体已破碎或分离错误。研究人员还转向一种天然产生交错断裂的来源:酶TOP2,它在细胞正常活动中通过短暂切断DNA来缓解超螺旋。一种化疗药物依托泊苷会将TOP2困在断裂状态,将这些暂时的切口转化为持续的交错断裂。缺失ERCC6L2 的细胞对依托泊苷显著更敏感,并表现出过度的DNA末端侵蚀,这与Cas12a诱导的断裂所见相似。
ERCC6L2 如何控制损伤处理机器
为理解ERCC6L2 在分子层面的作用,研究团队在体外用纯化蛋白和DNA 重建了这一过程。他们发现ERCC6L2 可结合多种DNA 结构,但具有一项特殊能力:它能主动“熔解”或解开交错断裂上的短突出末端,这一过程依赖其耗能的马达活性。在细胞内,ERCC6L2 抵消另一套修复机器MRN 复合体的作用,后者通常会啃咬DNA 末端以产生单链DNA 伸展。适度的切除在某些修复途径中是有益的,但一旦过度就会导致大片缺失和染色体破碎。在缺失ERCC6L2 的细胞中,MRN 驱动的切除在交错断裂处失去控制。阻断MRN 或其调节因子ATM 能逆转过度的DNA 咀嚼并降低大片缺失的发生率,显示ERCC6L2 通常对该通路起到抑制作用。
这对患者与基因组编辑意味着什么
综合这些发现,作者提出ERCC6L2 在交错DNA断裂处充当专门的守护者。通过熔解突出端并促进快速、整洁的重连,它防止了长片段DNA的丢失和远处染色体间的不当连接。在天生携带ERCC6L2 突变的人群中,日常产生的交错断裂——尤其是由TOP2 产生的那些——可能积累为未被修复或错误修复的损伤,推动骨髓功能衰竭、白血病,及可能的某些神经系统问题。对于基因治疗,这项工作发出明确警示:那些刻意产生突出末端切口的基因编辑工具(如Cas12a、TALEN或某些nickase 设计)在这些患者中可能特别危险。选择避免交错断裂的编辑策略,可能对应确保修复目标基因时不会意外破坏整个基因组至关重要。 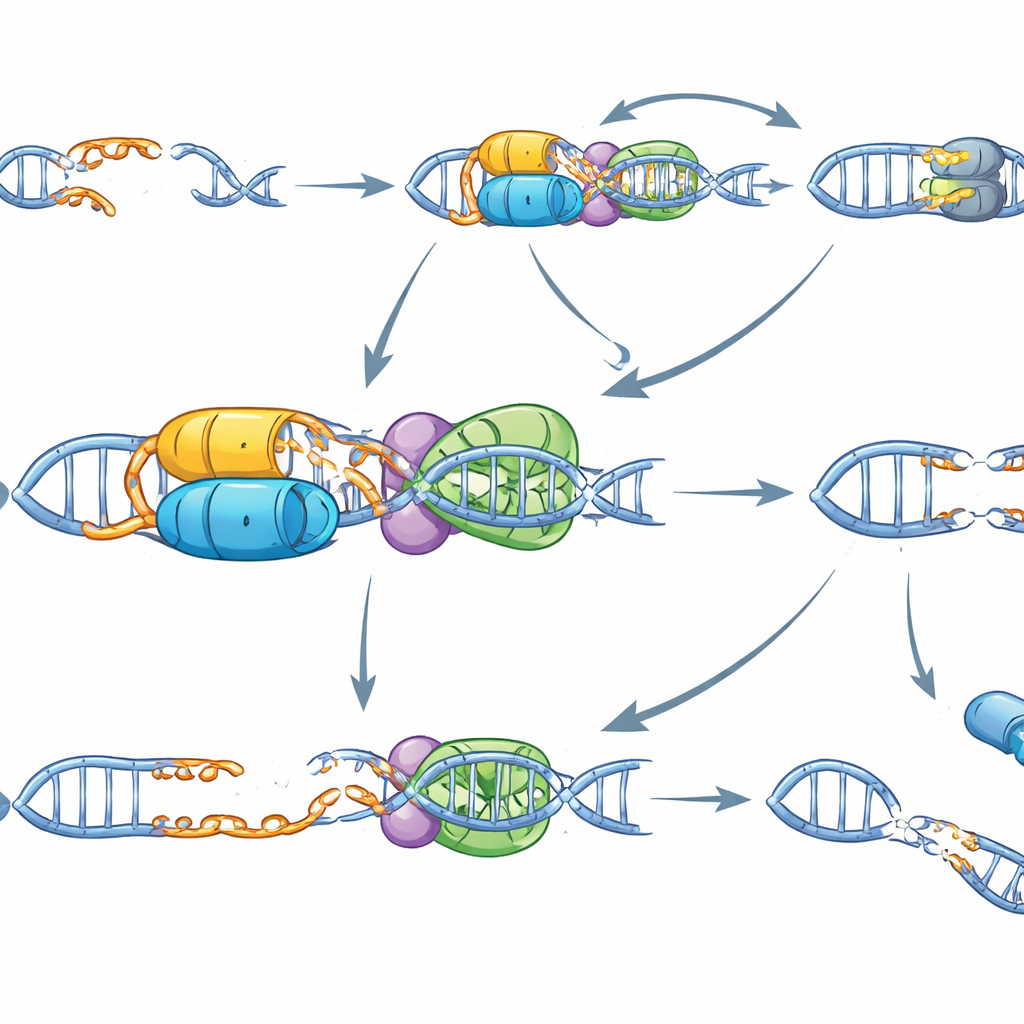
引用: Aird, E.J., Serrano-Benitez, A., Siegner, S.M. et al. ERCC6L2 ensures repair fidelity for staggered-end DNA double-strand breaks. Nat Commun 17, 2743 (2026). https://doi.org/10.1038/s41467-026-69843-w
关键词: DNA 修复, 基因组编辑, 双链断裂, ERCC6L2, 染色体不稳定性