Clear Sky Science · zh
利用无菌小鼠肠道生物反应器对益生菌进行定向进化以对抗非酒精性脂肪肝
为什么这个肠道故事关系到你的肝脏
非酒精性脂肪肝(NAFLD)如今影响数亿人,其发生与饮食和肠道健康密切相关。本研究探讨了一个不同寻常的想法:把肠道本身当作一种“活的工厂”,用来“训练”有益细菌,使其成为更有效的药物。研究者在无菌小鼠体内、在高脂饮食压力下让益生菌进化,从而培养出一种更高效处理胆汁酸的细菌株。胆汁酸是类似洗涤剂的分子,将我们摄入的食物与肝脏如何储存脂肪连接起来。这项工作表明了一种新路径:制造下一代益生菌时,可以让它们天然地适应宿主,而不仅仅在试管中工程化改造。
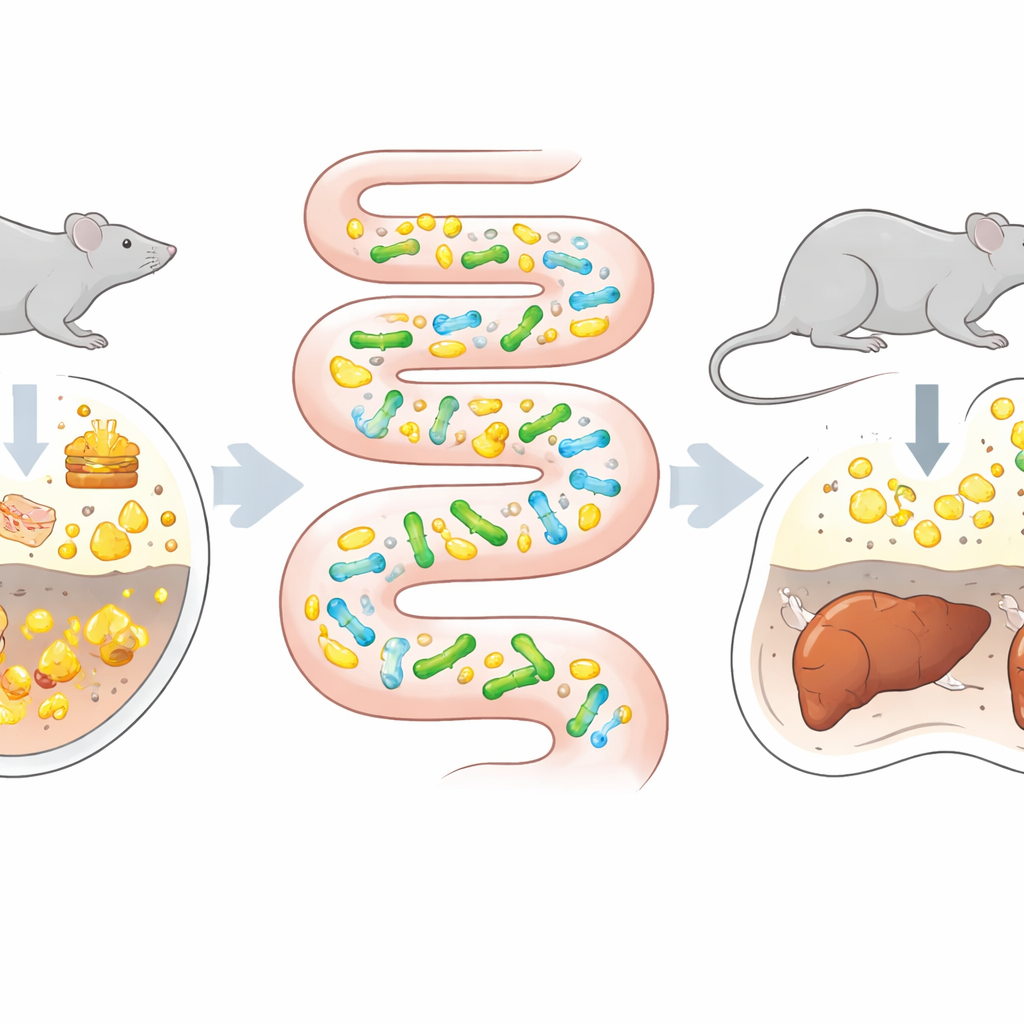
把肠道变成进化室
传统的定向进化——诱变微生物并挑选表现最佳者——通常在实验瓶中进行。这种方法适用于酶或工业微生物,但常常不适用于益生菌,后者必须应对肠道中复杂的化学成分、免疫信号和物理力学条件。作者们设想:如果把肠道自身及其自然选择压力作为筛选环境,会怎样?他们选择了已具备部分分解胆汁酸能力的益生菌种Bifidobacterium animalis subsp. lactis。无菌小鼠(体内无其他微生物)被该菌株定殖,随后喂以逐步升高脂肪和胆固醇的饮食,这种饮食会提升肠道胆汁酸水平。与此同时,同一菌株也在含胆汁酸的标准实验培养基中进行体外适应,以便直接比较体外与体内进化的效果。
肠道训练出的益生菌胜过在实验室训练的同类
在培养瓶中反复传代后,实验室进化的细菌在处理胆汁酸的能力上并未显示出有意义的提升。形成鲜明对比的是,从高脂喂养小鼠肠道中分离出的菌株表现差异很大;约四分之一显示出明显更强的胆汁酸分解能力。表现最突出的一株被命名为W5S9,其代谢胆汁酸的效率比母株高出77%。这种多样性以及既有胜出者也有落后者的现象,凸显了宿主肠道环境施加的复杂多维选择压力,是简单实验培养基无法模拟的。研究也证实,肠道可作为强大的“生物反应器”,在与真实生活条件接近的环境中不断产生并检验基因变体。
聚焦关键的突变
为了解W5S9内部发生了哪些变化,团队对其基因组进行了测序,并比较了与原始菌株相比哪些基因表达上调或下调。在数百处小的DNA差异中,两个突变尤其突出。一处位于名为cbh基因的上游,该基因产生一种切割胆盐的酶;该变异像一个更强的开启开关,在胆汁胁迫下提高了该酶的产量。第二个突变改变了一种转运蛋白(MDR)的结构和活性,该蛋白负责将处理后的胆汁酸泵出细胞。体外实验显示,这些调整使益生菌在切割缀合胆汁酸和输出产物方面更有效,从而在胆汁丰富的恶劣环境中提高了其存活能力。换言之,肠道内的进化微调了胆汁酸代谢途径中的“剪刀”和“出口门”。
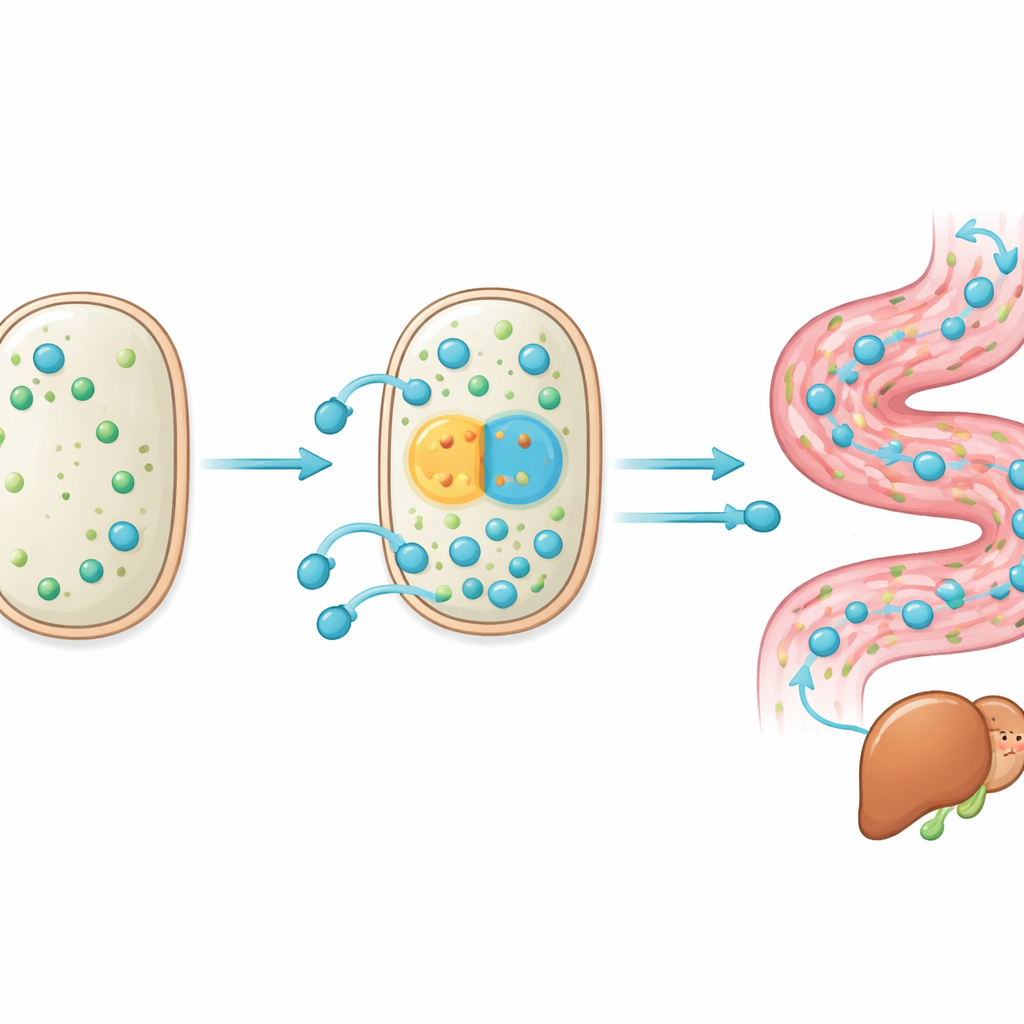
在饮食胁迫的个体中保护脂肪肝
关键的考验是这种肠道训练的菌株是否能真正保护动物免受肝损伤。研究者使用了NAFLD小鼠模型:长期高脂饮食导致体重增加、肝脏脂肪堆积和炎症。小鼠被分为四组:正常饮食、高脂单独组、高脂加原始益生菌组以及高脂加适应后的W5S9组。与高脂组相比,两组益生菌组都有所改善,但W5S9始终表现更好。这些小鼠体重增幅更小,胆固醇谱更健康,肝损伤与炎症的标志物更低,肝组织中可见的脂滴也明显更少。对粪便的详细化学分析显示,W5S9更强烈地降低了与疾病相关的胆汁酸,并将胆汁酸池推回更健康的平衡,而并未大幅重塑整体肠道微生物群落。
这对未来益生菌药物意味着什么
对非专业读者而言,关键观点是:研究者并非仅仅找到一个“好”的益生菌,而是利用宿主体内的自然选择来塑造出更好的菌株。通过在无菌小鼠内让自然选择在精心设计的高脂、高胆汁环境中发挥作用,他们得到了一株更有效处理胆汁酸、从而更好保护肝脏免受饮食诱发损伤的菌株。由于未引入外源DNA,这些进化后的微生物仍属非转基因(non-GMO),这可能有助于减轻监管和公众的顾虑。更广泛的含义是,类似的宿主引导进化策略可针对其他疾病进行定制,从炎症性肠病到代谢性甚至神经性疾病,开启了通往个性化、功能性调谐活体微生物疗法的大门。
引用: Han, Z., Sun, Z., Liu, X. et al. Harnessing a germ‑free mouse gut bioreactor for directed evolution of probiotics to combat non-alcoholic fatty liver disease. Nat Commun 17, 3133 (2026). https://doi.org/10.1038/s41467-026-69823-0
关键词: 益生菌, 肠道微生物组, 胆汁酸, 脂肪肝疾病, 定向进化