Clear Sky Science · zh
来源于β细胞的胆囊收缩素促进与肥胖相关的胰腺腺癌发展
过重如何“对话”胰腺
众所周知,肥胖会增加胰腺癌的风险——这是死亡率极高的癌症之一——但将多余体脂与肿瘤联系起来的生物学“对话”一直不明朗。这项研究揭示了一个意想不到的信使:一种称为胆囊收缩素(CCK)的消化激素,它在胰腺的胰岛素产生细胞内产生。通过追踪这些细胞在代谢压力下的变化,作者展示了本应帮身体应对挑战的激素如何反过来助长癌变,并提出了在疾病成形前拦截它的新方法。
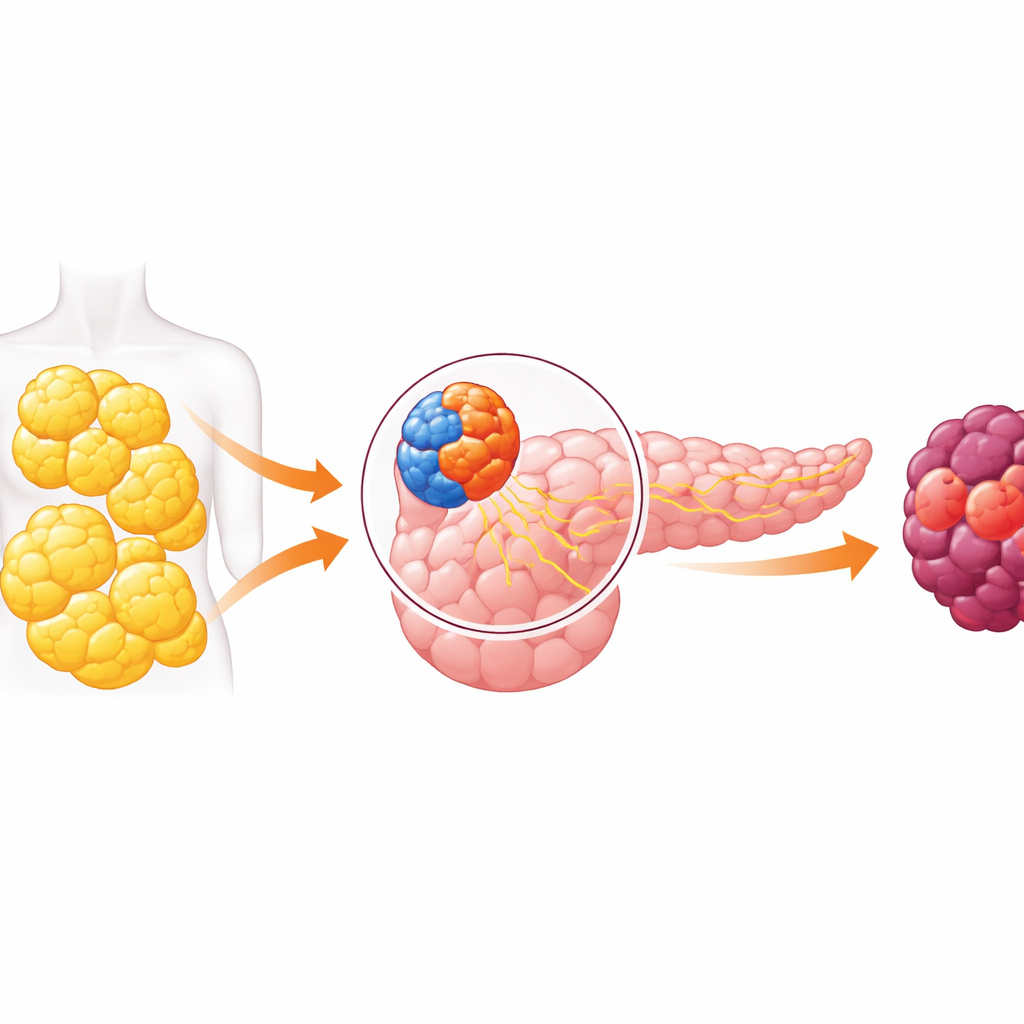
一器官两面与危险的对话
胰腺有两项主要功能。一方面是内分泌部分,含有释放胰岛素等激素以控制血糖的小岛群;另一方面是外分泌部分,产生消化液,并包含最常起源于胰腺癌的细胞。多年来,研究者普遍认为这两部分在很大程度上相对独立。近期工作推翻了这一观念,表明来自产生激素细胞的信号可以影响邻近的消化细胞。本文深入研究了这种跨区“对话”,并发现肥胖时它会将胰腺的消化侧推向癌变方向。
激素细胞的压力引发新信号
在肥胖状态下,产生胰岛素的β细胞面临持续的压力,必须满足身体日益增加的胰岛素需求。研究者利用单细胞RNA测序和先进的计算工具,跟踪小鼠从瘦到超重再到严重肥胖过程中单个β细胞的变化。他们发现一部分未成熟的β细胞扩增并逐渐失去其特化的胰岛素身份。随着这些细胞变得应激,蛋白折叠负荷和细胞损伤的标志增加,而胰岛素产生下降。与此同时,这些细胞开始大量产生CCK——一种通常与肠道相关、能刺激消化细胞生长和改变的激素。
从有益激素到癌症燃料
为检验新产生的CCK是应激的副产物还是疾病的主动驱动因子,团队构建了β细胞即便在无肥胖情况下也过表达CCK的小鼠。这些动物尽管体重和血糖正常,却出现了与肥胖小鼠相似程度的胰腺癌前病变和侵袭性肿瘤。相反,当在肥胖小鼠的胰腺中有针对性地去除CCK时,肿瘤负担显著下降,尽管这些动物仍然肥胖且胰岛素水平较高。在多种小鼠模型中,胰腺内的CCK水平与肿瘤量密切相关,而胰岛素水平往往呈相反趋势。这些结果表明,在这些体系中,CCK——而非胰岛素——是将肥胖与胰腺癌联系起来的主要激素。
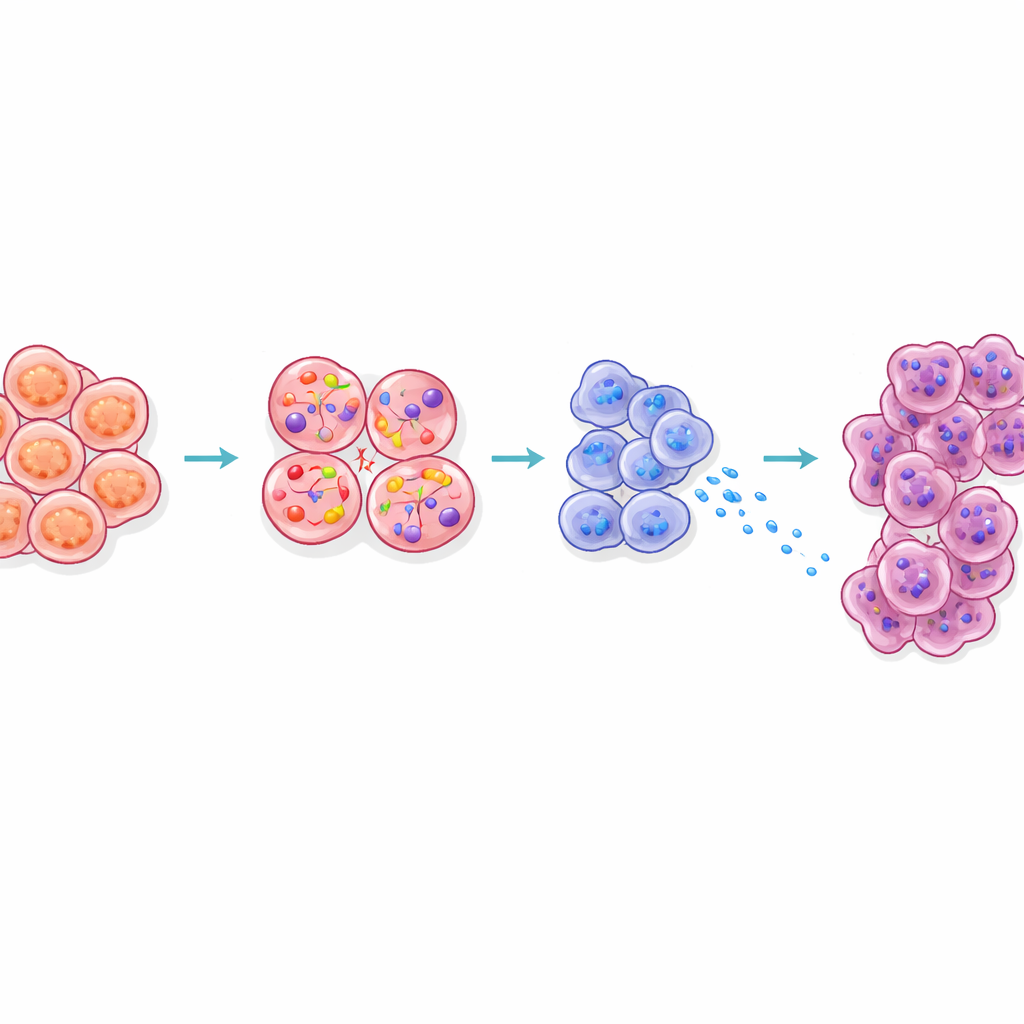
信号如何到达并激活邻近细胞
研究还考察了来自β细胞的CCK如何重塑周围组织。腺泡细胞通常分泌消化酶,位于胰岛旁边。在肥胖小鼠中,靠近胰岛的腺泡细胞显示出应激特征,产生更多消化酶和称为Reg的蛋白,并转变为更容易被转化为癌细胞的状态。在肥胖小鼠中阻断CCK信号能降低这些Reg信号。三维成像进一步显示,早期癌前病变在肥胖动物中倾向于异常靠近胰岛形成。综合这些结果,提示应激的β细胞分泌的CCK在胰岛周围形成一个“高风险区”,使得消化细胞更容易被促成肿瘤形成。
与人类糖尿病的共性模式与关键开关
通过将小鼠数据与来自有无2型糖尿病患者的人类胰腺组织进行比较,作者发现了显著的相似性:来自糖尿病供体的β细胞映射到与肥胖小鼠中相同的应激、去成熟状态。随后他们使用调控分析来探寻在β细胞中何种机制开启CCK表达,确定了以蛋白cJun为中心的应激响应通路。当在肥胖小鼠或培养皿中的类β细胞中阻断上游的JNK–cJun通路时,CCK水平下降,并观察到cJun在CCK基因的一个调控区附近结合。这表明慢性应激激活JNK–cJun,进而将β细胞翻转为产生CCK的模式。
对有风险人群的意义
对普通读者而言,核心信息是:在肥胖和糖尿病的压力下,胰腺中的胰岛素细胞不仅功能衰退——它们还发生适应性改变,反而无意中促使邻近细胞形成癌变。其方式是开启CCK,这种激素对邻近的消化细胞既是生长信号也是应激信号,帮助创造了有利于肿瘤生长的环境。因为胰腺来源的CCK并非维持血糖控制所必需,针对这一特定激素来源或其由应激激活的开关,理论上可以在不破坏整体激素平衡的前提下降低肥胖或2型糖尿病人群的胰腺癌风险。这项工作将胰腺癌重新框定为该器官两侧间误导性通信的问题,并指出了早期预防的新途径。
引用: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
关键词: 胰腺癌, 肥胖, β细胞, 胆囊收缩素, 2型糖尿病