Clear Sky Science · zh
复合 SMG5‑SMG6 PIN 域的形成对 NMD 至关重要
细胞如何保护自己免受错误信息的伤害
我们的细胞不断读取遗传信息(mRNA)来合成蛋白质。但这些信息有时包含提前的终止信号,会产生截短且可能有害的蛋白质。消除此类错误信息的过程称为无义介导的 mRNA 降解(NMD)。本文揭示了两个关键蛋白 SMG5 和 SMG6 如何通过物理合作切割有缺陷的信息,解释了细胞质量控制机制中长期存在的一个谜题。
发现隐秘的协作关系
多年来,科学家们知道 SMG6 能直接切割 RNA,而 SMG5 被认为“催化上失活”,主要起辅助或支架作用。然而细胞实验显示了一个令人困惑的现象:SMG6 若无 SMG5 就无法正常工作,而且任何一方缺失都会导致 NMD 崩溃。作者使用了最先进的结构预测(AlphaFold)、用纯化蛋白进行的生化测定以及人类细胞系中的遗传学检验来解决这一矛盾。他们的模型预测 SMG5 和 SMG6 的尾部区域,称为 PIN 域,会相互靠近对接,形成一个联合结构。这个复合单元——被称作“cPIN”——被提出为 NMD 中真正的切割机器。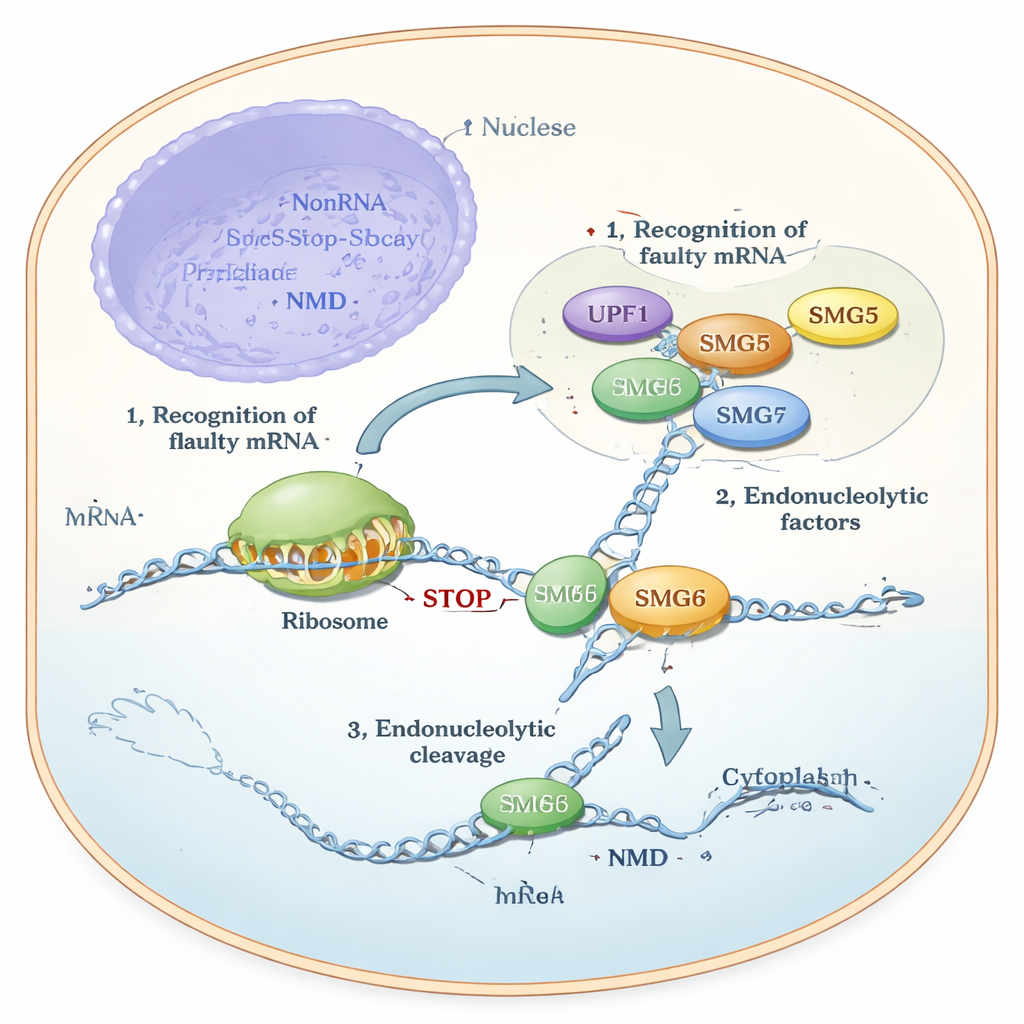
在试管中重建分子剪刀
为检验这一预测,研究团队在细菌中制备并纯化了人类 SMG5 和 SMG6 的片段。单独存在时,SMG6 对设计的 RNA 底物仅表现出弱的切割能力,而 SMG5 几乎没有任何切割活性。但当两者混合时,切割活性显著提高,即便在不太可能存在污染酶的条件下仍然如此。对线性和环状 RNA 测试分子都观测到相同效应,表明增强的切割确实来自 SMG5–SMG6 配对。化学交联和质谱分析进一步显示两蛋白相互接触紧密,支持它们存在直接(即便是瞬时的)协作关系的观点。
完成切割的锋刃
结构模型精确地揭示了 SMG5 如何增强 SMG6。SMG6 提供四个酸性氨基酸,在切割位点的核心处结合金属离子,这是这类酶的典型特征。出乎意料的是,模型显示来自 SMG5 的另一个酸性残基恰好位于其旁,实质性地扩展了催化口袋。SMG5 上的其他带正电残基被预测可以抓握 RNA 主链并帮助将其定位以便切割。当研究者突变这些关键的 SMG5 或 SMG6 残基时,复合体在体外的切割活性大幅丧失。在经工程改造、正常蛋白被耗尽的人类细胞中,这些相同突变也无法恢复 NMD,将结构模型与真实细胞功能紧密联系起来。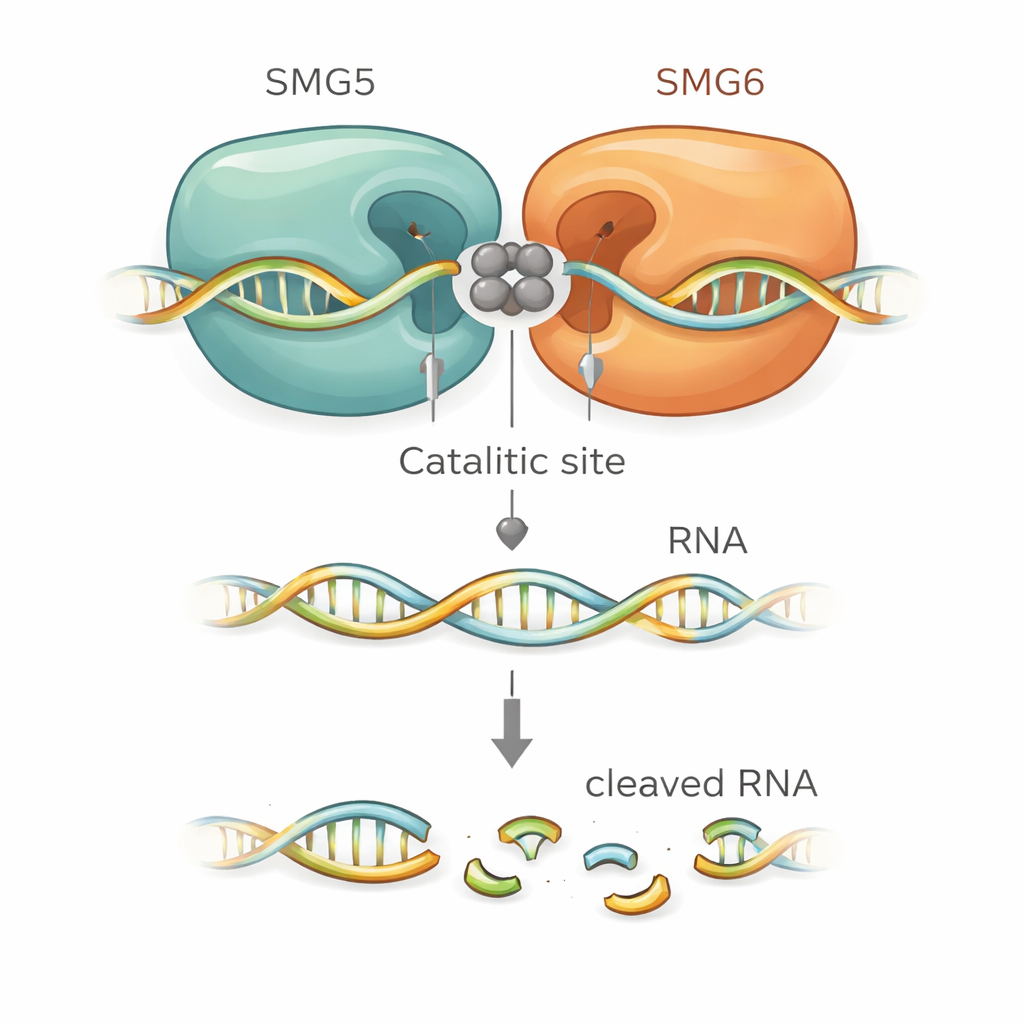
在细胞内证明两者同等重要
由于完全去除 SMG5 或 SMG6 会致细胞死亡,团队采用了一种“降解子(degron)”系统,使他们可以给每个蛋白加上标签,从而用小分子迅速摧毁该蛋白。将这种快速降解与 RNA 干扰相结合,几乎完全去除了 SMG5、SMG6 或一个名为 UPF1 的核心调控因子。随后的全基因组 RNA 测序揭示了失去每个因子时 NMD 会发生什么。耗尽 SMG5 或 UPF1 导致细胞 RNA 的变化几乎相同,易受 NMD 调控的有缺陷转录本强烈积累。去除 SMG6 也产生非常相似但略温和的效应。这些数据表明 SMG5 和 SMG6 并非可选的平行分支;相反,它们与 UPF1 一起作为一条主要降解通路的核心组分协同作用。
这对细胞健康为何重要
简而言之,这项研究表明 SMG5 和 SMG6 咬合在一起,形成一对单一而强大的分子剪刀,用以切除有缺陷的遗传信息。SMG6 提供了大部分刀刃,但 SMG5 补上了缺失的一侧并帮助固定 RNA,从而把一个弱切割酶转变为高效的切割复合体。这个复合“cPIN”解释了为什么细胞绝对需要这两种蛋白来保持 RNA 信息的清洁。通过阐明 NMD 关键切割步骤仅在识别出有缺陷的信息时被激活,这项工作为我们理解细胞如何防止有毒截短蛋白积累并精细调控基因表达提供了更清晰的图景。
引用: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
关键词: 无义介导的 mRNA 降解, RNA 质量控制, SMG5 SMG6, mRNA 监控, 基因表达调控