Clear Sky Science · zh
用于体外和细胞内研究蛋白质乙酰化的非水解性乙酰赖氨酸类似物
为什么蛋白上的微小化学标签很重要
在每个细胞内部,蛋白质不断被附加小的化学标签,这些标签像开/关开关或调光器一样调节蛋白的活性。其中一种最重要的标签称为乙酰化,它可以在不改变基因序列的情况下改变蛋白的行为。要精确理解在某一特定位点上的乙酰化作用为何,往往很困难,因为细胞内既可以快速添加这些标签,也能同样迅速地去除它们。这项研究提出了一种巧妙的化学“替代物”,它不可被去除,为科学家提供了一种将这些开关固定并观察后果的方法。
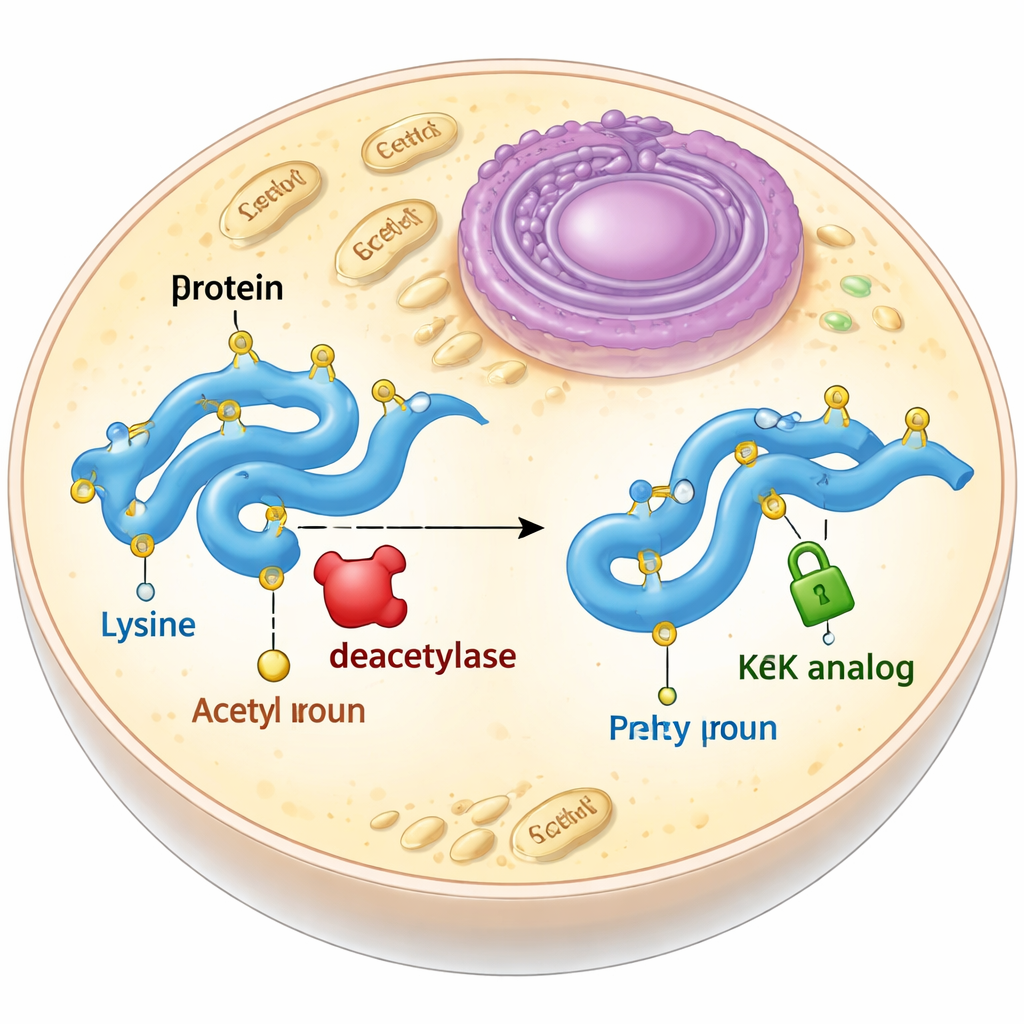
为瞬时标签提供一个稳定替代物
乙酰化通常发生在构成蛋白质的残基赖氨酸上。赖氨酸被乙酰化后会失去正电荷,侧链也变得略长。生物学家常用将赖氨酸突变为谷氨酰胺来模拟这种变化,后者不带电但侧链更短,或通过扩展遗传密码直接引入真实的乙酰赖氨酸。但两者各有缺陷:谷氨酰胺不能完全复制乙酰化引起的构象变化,而真实的乙酰赖氨酸在细胞内很快被去乙酰酶切除。作者着手设计并测试那些保持合适尺寸和形状但不可被去除的乙酰赖氨酸拟体。
在模型蛋白上测试新的化学模拟物
研究团队首先以泛素为重点,泛素是一个小而研究透彻的蛋白,且本身会被修饰多种标签。通过先进的基因工程,他们在泛素的同一位点引入了不同的赖氨酸变体:天然的乙酰赖氨酸、两种不可去除的类似物TFAcK和酮赖氨酸(KeK),以及常见的替代物如谷氨酰胺、丙氨酸和精氨酸。随后他们检查这些变化如何影响泛素的构象和功能。高分辨率核磁共振(NMR)测量显示乙酰赖氨酸、TFAcK和KeK在结构上几乎产生相同的变化,尤其是在中心螺旋周围,而谷氨酰胺和其他简单突变则没有。用一种叫HDM2的酶进行的功能测试表明,携带乙酰赖氨酸、TFAcK或KeK的泛素表现相似,但与谷氨酰胺版本不同,这强调了侧链的长度和体积——而不仅仅是电荷——在功能上的重要性。
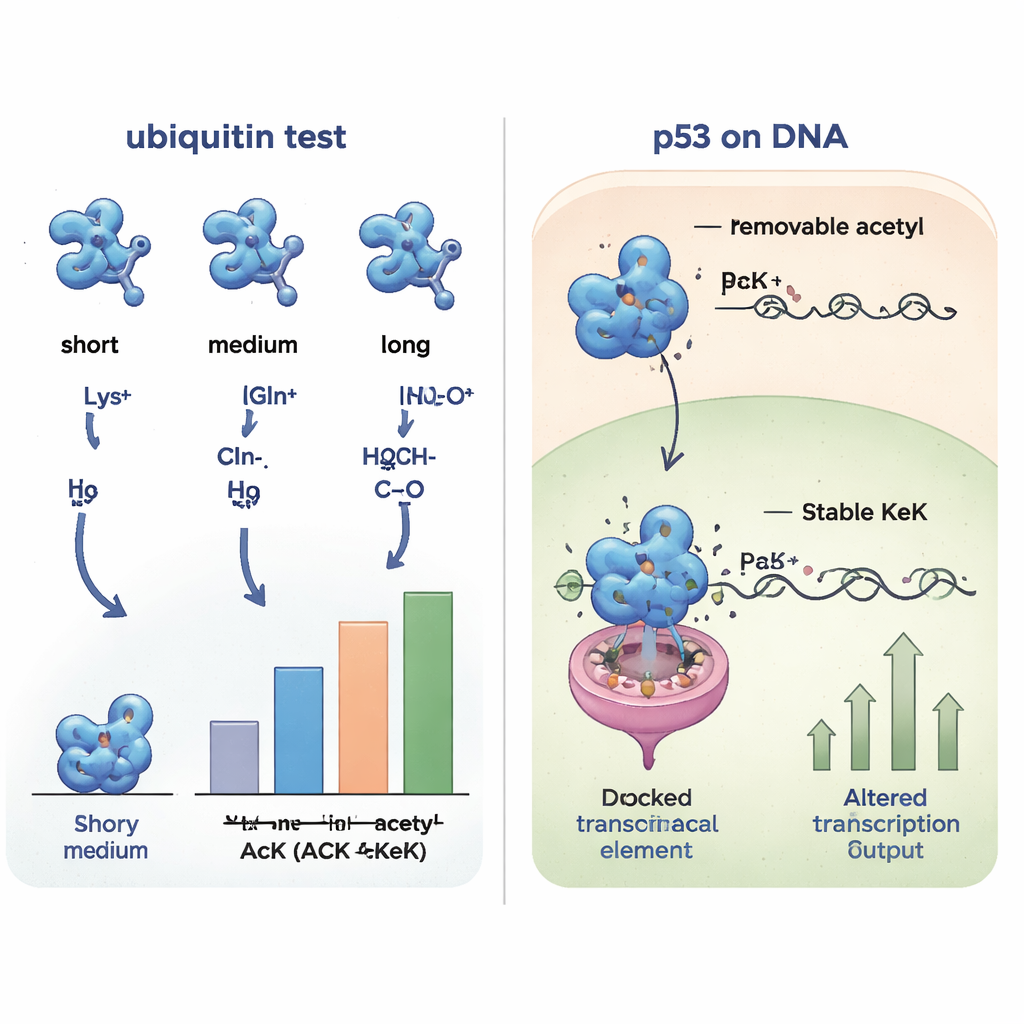
在细胞中探测蛋白相互作用网络
由于细微的结构变化会改变蛋白与哪些伙伴互作,研究者接着比较了不同泛素版本与来自人细胞裂解物中其他蛋白的结合情况。通过“捕捞”结合伙伴并用质谱鉴定,他们发现含有乙酰赖氨酸、TFAcK或KeK的泛素具有非常相似的相互作用谱,而含谷氨酰胺或丙氨酸的形式则聚为一类,表现不同。带正电的变体(赖氨酸或精氨酸)又形成了另一组。这个系统性比较表明,不可去除的拟体TFAcK,尤其是KeK,在再现真实乙酰化的结构和结合行为方面,要比传统的谷氨酰胺替代更为逼真。
在抑瘤蛋白p53上锁定乙酰化
为检验这些工具在活细胞内是否有效,作者把目光转向了p53,这个关键的抑瘤蛋白常被称为“基因组守护者”。p53的DNA结合区上的特定位点赖氨酸可以被乙酰化,从而改变它启动的基因,例如那些阻止细胞周期或触发细胞死亡的基因。团队改造了人类细胞,使得p53仅在提供相应的非标准氨基酸时,才在两个重要赖氨酸位点(120和164)中掺入乙酰赖氨酸、TFAcK或KeK。三者都能被嵌入p53,但细致测量显示在细胞内,乙酰基和TFAcK大多被去乙酰酶去除,而KeK则保持不变。当他们测试p53激活报告基因和天然p21基因的能力时,在这些位点携带KeK的变体活性显著降低,这与将那些位点的乙酰化“锁定”时的预期一致;而乙酰赖氨酸和TFAcK由于被去乙酰化,其行为更接近正常p53。
这对研究细胞决策意味着什么
总体而言,这项研究表明KeK是对乙酰赖氨酸的一种忠实且不可去除的替代物:它高度再现了乙酰化带来的结构变化、结合偏好和功能后果,但不会被细胞酶清除。对非专门领域的读者来说,这意味着研究者现在可以在蛋白的单个位点上“冻结”通常可逆的化学开关,然后观察这如何影响基因调控和细胞命运决策等过程。这应能更容易地将乙酰化的特定作用与其他重叠修饰区分开来,并最终澄清蛋白质乙酰化失调如何促成诸如癌症等疾病。
引用: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
关键词: 蛋白质乙酰化, 翻译后修饰, 泛素, p53, 遗传密码扩展