Clear Sky Science · zh
移植的人类神经祖细胞在转录组上的动态重塑揭示了大鼠视网膜色素变性模型中视力保护的机制
为何保护逐退的视力至关重要
视网膜色素变性是一组遗传性疾病,会缓慢夺走患者的视力,通常从夜盲开始,逐步发展到法律意义上的失明。由于导致该病的基因突变多达数百种,针对每一种突变采用基因治疗存在巨大困难。本研究探讨了一种更具普适性的策略:将实验室培养的人类神经祖细胞——未成熟的神经细胞——移植入眼内,以保护尚存的感光细胞。弄清这些移植细胞具体如何在体内表现并帮助维持视力,将有助于为视网膜色素变性及其他致盲疾病塑造未来疗法。
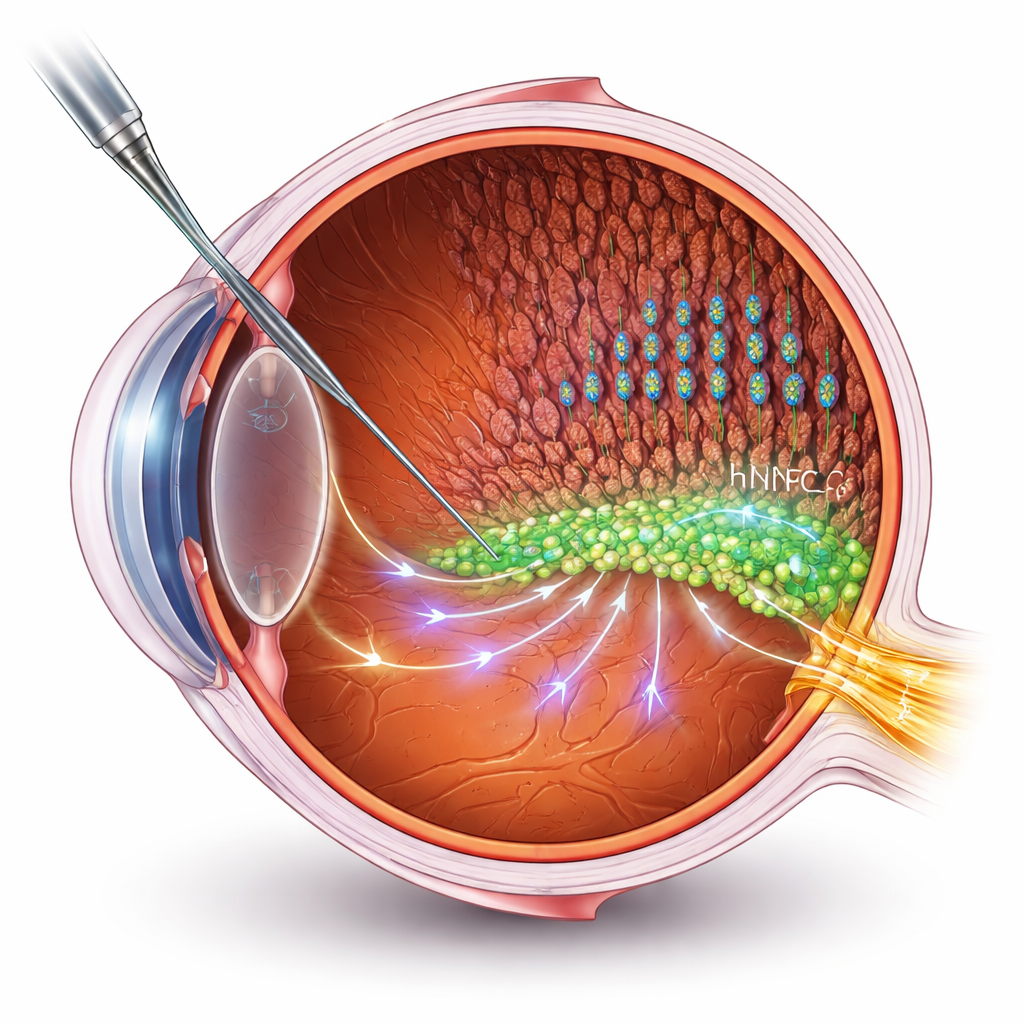
帮助细胞而非替代细胞
许多干细胞疗法旨在替换死亡或受损细胞。但在晚期视网膜疾病中,重建通往大脑的新连接是一个重大技术障碍。在这里,研究者采取了不同路径:将人类神经祖细胞(hNPCs)作为“助力者”来支持患者自身的视网膜细胞。他们将 hNPCs 移植到一种常用视网膜色素变性大鼠模型的视网膜下腔,并通过电生理记录和行为学测试来评估视力。与未处理动物相比,接受治疗的大鼠在视觉功能和光感受器(捕捉光线的杆状和锥状细胞)层结构的完整性方面表现更好,尽管退化仍在缓慢进行。
移植细胞在病变眼内如何改变
为了弄清分子层面的变化,团队使用了单细胞 RNA 测序,这一技术可以描绘出数千个单细胞中哪些基因被激活。他们在移植后的大体早期和晚期两个时间点追踪了移植的 hNPCs。大多数移植细胞并未转化为新的光感受器,而是成熟为类似星形胶质细胞的支持细胞,另有一小部分呈现出少突胶质细胞或未成熟神经元的标志。随着时间推移,这些细胞趋于稳定,表现出适应应激性退化环境并与邻近视网膜细胞密切相互作用的特征。
保护信号、代谢与清理机制
这些 hNPCs 产生了丰富的保护性蛋白质混合物,即营养因子。其中包括与细胞存活、降低氧化应激和抑制炎症相关的 MANF 和 MYDGF,以及支持神经细胞生长和迁移的 midkine(中连蛋白)和 pleiotrophin(多效素)等其他因子。这些分子似乎既作用于移植细胞自身,也作用于周围的视网膜。在接受治疗的大鼠中,杆细胞和锥细胞的基因表达模式更接近健康对照,视觉信号传递和细胞维持相关的支持增强。移植细胞还增强了与清除细胞碎片和调整代谢相关的通路,提示它们帮助光感受器应对疾病过程中积累的能量需求和有毒代谢产物。
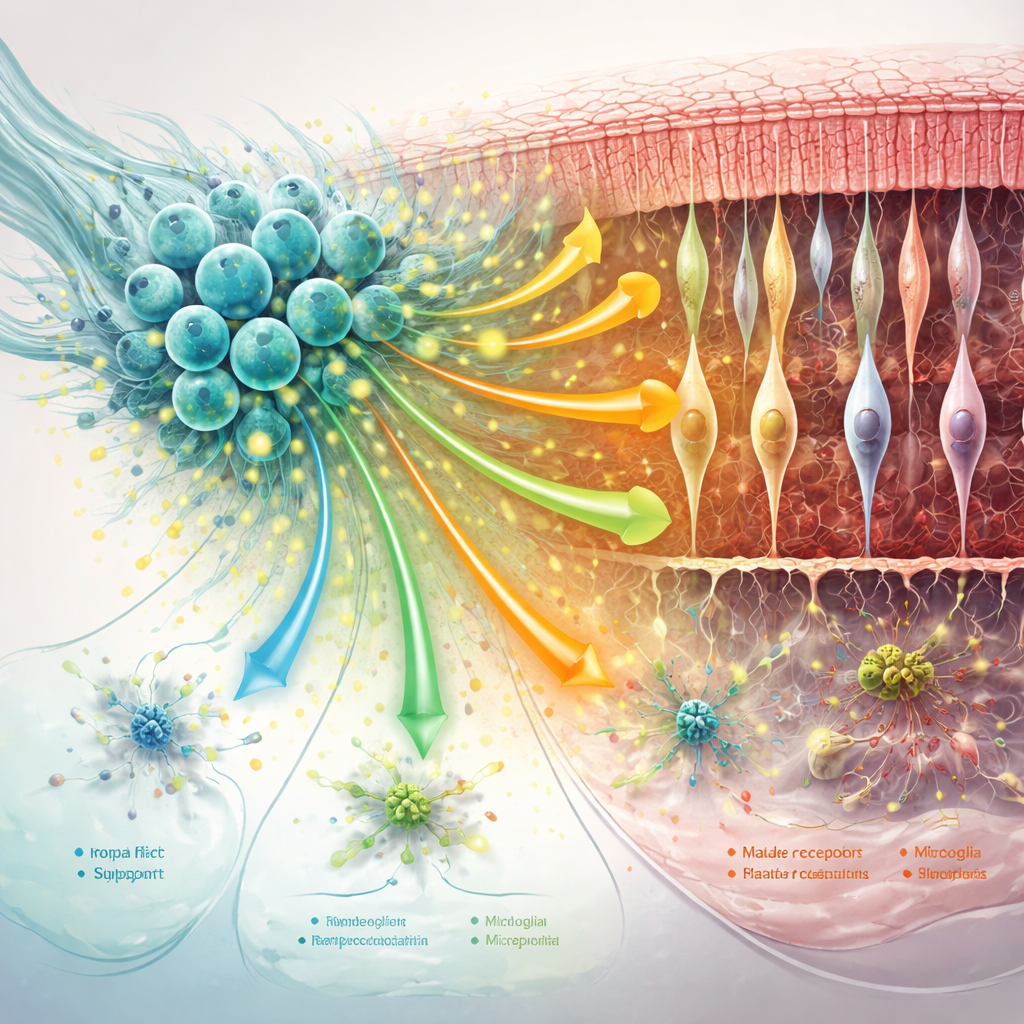
平抑反应性支持细胞并重塑视网膜微环境
视网膜的支持网络——穆勒胶质细胞、微胶质细胞以及周围的蛋白基质——在加剧或减缓退化中起重要作用。研究发现,hNPCs 治疗降低了穆勒胶质细胞中有害“反应性”变化的关键标志物,并使微胶质细胞远离过度炎症的状态,尤其在早期时间点更为明显。同时,有助于稳定突触、细胞粘附以及维持光感受器周围支架的通讯信号得到加强。随着疾病进展,这些益处部分减弱:细胞间总体通讯变弱,某些保护性通路——包括与 MANF 相关的信号——下降,支持细胞呈现出更多应激和免疫相关的表型。
对未来眼科治疗的意义
面向非专业读者,核心结论是:移植的人类神经祖细胞可以像现场的“急救员”一样在退化性视网膜中发挥作用。它们并不从零重建视网膜,但会释放保护性分子、调整代谢、抑制有害炎症并帮助维持局部结构,这些都能减缓视力丧失。然而,随着环境变得更为不利、移植物与宿主细胞之间的对话减弱,这种保护效应会随时间减退。作者建议,提升诸如 MANF 的关键因子以及改善宿主视网膜健康——可能通过对移植细胞进行基因改造或采用联合治疗——或许是将短暂缓解转化为持久视力保护的关键。
引用: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
关键词: 视网膜色素变性, 干细胞疗法, 视网膜退化, 神经保护, 单细胞 RNA 测序