Clear Sky Science · zh
TCL1A 在携带 NLRP7 致病变异的复发性葡萄胎中介导 DNA 甲基化缺陷
这对女性健康的重要性
有些妊娠在非常早期就出现异常,形成一团异常的胎盘组织而非正常发育的胎儿。这种病症称为葡萄胎,在部分妇女中会复发,有时还会进展为癌症。本研究深入探讨了导致这些罕见但严重妊娠问题的主要遗传原因,并揭示了卵细胞中单一失效防护机制如何扰乱指导正常发育的化学“标记”。
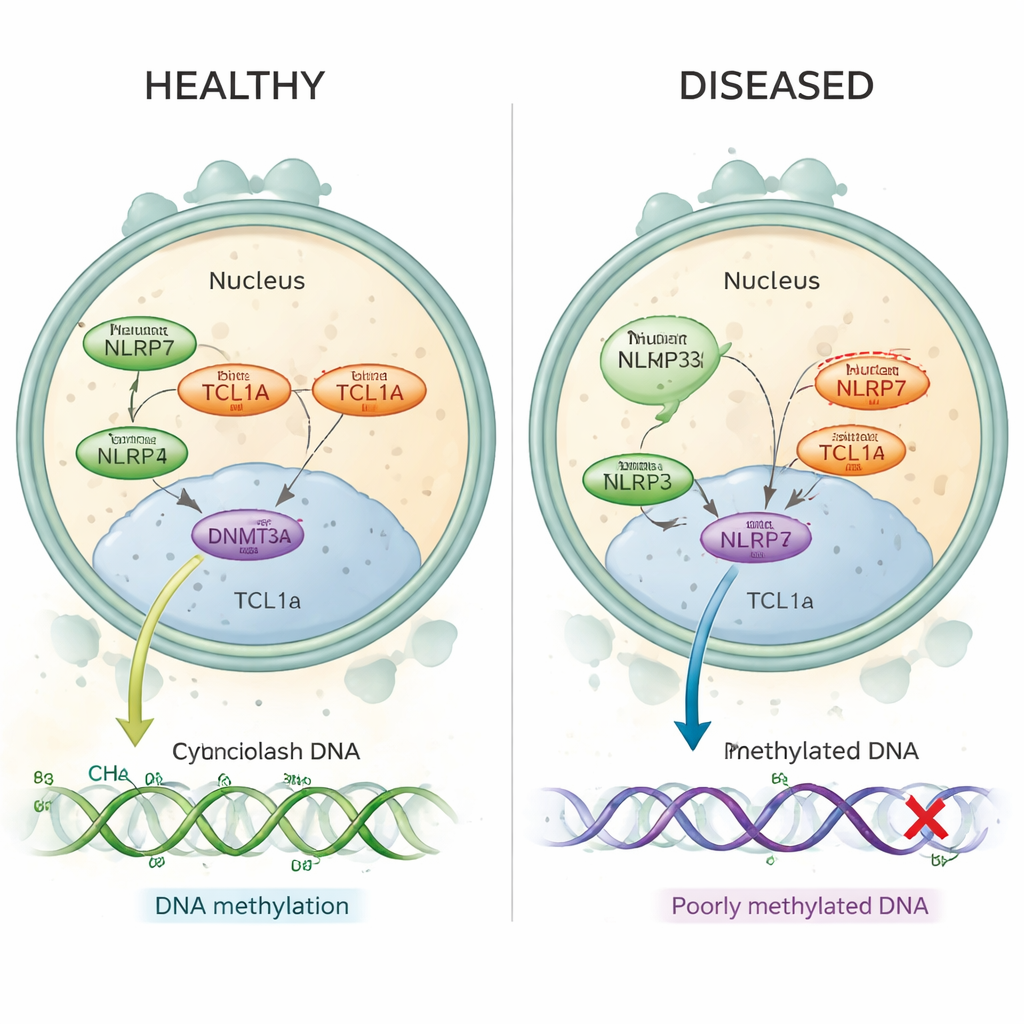
源自卵细胞的妊娠问题
复发性葡萄胎是一种疾病,患者会出现反复的葡萄胎妊娠,通常中间没有任何正常妊娠。现在已知许多此类病例是由名为 NLRP7 的基因发生有害变异引起的,该基因在受精前后即在卵细胞中表达。在这些女性中,本应带有来自母方“印记”的关键 DNA 区域缺乏正常的甲基化标记——这些小化学标签有助于在恰当时间开启或关闭基因。此前,科学家尚不清楚位于卵细胞胞质中的像 NLRP7 这样的蛋白,如何控制发生在包裹在细胞核内的 DNA 上的甲基化过程。
寻找缺失的搭档
为了解开这一谜题,研究人员检查了来自生育诊所的被舍弃的人类卵子和早期胚胎。他们从这些细胞中拉下 NLRP7 及其已知伙伴,并鉴定出伴随出现的其他蛋白。其中一个脱颖而出:TCL1A,已知在血液肿瘤中可进入细胞核并干扰称为 DNMT3A 和 DNMT3B 的 DNA 甲基化酶。TCL1A 在人类卵子中含量异常丰富,提示其在卵子中具有重要作用。详细的相互作用测试表明,TCL1A 与 NLRP7 具有紧密且特异性的结合,而不与密切相关的其他蛋白结合,并且该复合体纳入了一个更大的卵细胞特有结构——皮质下母源复合体。
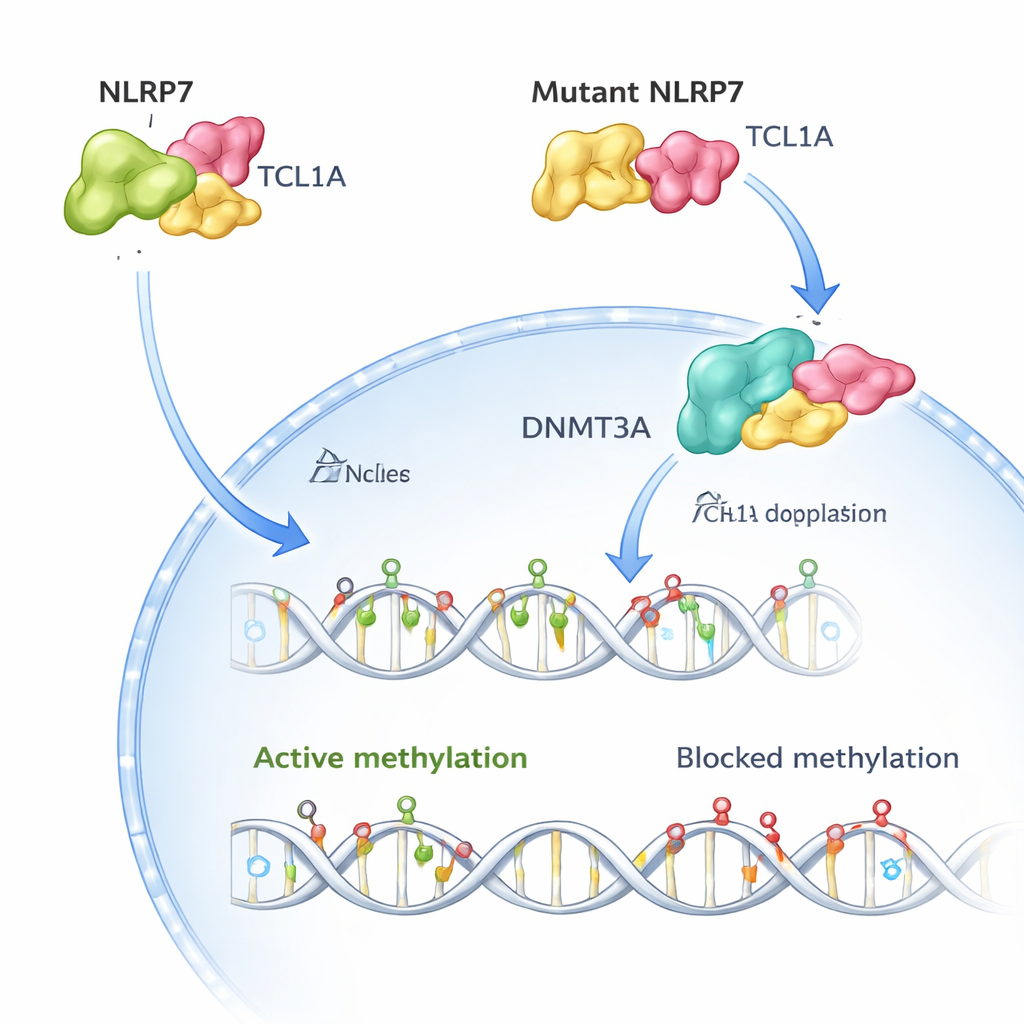
看到分子层的拥抱
研究团队随后使用冷冻电子显微镜可视化了 NLRP7–TCL1A 复合体的三维结构。他们发现两个 NLRP7 分子配对,每个 NLRP7 沿着由重复基序构成的弯曲表面握住一个 TCL1A 二聚体。这种构型解释了为何许多致病变异在 NLRP7 的该表面聚集:改变关键接触点会削弱或破坏与 TCL1A 的结合。当研究人员在细胞中重建 50 多种已知患者变体时,与复发性葡萄胎相关的大多数变体要么使 NLRP7 不稳定,要么显著降低其与 TCL1A 的结合能力。
蛋白错位如何扰乱 DNA 标记
在健康的人类卵子中,NLRP7 和 TCL1A 主要位于胞质中,只有少量 TCL1A 进入细胞核。作者展示了 NLRP7 实际上充当了一个守门员:当它能够抓住 TCL1A 时,TCL1A 被限制在胞质外。当 NLRP7 突变且无法很好结合时,TCL1A 会漏入细胞核。在那里它与将新甲基标记写入卵子 DNA 的主要酶 DNMT3A 结合,并抑制其活性。在通常随着分化而获得甲基化的干细胞模型中,过表达 TCL1A 导致全基因组范围内甲基化的显著丢失,而与 NLRP7 共表达则部分挽救了该缺陷。这些发现共同支持一个简单的图景:正常的 NLRP7 将甲基化“刹车”(TCL1A)锁在胞质中,使 DNMT3A 能正常标注 DNA;而失效的 NLRP7 使该刹车滑入细胞核并阻断该过程。
从机制到诊断
除了说明复发性葡萄胎如何产生之外,该研究还提出了一种实用方法来判断患者中新发现的 NLRP7 变异是否真正有害。作者比较了三种方法——实验室中 NLRP7–TCL1A 结合的功能检测、基于计算的预测以及标准基因评分工具——并显示 TCL1A 结合丧失与致病变体高度一致。他们还在有复发性葡萄胎的家族中发现了先前未识别的有害变体 L766R,证实该变体既削弱蛋白质稳定性又错误地将 TCL1A 引入细胞核。
通俗说来这意味着什么
这项工作揭示了一条分子连锁反应,解释了一种罕见但毁灭性的妊娠障碍。本质上,受累妇女的卵子携带一个失效的“保镖”蛋白 NLRP7,不能将其伙伴 TCL1A 禁锢在胞质中。一旦进入细胞核,TCL1A 干扰负责在 DNA 上写入关键化学标签的酶。没有这些标签,早期胎盘异常生长,胎儿无法形成。通过逐步追踪这一路径,该研究阐明了为何母体的某些遗传变异会反复破坏妊娠,并为有复发性葡萄胎的女性提供更精确的遗传咨询和诊断方向。
引用: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
关键词: DNA 甲基化, 复发性葡萄胎, NLRP7, TCL1A, 基因组印记