Clear Sky Science · zh
GCN5通过LXRα/SREBP1c信号通路介导的内源性脂质生成推动MASLD进展
为何这个肝脏研究重要
代谢功能失调相关脂肪性肝病(MASLD,原称非酒精性脂肪性肝病)目前约影响全球四分之一的人口。它常常无声发生,但可进展为肝纤维化、肝癌和严重的代谢紊乱。本研究揭示了一个分子“音量旋钮”,推动肝脏有害脂肪积聚,并表明调低该旋钮既能保护肝脏,也可能使现有的心血管药物策略更为安全。
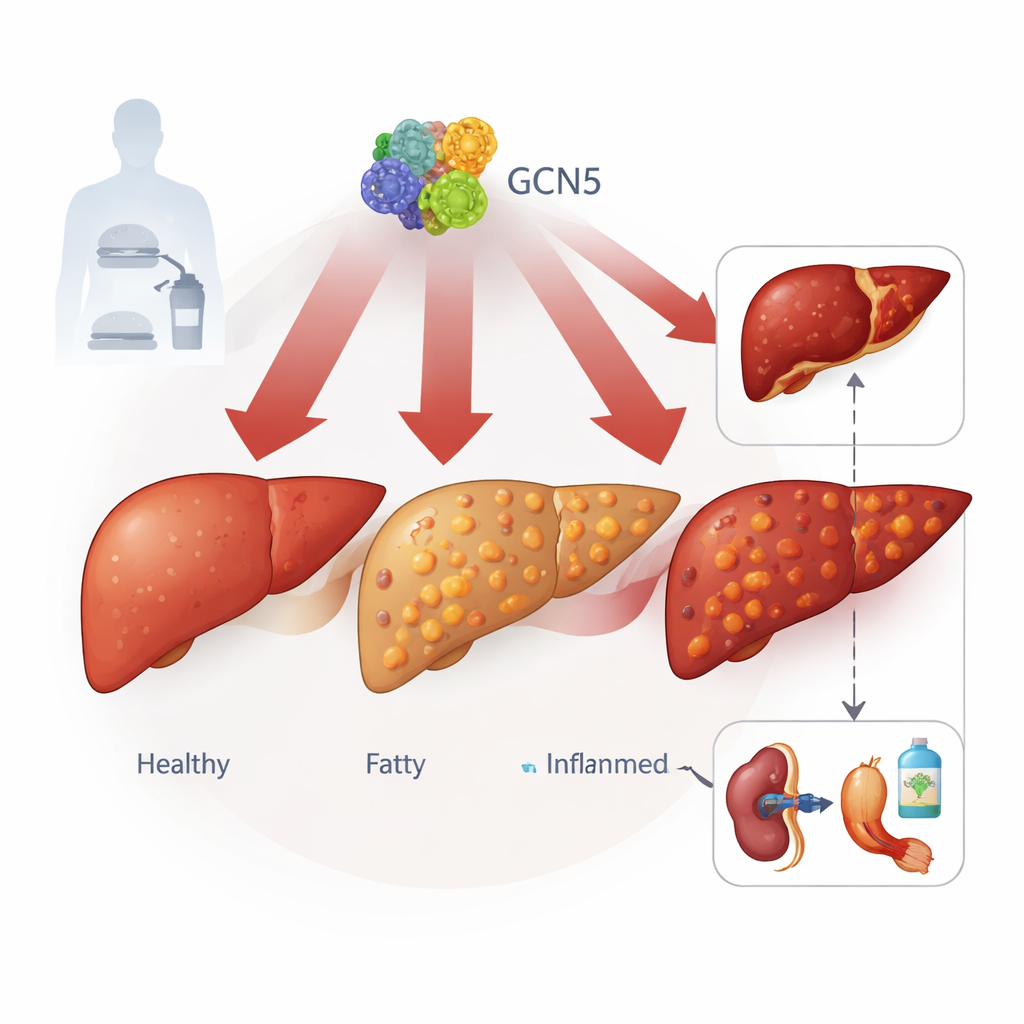
肝细胞内的隐秘开关
作者将注意力集中在一种名为GCN5的蛋白上,该蛋白以调控DNA包装紧密度而著称。通过研究来自100多名从健康到严重MASLD患者的肝组织样本以及若干饮食诱导脂肪肝的小鼠模型,他们发现肝细胞中的GCN5水平随着疾病加重而持续上升。与之密切相关的蛋白PCAF未显示相同模式,提示GCN5具有特殊作用。GCN5水平升高与更多的肝脂肪、更高的血脂以及更明显的肝损伤标志相关,将这一分子开关与临床疾病严重度联系起来。
在动物中调节GCN5的表达
为了检验因果关系,研究团队在小鼠肝细胞中特异性地增强或删除了GCN5。GCN5被提高时,接受高脂饮食的小鼠出现更大、更脂肪的肝脏、更高的血脂和更多的肝细胞损伤,尽管它们的食量和体重并未增加。在培养的肝细胞中也观察到类似现象:额外的GCN5导致更大且更多的脂滴。相反,肝细胞特异性缺失GCN5的小鼠则受到强烈保护。在多种模拟人类MASLD及其更严重炎症形式的饮食模型中,这些动物积累的肝脂更少,血脂和肝酶更低,炎症和纤维化也较轻。
GCN5如何推动肝脏合成脂肪
深入代谢层面,研究人员测量了肝脏中的多种脂肪酸及其前体。GCN5的缺失主要减少了肝脏自身合成的脂肪,即所谓的内源性脂质生成(de novo lipogenesis),而饮食来源的多不饱和脂肪酸则基本不受影响。基因表达和同位素追踪实验显示,GCN5位于脂肪生成主控因子SREBP1c的上游。当GCN5活跃时,参与合成和修饰脂肪酸的基因被激活,肝脏内部的脂肪合成速率上升。去除或阻断GCN5会将该程序调低,减少来自糖类到新合成肝脂的碳流入。
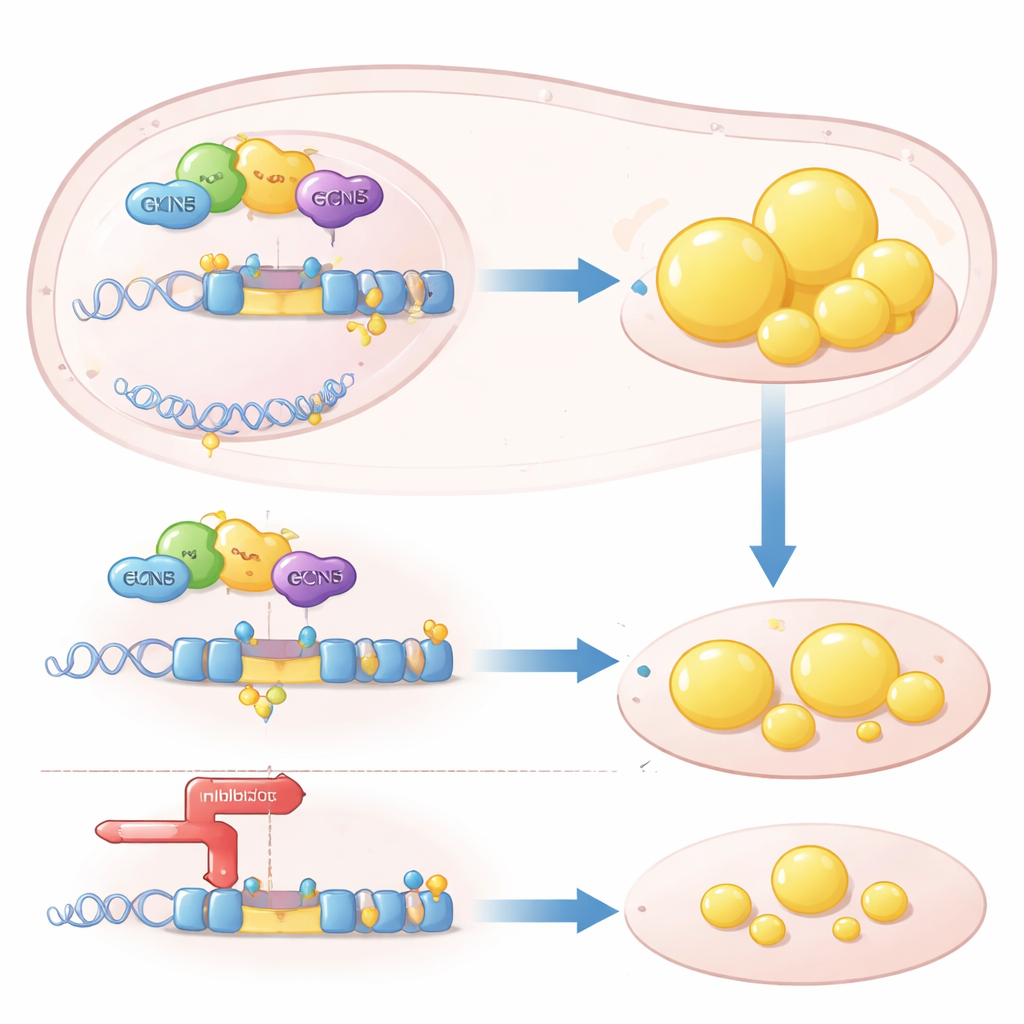
对关键脂肪基因的表观遗传杠杆作用
从机制上看,GCN5充当一种“表观遗传”杠杆:它通过化学修饰包裹DNA的组蛋白,使某些基因更易被读取。作者展示了GCN5与感知胆固醇相关分子的核受体LXRα一起被招募到SREBP1c基因的调控区域。到位后,GCN5在组蛋白H3上添加乙酰标记,松开局部染色质并增强SREBP1c的转录。这一效应高度选择性:GCN5增强了LXRα激活SREBP1c的能力,但并未增强另一个LXR靶基因ABCA1(其有助于组织清除胆固醇)。没有GCN5时,LXRα无法有效作用于SREBP1c的启动子,下游的脂肪合成程序因此受阻。
一种候选药物与有前景的联用策略
团队随后测试了CPTH2,这是一种在肝脏富集的小分子GCN5抑制剂。在已被置于高脂饮食的小鼠模型中,CPTH2减少了肝脏体积、脂含量和损伤标志物,且未见明显毒性或食量变化。在培养的人和小鼠肝细胞中,CPTH2仅在存在GCN5时降低脂滴和甘油三酯,证实其作用具有特异性。重要的是,在细胞和小鼠中与旨在改善胆固醇清除及对抗动脉粥样硬化的LXR激活剂共同处理时,CPTH2选择性阻断了SREBP1c驱动的脂肪生成上升,同时保留了促进逆向胆固醇转运的基因表达。在高脂饲喂小鼠中,与LXR激动剂联用时,CPTH2进一步降低了有害血脂和肝脏胆固醇,并防止了肝脏的额外脂肪积聚。
对患者意味着什么
该研究将GCN5定位为MASLD中肝脂积累的核心驱动因子,将饮食和激素信号与SREBP1c脂肪生成开关连接起来。因为GCN5似乎对LXR信号中有益的胆固醇清除臂并非必需,抑制GCN5的药物——例如CPTH2或更先进的后续药物——有望在控制肝脂和炎症的同时,允许对心脏有保护作用的治疗发挥作用。对于同时面临脂肪肝和心血管疾病风险的人群,靶向这一表观遗传开关未来可能为在不牺牲改善胆固醇处理益处的前提下保护肝脏提供一种途径。
引用: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
关键词: 脂肪肝病, 表观遗传学, 脂质代谢, 肝脏代谢, 核受体