Clear Sky Science · zh
精氨酸酶1通过以非典型方式调控ERK2/PPARγ信号促进肝脏脂质生成
为什么肝脏脂肪与日常健康相关
许多人腰腹部有多余脂肪,但很少有人意识到肝脏内隐性脂肪可以悄然推动糖尿病、心脏病,甚至肝癌的发展。本研究探讨了为何有些肝脏会堆积脂肪而另一些保持瘦性,并揭示了一个对已知肝脏酶—精氨酸酶1(Arg1)—出人意料的作用。通过展示Arg1如何帮助肝脏合成和储存脂肪,以及在小鼠中阻断一种特定蛋白相互作用如何逆转这一过程,研究指向了针对肥胖和脂肪肝病的新治疗思路。
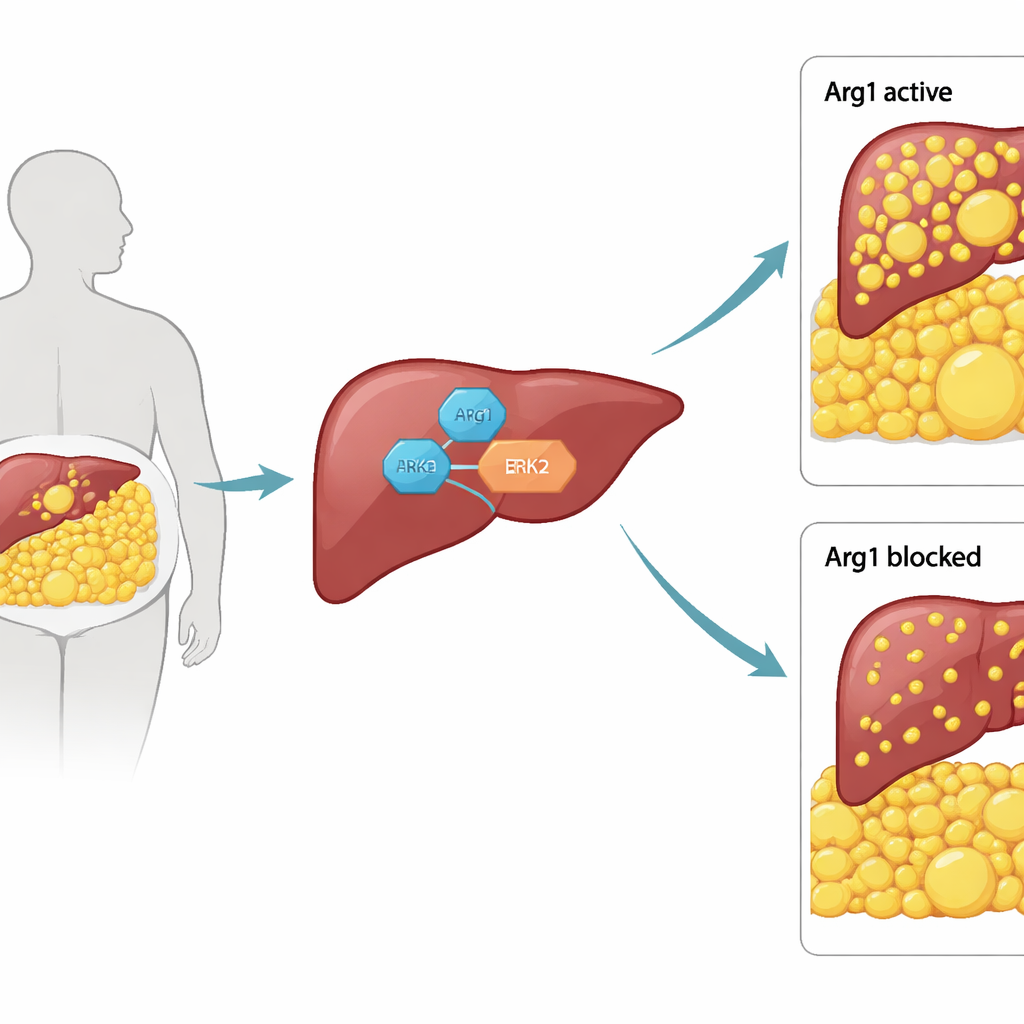
熟悉的肝酶承担的意外职责
Arg1以其在尿素循环中的核心作用而闻名——通过将氨基酸精氨酸转化为尿素帮助肝脏解毒氨。基于这一经典角色,大多数研究者假定Arg1仅支持基础代谢。作者则提出Arg1是否也会影响肝脏处理脂肪的方式。他们首先在小鼠中选择性地去除肝细胞中的Arg1。这些动物摄食正常,但体型更小、肝脏更轻,且肝脏和体脂储存的脂肪明显减少。血液和组织测量显示三酰甘油与游离脂肪酸降低,通常驱动脂质生成的基因,尤其受主调控因子PPARγ控制的那些基因,表达下调。
从酶的缺失到更好的代谢健康
为将Arg1的作用与完全丧失尿素循环功能引起的毒性效应区分开,研究团队构建了成人发病型的Arg1敲除模型,并且还使用了化学抑制剂阻断Arg1。在多种严重肥胖与脂肪肝的小鼠模型——遗传性肥胖、高脂饮食以及一种能快速损伤肝脏的特殊饮食——中,减少Arg1活性始终导致体重增加变少、脂垫变小,且肝脏内炎症和脂肪显著减少。这些益处并非由食物摄入或整体能量消耗的重大变化引起,提示Arg1直接影响肝脏合成和输出脂肪的过程,而不是简单地改变动物的食量或能量消耗。
蛋白伙伴关系如何引导脂质生成
深入分子机制,研究者发现Arg1以一种完全不同于预期的方式发挥作用。Arg1并非通过对精氨酸的常规化学反应起作用,而是物理性地与一种名为ERK2的信号蛋白结合,结合位点位于一个小的结构口袋内。该接触依赖于Arg1上一个可变的“S形”尾部,并干扰通常停靠在同一位点的其他蛋白。当Arg1存在时,它促进对ERK2的标记以便降解,从而降低ERK2水平。这一变化提升了两条主要通路,牵涉AKT、mTOR以及像Elk1和c-Fos这样的转录因子,最终增强PPARγ活性,推动肝细胞合成并储存更多脂肪。当Arg1被去除或被阻断时,ERK2积累并重新平衡这些通路,从而抑制PPARγ及脂质生成。
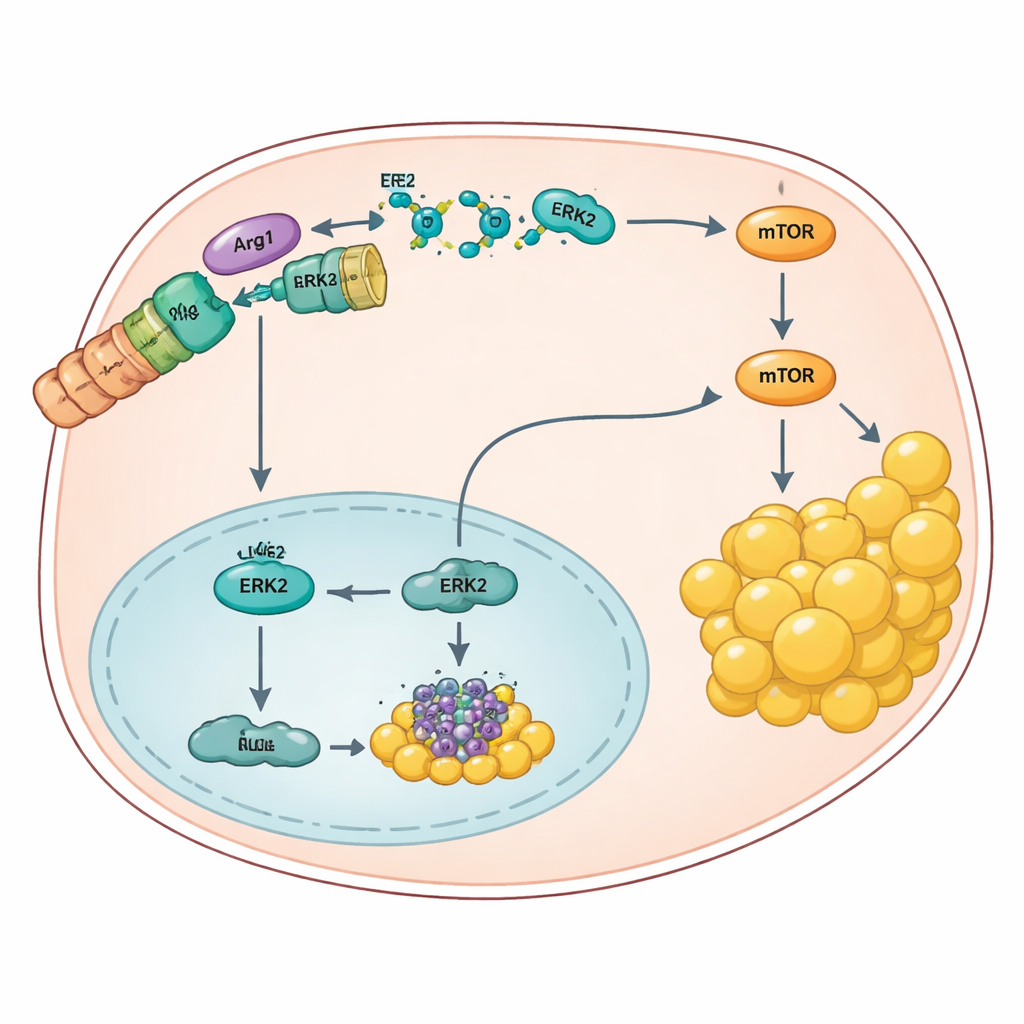
可解除有害联系的设计肽
基于该机制,团队设计了模仿ERK2结合口袋的短蛋白片段(肽)。这些肽能够进入肝细胞并与Arg1的S形结构结合,阻止Arg1抓住ERK2。在给予高脂或损伤性饮食的肥胖小鼠中,日常肽治疗保护ERK2免遭降解,降低指示肝损伤的酶水平,并显著减少肝脏及体脂储存的脂肪。重要的是,这一策略并未引发在完全丧失Arg1经典酶活时可能出现的精氨酸危险性累积,暗示可以在不干扰尿素循环核心功能的情况下,选择性地靶向Arg1与ERK2的物理相互作用。
这对未来疗法的意义
对非专业读者而言,结论是Arg1有两重身份:一方面参与氮的解毒,另一方面通过与ERK2的特定蛋白伙伴关系,悄然提升肝脏的脂肪生成。研究显示,仅破坏这一伙伴关系——而不完全关闭Arg1的核心功能——至少在雄性小鼠中可以缓解与肥胖相关的脂肪肝并改善代谢健康。尽管在将这种肽或类似药物在人类中测试之前仍需大量工作,这些发现揭示了一个位于肝脏化学和细胞信号交叉点上的精确新靶点,未来有望用于治疗肥胖和代谢性肝病。
引用: Shao, M., Cao, X., Chen, Y. et al. Arginase 1 promotes hepatic lipogenesis by regulating ERK2/PPARγ signaling in a non-canonical manner. Nat Commun 17, 2903 (2026). https://doi.org/10.1038/s41467-026-69731-3
关键词: 脂肪肝, 肥胖, 精氨酸酶1, 肝脏代谢, 信号通路