Clear Sky Science · zh
N-Myc MB0–MBI 区域与 Aurora 激酶 A 的 N 叶特异且动态地相互作用
这对癌症治疗为何重要
许多侵袭性儿科肿瘤依赖一种称为 N-Myc 的蛋白来维持肿瘤细胞增殖。N-Myc 本身很难用药物直接抑制,因为它更像一团柔软的意大利面而非刚性的锁让钥匙插入。本研究以前所未有的细节揭示了 N-Myc 如何抓握另一种蛋白——酶 Aurora 激酶 A(AurA),以增强其活性并帮助癌细胞存活。通过绘制这一伙伴关系的图谱,研究者们发现了用小分子打破它的可行路径。
柔性的麻烦制造者找到坚实的伙伴
N-Myc 属于 MYC 家族,这些是控制细胞生长、代谢和分裂的主开关。当它们过度表达时,会成为强大的致癌因素,尤其在神经系统肿瘤如儿童高危神经母细胞瘤中。与许多酶或受体不同,N-Myc 本身并不折叠成固定的三维构象;它是“先天无定形”蛋白,持续摆动并重塑。这样的柔性使其具有适应性,但也使之极难以通过药物靶向。相比之下,AurA 是结构良好的酶,参与组织细胞分裂。早期工作表明 AurA 有助于在肿瘤细胞中稳定 N-Myc,且两者存在物理相互作用,但接触点的确切性质和重要性尚不清楚。
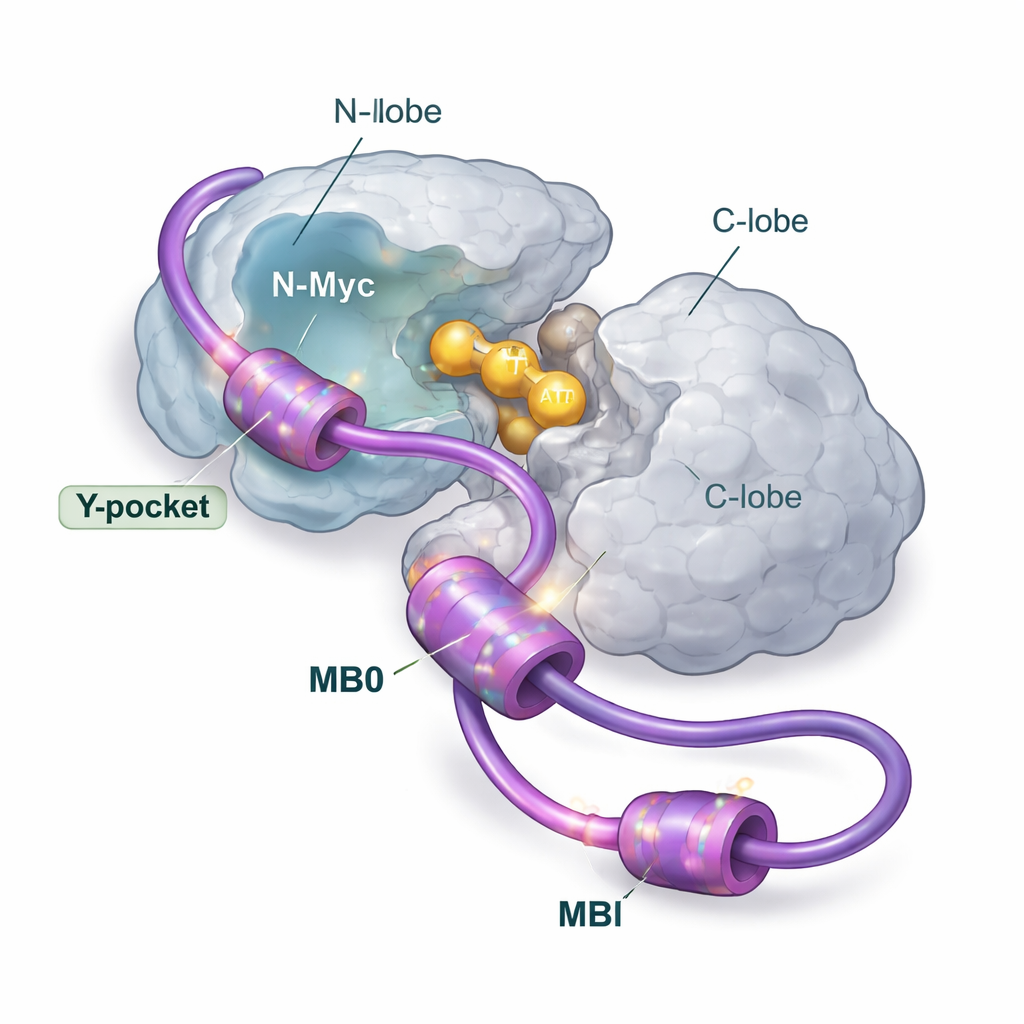
多处抓握点,但有一个主要着陆区
作者们使用包括核磁共振、X 射线散射、质谱、量热法和计算建模在内的广泛结构与生物物理学方法,剖析了 N-Myc 与 AurA 在溶液中如何结合。他们聚焦于 N-Myc 的前端,该处包含两个保守区段,称为 MB0 和 MBI。这些短片段富含芳香族残基(如苯丙氨酸、酪氨酸和色氨酸),倾向于与伙伴蛋白的疏水口袋相互作用。研究团队表明,N-Myc 主要以 1:1 的比例与 AurA 结合,MB0 和 MBI 起到主要接触区的作用。先前晶体结构中引起注意的另一个 N-Myc 片段在完整的 MB0–MBI 区域存在时,角色却相对次要。
一种将酶打开的动态握手
N-Myc 与 AurA 结合时并非僵硬地定格为单一构象,而是在结合态下仍然大体无定形。数据支持一种“模糊”复合体:数段 N-Myc 轮流接触 AurA N 叶的不同斑块,尤其是称为 Y 口袋的沟槽和连接信号至活性位点的邻近回环。尽管结合较为松散,但其效应明显——MB0 与 MBI 的结合稳定了 AurA 的 N 叶并提高了其激酶活性,意味着它更有效地向底物转移磷酸基。当研究者系统性地将 MB0 和 MBI 中的关键芳香残基替换为丙氨酸时,N-Myc–AurA 复合体变弱、酶的稳定性降低、活性下降。这表明在本质上柔软的 N-Myc 链中,特定的芳香“锚点”对于激活 AurA 至关重要。
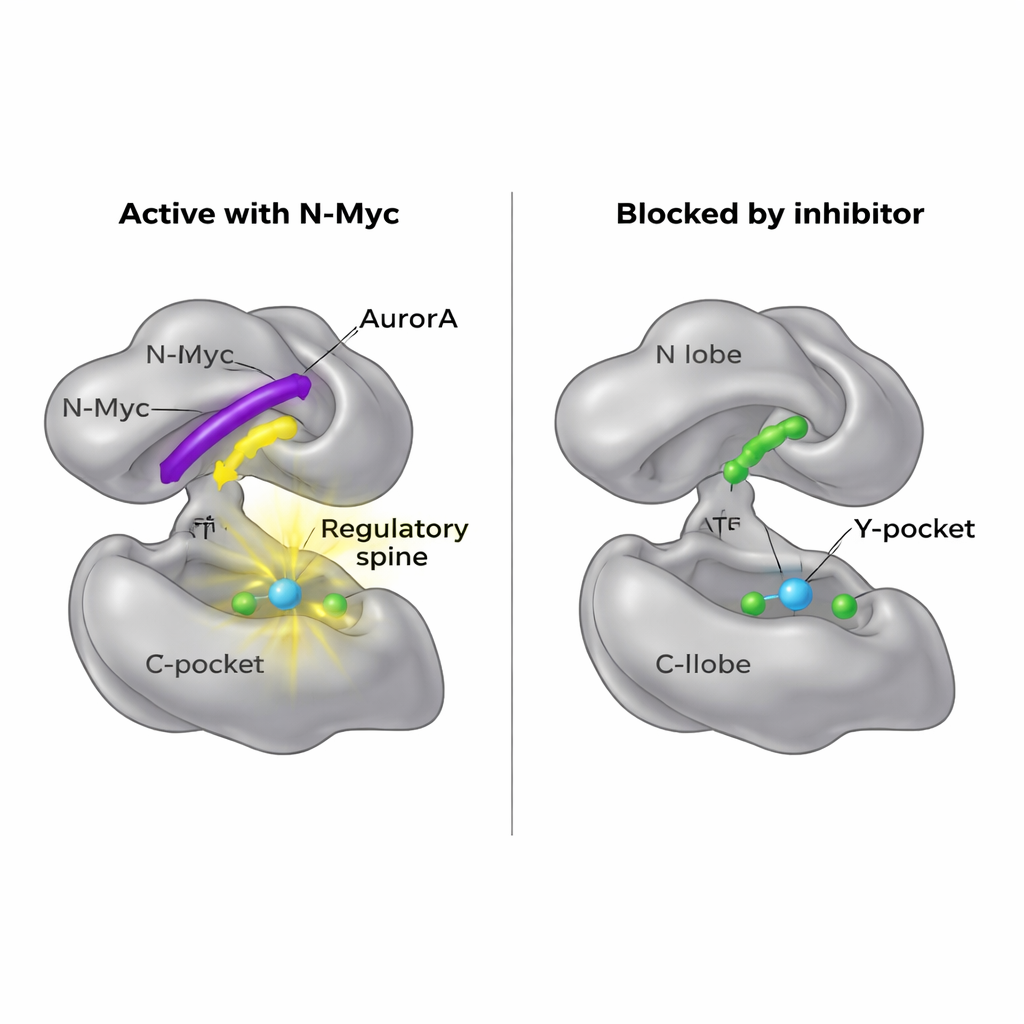
打开一个新的药物入口
由于直接针对 N-Myc 难度大,研究者转而询问是否可以阻断其在 AurA 上的停靠位点。他们的结构图谱显示,MB0 与 MBI 占据了 N 叶的同一区域,这一区域也是另一种伙伴蛋白 TPX2 激活 AurA 时使用的。已有一种名为 AurkinA 的小分子被证实可楔入 Y 口袋并驱逐 TPX2。在结合实验中,AurkinA 同样有效地与 N-Myc 在 AurA N 叶上竞争,阻止了 N-Myc1–69 和 N-Myc1–100 片段的附着。该结果表明 N 叶表面,特别是 Y 口袋,是一个可成药的热点,不仅控制经典调节子如 TPX2,也控制像 N-Myc 这样的无定形致癌蛋白。
这对未来治疗的意义
这项工作将 N-Myc–AurA 的伙伴关系重新描绘为以 AurA N 叶为中心的动态、多点接触的拥抱,而非单一的刚性结合位点。对于非专业读者,关键信息是:即便是形状不定的癌蛋白如 N-Myc,也可以通过间接靶向其伙伴酶上的坚实停靠补丁来应对。研究表明,已有的结合 N 叶的小分子能够将 N-Myc 推离 AurA,这为有选择性破坏该相互作用的药物开辟了明确路径。此类药物可以削弱 N-Myc 在高危儿童肿瘤中的关键支持作用,并在进一步开发下,为长期被认为“不可成药”的癌症提供新的治疗途径。
引用: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
关键词: N-Myc, Aurora 激酶 A, 先天无定形蛋白, 神经母细胞瘤, 蛋白质–蛋白质相互作用抑制剂