Clear Sky Science · zh
一个空间分辨的人类胶质母细胞瘤图谱揭示了解剖学生态位的不同细胞与分子模式
为什么这份脑癌地图很重要
胶质母细胞瘤是最致命的脑癌之一,部分原因在于每个肿瘤都是不同细胞类型和微环境的拼贴。常规影像与实验室检测通常只把肿瘤视为一个整体团块。本研究构建了一个高分辨率的“图谱”,显示人类胶质母细胞瘤中每种主要细胞类型的空间分布,它们如何聚集成不同的“社区”,以及其中某些社区如何可能促使肿瘤再生并缩短患者生存期。
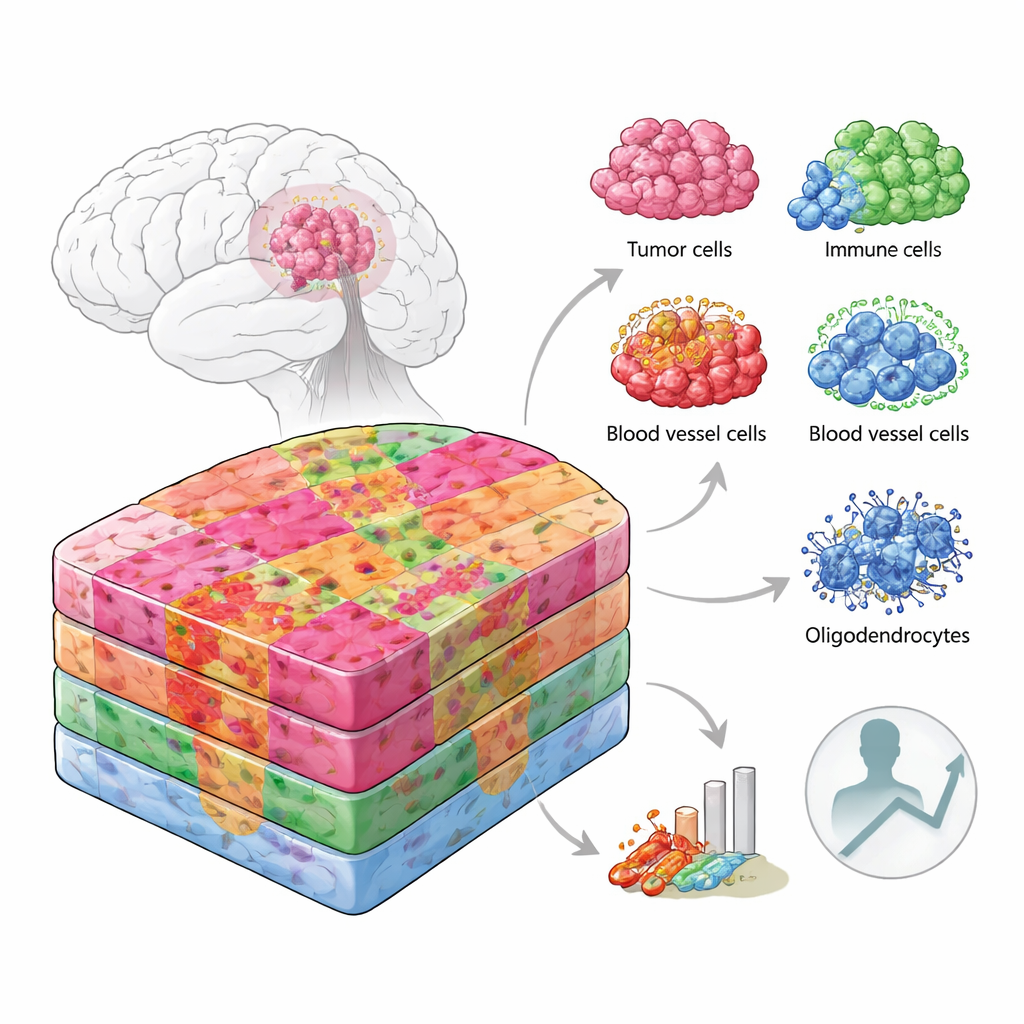
把肿瘤当作城市地图来观察
研究者没有把肿瘤切片视为均质体,而是像看城市地图那样,每个区域有自己的布局和居民。他们结合了数种前沿技术,从肿瘤组织上成千上万个微小点读取基因活动,并将这些信息与单细胞数据和蛋白质测量相匹配。重要的是,他们不仅在手术室获取的新鲜冷冻样本上开展研究,也在常规存档的石蜡包埋医院组织上进行分析——这正是大多数病理实验室保存的样本类型。总体上,他们分析了超过10万多个带有空间条码的区域和22万多个个体细胞,样本来自不同年龄和遗传背景的患者,覆盖了致密的肿瘤核心及其更弥散的边缘。
胶质母细胞瘤内的隐匿社区
通过将基因活动叠加在高倍显微图像上,团队把每个肿瘤划分为解剖学“生态位”,例如癌细胞侵入正常脑组织的前沿、拥挤的中心区、富含血管的区域以及围绕坏死或缺氧组织的地带。每个生态位都有其独特的细胞组合。灰质中的肿瘤边缘富含神经元和典型的支持细胞,而白质边缘则包含大量少突胶质细胞——这些细胞通常负责神经纤维的髓鞘包裹。某些血管相关生态位充斥着专门的血管细胞和支持细胞,而另一些则以免疫细胞和瘢痕样组织为主。靠近坏死组织的缺氧带主要由侵袭性、类间充质的肿瘤细胞和巨噬细胞占据,细胞多样性明显降低。
支持细胞的意外角色
最引人注目的发现之一涉及少突胶质细胞,这类细胞通常被认为是脑中相对“静默”的绝缘细胞。图谱揭示了四种不同的少突胶质细胞状态,其中包括一种先前未被充分重视的类型,几乎仅出现在胶质母细胞瘤的核心区域。这些细胞丢失了许多与髓鞘相关的基因,反而激活了与炎症和应激相关的基因,类似于多发性硬化等脑疾患中观察到的疾病相关少突胶质细胞。从空间分布上看,这类免疫样少突胶质细胞聚集在一个“免疫-胶质生态位”,与活化的小胶质细胞、巨噬细胞、异常的血管细胞和类间充质肿瘤细胞并存,但显著地不出现在最缺氧的区域。
将显微模式与患者结局联系起来
作者随后检验了定义这些少突胶质细胞状态的基因程序是否出现在与患者记录相关联的大型肿瘤样本集中。在两个独立的胶质瘤队列中,代表常规、生成髓鞘的少突胶质细胞的特征与更好生存相关,即使在调整了年龄和关键遗传风险标志后仍然显著。相反,免疫激活型少突胶质细胞的基因特征则与较差生存相关,并在侵袭性、耐治疗的肿瘤中更为显著,尤其是那些治疗后复发且缺乏常见的与DNA修复相关的甲基化改变的肿瘤。这提示少突胶质细胞在肿瘤内的重编程方式及其相对于肿瘤和免疫细胞的位置,可能会影响疾病对治疗的反应以及复发的可能性。
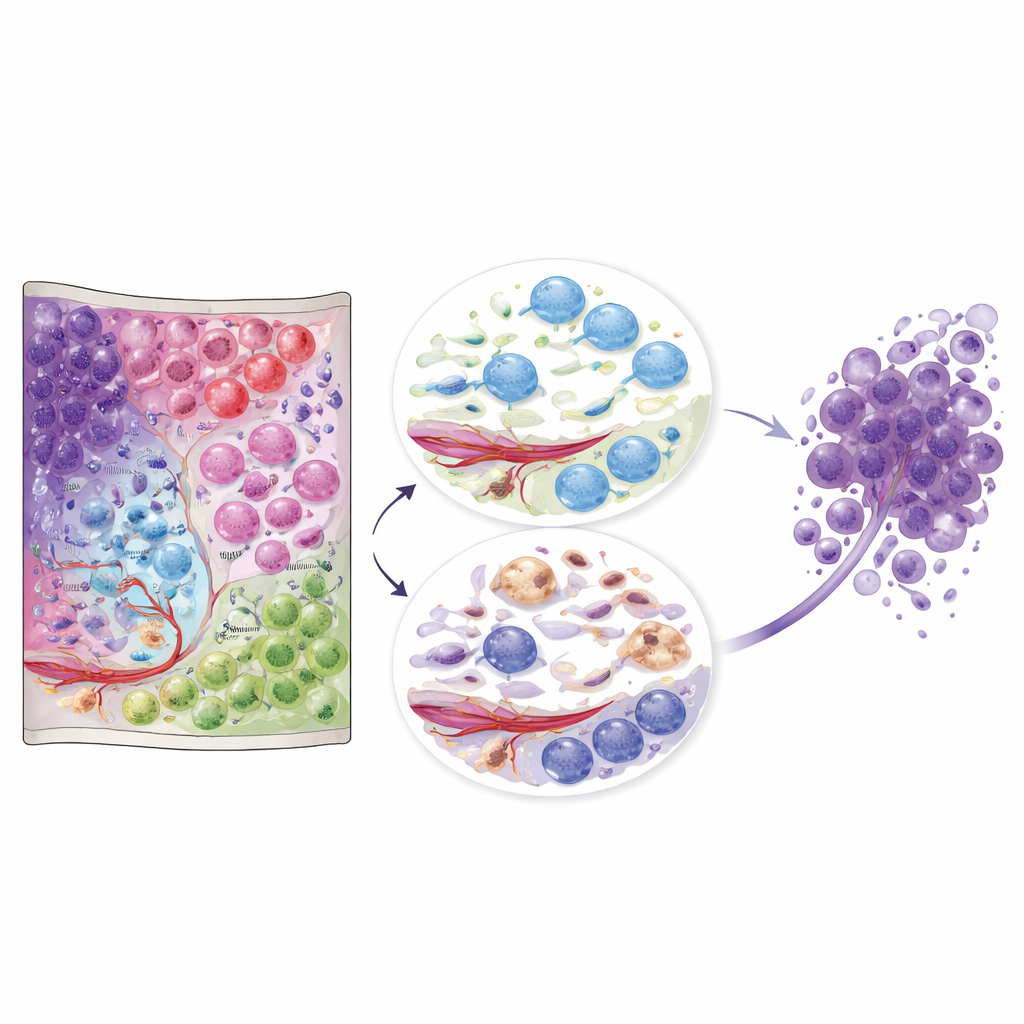
这份图谱对未来诊疗的意义
这些数据把胶质母细胞瘤从一个模糊的团块转变为一个细胞群体相互作用的详细景观。对非专业读者来说,关键信息是位置和邻里关系很重要:相同的大类细胞根据所处的生态位表现出截然不同的行为。公开可用的图谱为其他研究者和临床医生提供了一个参考,可以将其自己的样本置于这一空间语境中。长期来看,治疗策略可能不仅仅是消灭肿瘤细胞,而是针对破坏有害生态位——例如免疫-瘢痕区域或免疫激活的少突胶质细胞聚集区——这些区域似乎有助于肿瘤生存和复发。
引用: Sonpatki, P., Park, H.J., Xing, Y.L. et al. A spatially resolved human glioblastoma atlas reveals distinct cellular and molecular patterns of anatomical niches. Nat Commun 17, 2951 (2026). https://doi.org/10.1038/s41467-026-69716-2
关键词: 胶质母细胞瘤, 空间转录组学, 肿瘤微环境, 少突胶质细胞, 脑癌图谱