Clear Sky Science · zh
空间 Perturb-seq:在完整组织结构中进行单细胞功能基因组学
在活体脑回路中观察基因如何发挥作用
从阿尔茨海默病到帕金森病,许多脑疾病都与危险基因有关,但我们对这些基因如何影响活体大脑中单个细胞仍知之甚少。本研究提出了一种强有力的方法,用以在细胞仍处于其自然邻里环境中的情况下,观察特定基因被关闭后单个细胞发生的变化。该方法称为 Spatial Perturb-Seq,能够将遗传风险与完整大脑中被扰乱的细胞行为和细胞间通信联系起来。
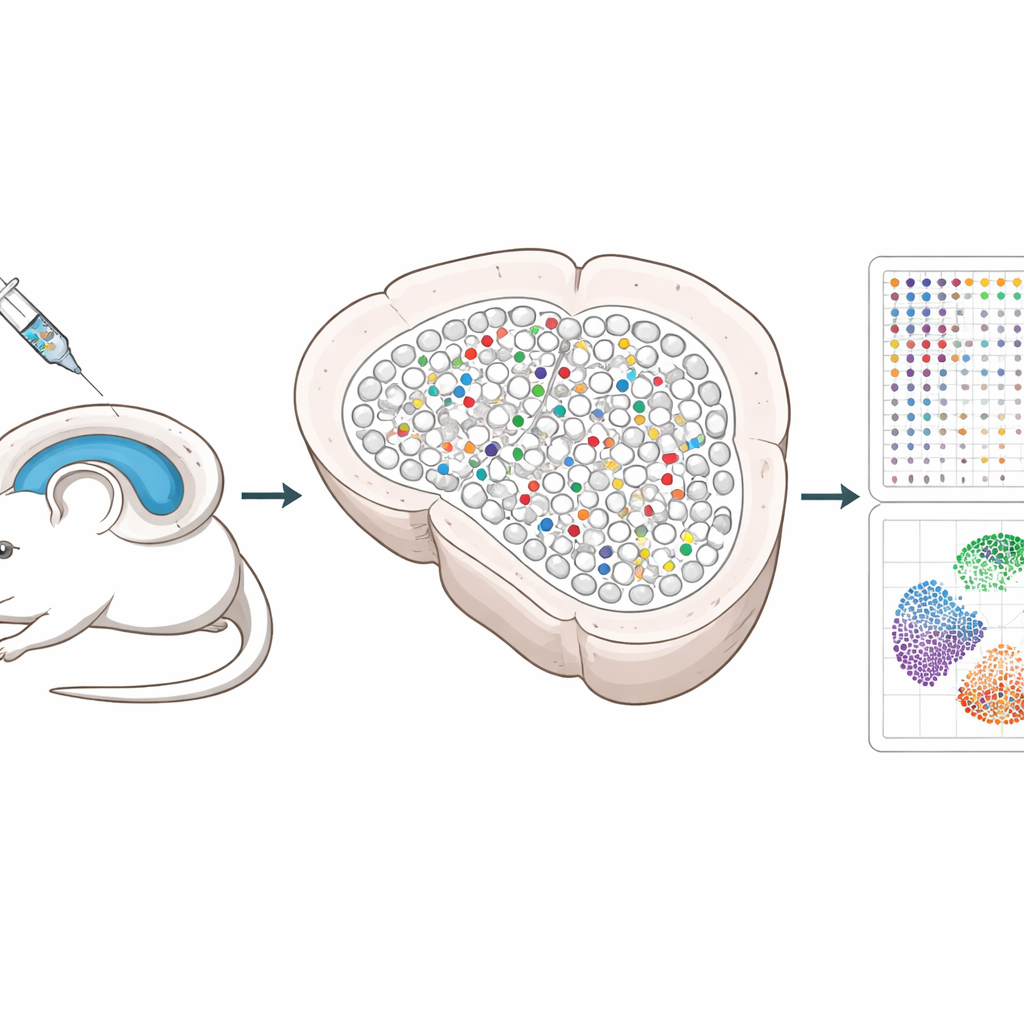
一次测试许多基因的新方法
研究人员构建了一个系统,使用由无害病毒递送到海马体(一处与记忆相关的大脑区域)的 CRISPR 基因编辑工具。每个病毒携带三个用以使特定基因失活的导向序列,以及独特的 DNA “条形码”和荧光标记,以便日后定位被编辑的细胞。通过将这些病毒混合并以低剂量注入,只有少数散布的细胞被编辑,大多数邻近细胞保持未受影响。这种稀疏的分布使科学家能够将编辑细胞内部发生的变化与周围健康细胞中发生的变化区分开来。
保持大脑地图的完整性
传统的单细胞方法需要将组织解离,这会破坏细胞的精确位置,甚至导致脆弱神经元的丢失。Spatial Perturb-Seq 则直接从薄切的大脑切片读取基因活动,从而保留每个细胞的位置。利用称为 Stereo-seq 的技术,团队获取了超过 20 万个细胞的完整基因表达谱,同时读取了 CRISPR 条形码并记录了每个细胞在组织中的坐标。随后他们使用先进的基于图像的算法勾勒出每个细胞,并用计算工具识别细胞类型和局部邻域,特别关注海马神经元及其紧密接触的细胞。
被编辑细胞如何影响其邻居
在掌握组织地图后,科学家将被编辑的神经元与未编辑的神经元进行比较,并分别将其与每个被编辑细胞周围的未编辑邻居进行对比。这使他们能够区分“细胞自主性”效应(发生在被编辑细胞内部)和“非细胞自主性”效应(发生在周围微环境中)。敲除 18 个不同基因中的许多与神经退行性疾病风险相关,产生了被编辑神经元内部不同的基因变化模式。有些编辑,例如针对基因 Cfap410 的编辑,还在邻近细胞中触发了强烈的基因活动变化,反映出局部信号传导和支持功能的改变。
关于神经退行性疾病通路的线索
若干基因提供了尤为有趣的见解。失活 Lrrk2(帕金森病的主要风险基因)在被编辑的神经元中引起了显著变化,包括降低了 Bc1 的水平——一种在突触处调节蛋白质合成的重要 RNA 分子。与此同时,邻近细胞显示出与突触结构、蛋白质运输和钙处理相关基因表达的变化,暗示与 Lrrk2 相关的问题会在局部回路中扩散。敲除另一个基因 Srf 则扰动了与神经元生长和可塑性相关的基因网络,并削弱了神经元之间特定的配体–受体信号通路,表明细胞间通信受损。通过系统地评估这些信号对,团队能够确定每个基因最受影响的通信路线。
用于描绘遗传效应的灵活工具
为证明 Spatial Perturb-Seq 并非仅限于单一平台,研究人员还将其适配到一种基于成像的系统 Xenium。在该方法中,预设计的探针面板和定制条形码探针可以在组织中直接读出所选基因和条形码。尽管这种目标化方法覆盖的基因比全转录组的 Stereo-seq 少,但对于关键编辑(例如 Lrrk2 和 Srf)的基因变化模式在两种方法之间以及与大型外部大脑图谱之间高度一致。这样的交叉验证支持了所观察到的基因和邻域效应的稳健性。
这对脑健康研究意味着什么
简单来说,Spatial Perturb-Seq 让科学家能够在单个脑细胞中关闭许多不同的基因,然后在组织连线图保持完整的情况下观察这些细胞及其直接邻居的反应。这样可以追踪遗传风险如何影响的不仅是单个细胞,还有它们之间的对话,而这些对话对大脑健康至关重要。随着测序成本降低和更大规模实验的开展,这种方法有望帮助揭示在阿尔茨海默病、帕金森病和 ALS 等疾病早期阶段最关键的基因和局部回路,从而为更精确的治疗策略提供指导。
引用: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
关键词: 空间基因组学, CRISPR 筛选, 单细胞测序, 神经退行性疾病, 细胞间通讯