Clear Sky Science · zh
外显子包含特征可实现剪接因子活性准确估计
解读细胞的隐藏编辑印记
我们体内的每个细胞在把 RNA 信息翻译成蛋白之前,都会不断地编辑这些信息。这种被称为剪接的编辑过程,决定了细胞是保持健康还是转向癌变。本文所基于的研究表明,通过仔细观察哪些 RNA 片段被保留或跳过——即外显子包含特征——科学家能够准确推断控制剪接的分子“编辑者”的活性,即便是在像癌症这样复杂的疾病中。
细胞如何剪切并粘贴它们的信息
基因并不是以一段连续的序列被读取的。相反,细胞会移除非编码片段并将编码片段(称为外显子)缝合在一起,构建最终的 RNA 信息。被称为剪接因子的特化蛋白引导这一剪切与粘贴的过程,决定哪些外显子被包含。它们的行为受到多层调控的影响:自身 RNA 和蛋白的产量、化学修饰、在细胞内的位置以及与其他蛋白的相互作用。由于有许多操控杆可以改变剪接因子的行为,仅测量一种类型的数据——例如基因表达——往往无法揭示这些因子真实的功能状态。
将外显子模式转化为活性读数
受早期转录因子研究的启发,作者提出了不同的策略:与其直接测量剪接因子,不如从它们的影响中读取其活性。当剪接因子发生变化时,其靶外显子的包含率会以可识别的模式发生移动。团队汇编了数百个针对单个剪接因子进行敲低、敲除或过表达的实验,并利用这些数据构建了将每个因子与其明显影响的外显子相连的“经验网络”。随后他们调整并采用了一种名为 VIPER 的计算框架,从新的外显子包含特征中读取并评分,推断出为解释观察到的模式每个剪接因子必须具有的活性水平。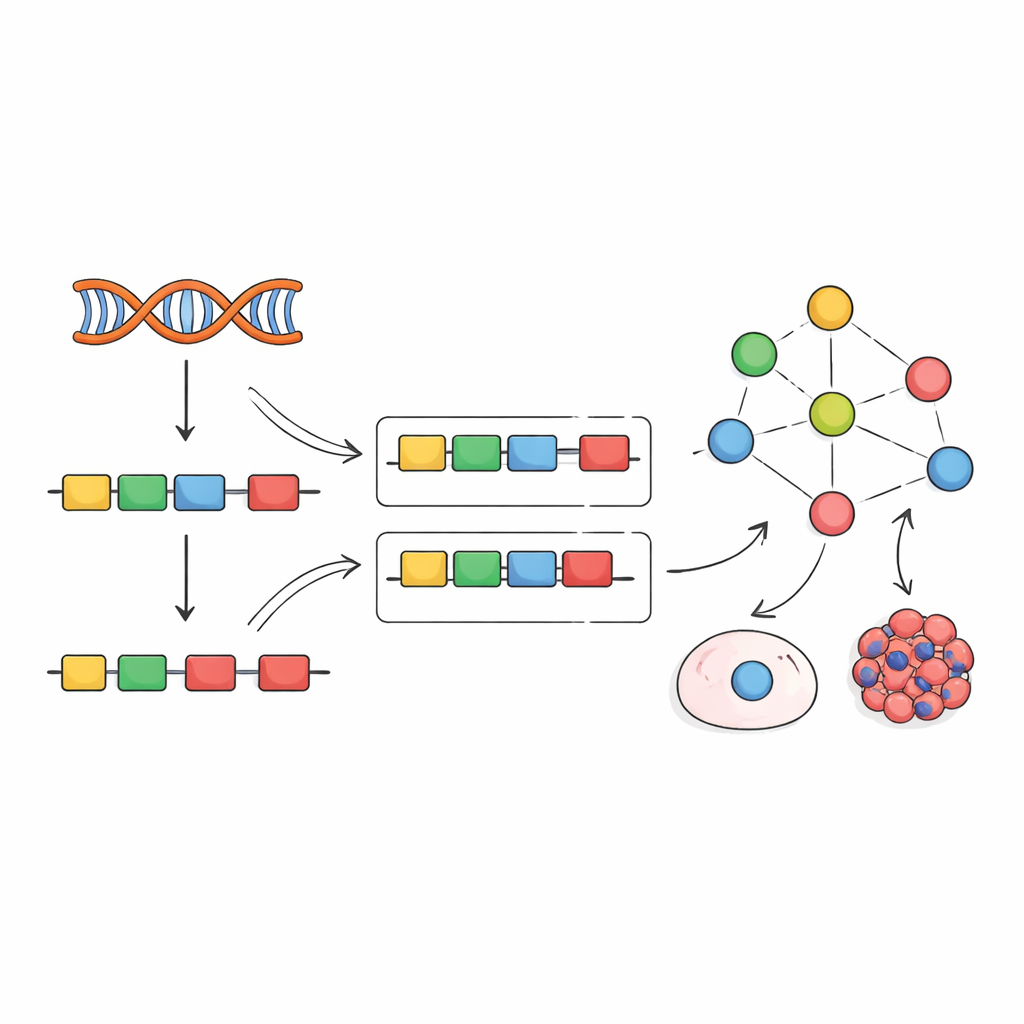
在真实扰动中测试该方法
为验证这一方法的有效性,研究者对多种构建网络和计算活性评分的方法进行了基准测试。直接来自扰动实验的经验网络,结合 VIPER 的富集分析,明显优于仅基于统计推断的替代方法。该方法在大多数测试中能够正确识别实验上被扰动的剪接因子,即便跨越不同细胞类型和研究。它还捕捉到了更细微的调控机制。例如,一种名为 Indisulam 的抗癌药物会触发剪接因子 RBM39 蛋白的降解,同时其 RNA 水平上升,似乎是补偿性反应。传统的表达分析会误导性地显示 RBM39 活性增加,但基于外显子的活性评分正确揭示了明显的功能丧失,与已知的药物作用一致。
在癌症中发现隐藏的剪接程序
借助这一工具,作者转向癌症基因组图谱(The Cancer Genome Atlas),分析了多种肿瘤类型及其对应健康组织的外显子层面数据。他们发现了两类广泛且反复出现的剪接程序。一类程序由在肿瘤中倾向于更活跃的剪接因子组成,并与较差的患者生存率相关——类似致癌程序;另一类则由在肿瘤中系统性活性降低且与更好预后相关的因子构成,类似肿瘤抑制程序。这些程序影响参与癌症基本特征的基因,例如快速细胞分裂和肿瘤逃避免疫监视的能力。例如,某些由类肿瘤抑制程序调控的外显子似乎影响患者对免疫检查点疗法的响应,指向潜在的新型生物标志物或干预点。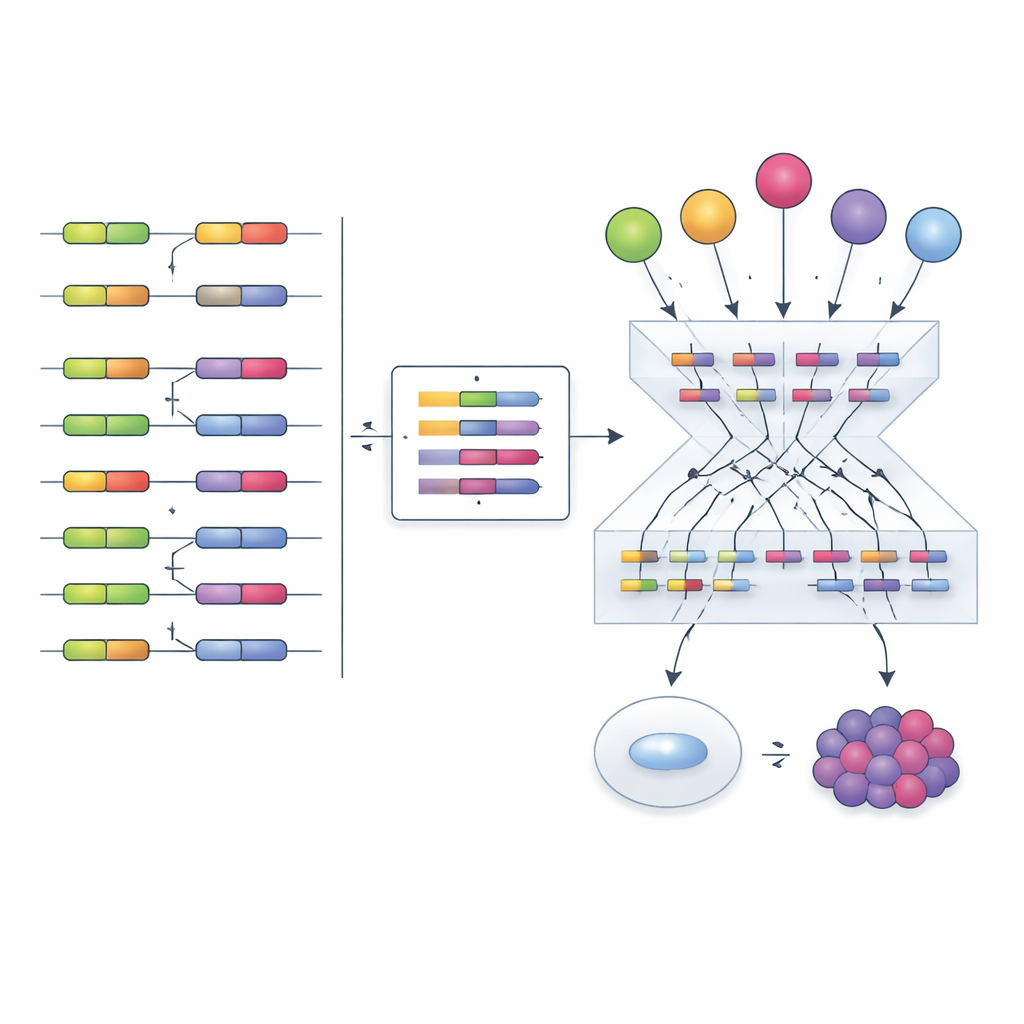
沿着通往癌变的道路追踪剪接变化
团队还研究了一个从正常细胞到永生化、成瘤、最终转移状态的人类细胞逐步模型。他们发现,随着细胞获得驱动癌变的突变,类致癌的剪接程序活性增强,而类肿瘤抑制的程序则逐渐减弱。通过整合多层数据——RNA 水平、蛋白丰度、化学修饰以及剪接因子自身的剪接变化——他们识别出一组集中的候选分子事件,可能驱动这些程序的转变,为未来的实验验证提供了优先级清单。
这对患者和未来研究的重要性
归根结底,这项研究表明,剪接因子复杂的行为可以被浓缩为一个可解释的活性评分,该评分来源于外显子被包含或跳过的模式。这使得使用标准 RNA 测序数据在大规模患者队列和多样化实验中研究剪接调控成为可能,而无需昂贵的多组学检测。对普通读者而言,核心信息是:基因如何被剪切和粘贴的模式蕴含着关于细胞隐藏控制系统的丰富信息,解码这些模式能够揭示新的癌症驱动因子、改进预后评估,并指导更精确治疗的探索。
引用: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
关键词: RNA 剪接, 剪接因子, 癌症基因组学, 转录组学, 蛋白活性推断