Clear Sky Science · zh
LOAd703 诱导肿瘤微环境基因工程联合阿特珠单抗治疗转移性恶性黑色素瘤:I/II期临床试验
这项新的黑色素瘤研究为何重要
对于那些对当前强效免疫治疗不再产生反应的晚期皮肤黑色素瘤患者,可选的治疗方案有限且常有较大毒性。本研究检验了另一种思路:将基因改造的病毒直接注入肿瘤,联合现有的免疫增强药物,以唤醒机体防御并重新控制癌症。早期结果表明,这种方法可安全给药,并可能帮助一部分先前对标准治疗耐药的患者获得临床获益。
一种能在治疗中占上风的顽固皮肤癌
黑色素瘤是西方国家中常见且严重的皮肤癌之一,发病率在近几十年明显上升。现代免疫检查点抑制剂——通过解除T细胞抑制来发挥作用——已经改变了预后,使晚期黑色素瘤的五年生存率提高到大约一半。然而,许多肿瘤最终会失去反应性。通常,这些耐药癌周围存在一个“冷”性的微环境,阻止免疫细胞进入或使其失活。寻找能重塑肿瘤微环境的方法,使T细胞重新识别并攻击癌细胞,是当前的重要研究方向。
一种旨在重塑肿瘤“邻里”的病毒
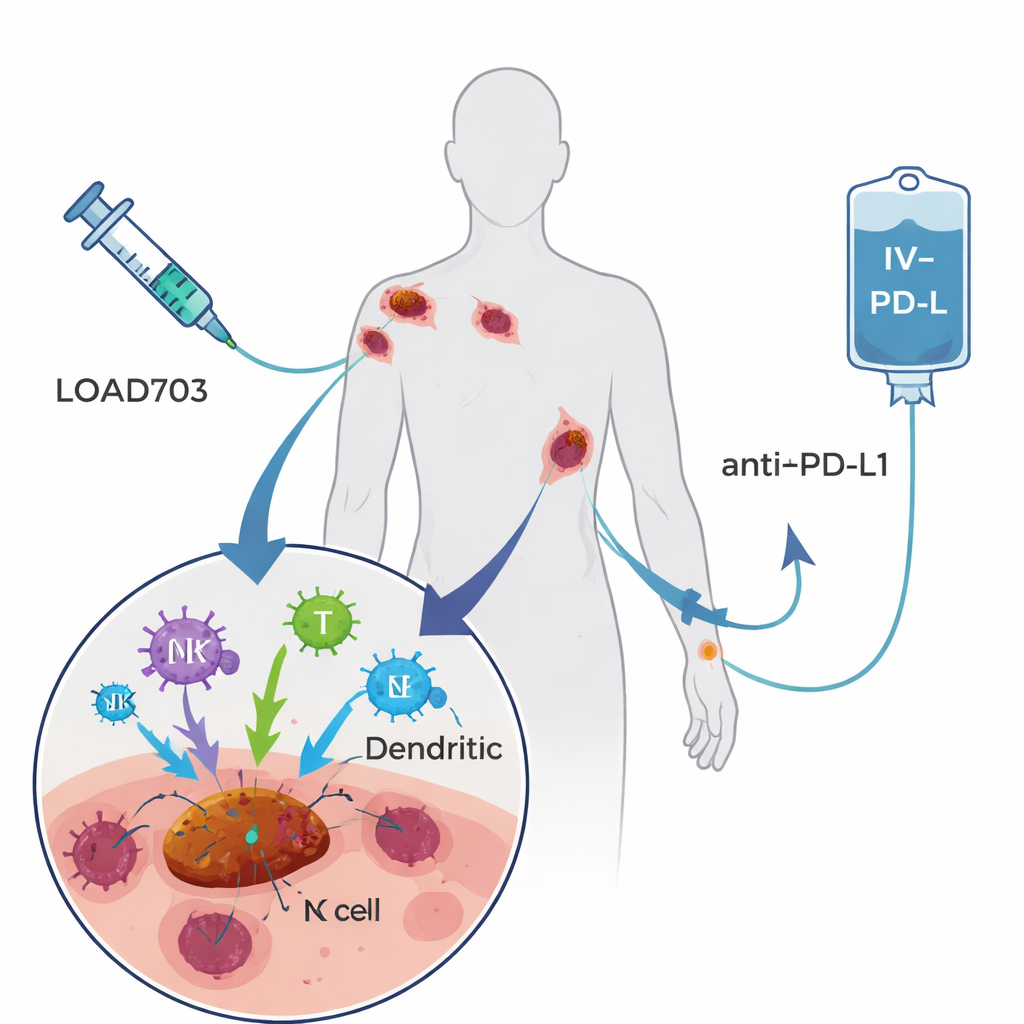
本研究测试的治疗方案称为 LOAd703,是一种经改造的腺病毒——一种常见感冒病毒类型——被设计来完成两项任务。首先,它优先在肿瘤细胞内复制并摧毁这些细胞,这是一种称为溶瘤病毒疗法的策略。其次,它携带编码两个强效免疫刺激信号的基因,置于被感染的细胞表面。这些信号,CD40L 和 4-1BBL,有助于专业免疫哨兵(树突状细胞)成熟并呈递肿瘤片段,同时增强并扩增抗癌的T细胞和自然杀伤细胞。受试者每三周在一个或多个肿瘤中直接注射 LOAd703,同时静脉给予已批准的抗体药物阿特珠单抗(atezolizumab),该药物阻断T细胞的 PD-L1 抑制通路。研究者希望病毒能将肿瘤转变为体内的“疫苗工厂”,而抗体则保持被再激活的T细胞持续活跃。
谁接受了治疗及其疗效如何
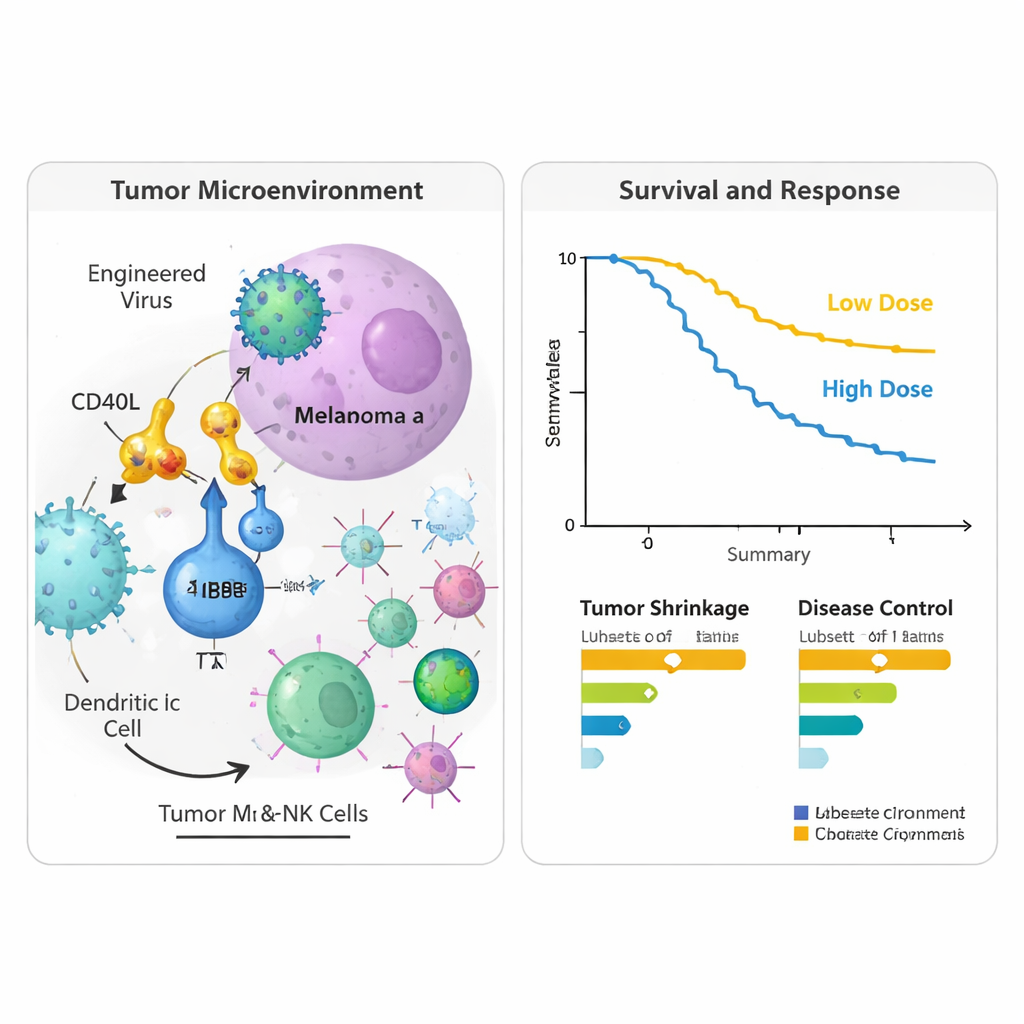
这项 I/II 期试验入组了24名 IV 期黑色素瘤患者,这些患者在至少接受过一次 PD‑1 抑制治疗后病情明确进展;其中许多人此前已接受多线免疫治疗和靶向药物。研究考察了两种病毒剂量水平。总体而言,该联合方案耐受性良好。与病毒相关的最常见不良反应——发热、寒战、恶心和类流感症状——大多为轻度且短暂。只有两名患者在较高剂量下出现较严重但可逆的反应,且无人因病毒相关问题被迫停药。肿瘤反应方面,四名患者(17%)出现可测量的肿瘤缩小,超过一半的患者在一段时间内至少表现为疾病稳定。入组两年后,近一半受试者仍然存活,其中包括一些在完成治疗后扫描显示长期受控或可检测病灶完全清除的患者。
免疫系统被重新激活的迹象
为了解肿瘤内及血液中的变化,研究团队分析了治疗前和开始治疗约九周后的组织活检和血液样本。在被注射的肿瘤中,他们观察到与1型免疫反应相关基因的活性提高,包括活化的T细胞和自然杀伤细胞的标志,以及有助于这些细胞从邻近血管进入肿瘤的分子。与抗原呈递相关的信号——即将肿瘤片段展示给T细胞的过程——也有所增加,这提示病毒疗法正在将肿瘤微环境从抑制性转向更有利于免疫的状态。在血液中,多种免疫相关蛋白(包括 PD‑L1 本身)在治疗后升高,与免疫通路的广泛激活一致。生存时间较长的患者往往显示出与强健T细胞功能和抗病毒保护相关的基因模式,而生存时间较短的患者则表现出与抑制性细胞类型和组织重塑信号相关的模式。
这对未来治疗可能意味着什么
这是一项样本量小且无对照组的单臂研究,因此其生存和应答数据需谨慎解读。尽管如此,良好的耐受性、肿瘤内的免疫激活以及在多线治疗失败患者中令人鼓舞的疾病控制提示,像 LOAd703 这样的基因工程溶瘤病毒或许能帮助黑色素瘤重新获得对检查点阻断的敏感性——甚至单独维持对肿瘤的控制。结果支持开展更大、受控的试验,可能将病毒与额外的免疫靶向药物联合,以明确哪些患者最可能受益以及如何将这一策略最佳整合进黑色素瘤的治疗体系。
引用: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
关键词: 黑色素瘤, 免疫治疗, 溶瘤病毒, 肿瘤微环境, 检查点抑制剂耐药