Clear Sky Science · zh
药物笼控策略实现光催化双重脱笼释放一氧化氮与麻醉药以用于抗菌镇痛
同时对抗细菌与疼痛
细菌感染不仅危及健康,还会带来剧烈疼痛。常规疗法通常只针对病原体,而需要患者额外依赖止痛药,这些药物可能持续时间短或产生副作用。本研究介绍了一种受光控制的药物,旨在通过一步协同释放既杀菌又止痛,为更智能、更舒适的感染护理提供了可能。
二合一药物的构想
研究人员以常用的局麻药四卡因为基础,通过化学方法将一氧化氮(一种以强抗菌和抗炎作用著称的小气体分子)连接到四卡因上,构建出一种“前药”TTC-NO,该分子在未触发时基本无活性。随后他们将TTC-NO与一种光敏助剂一同封装进可在水相环境(如血液或组织液)中运载的聚合物胶束微囊中。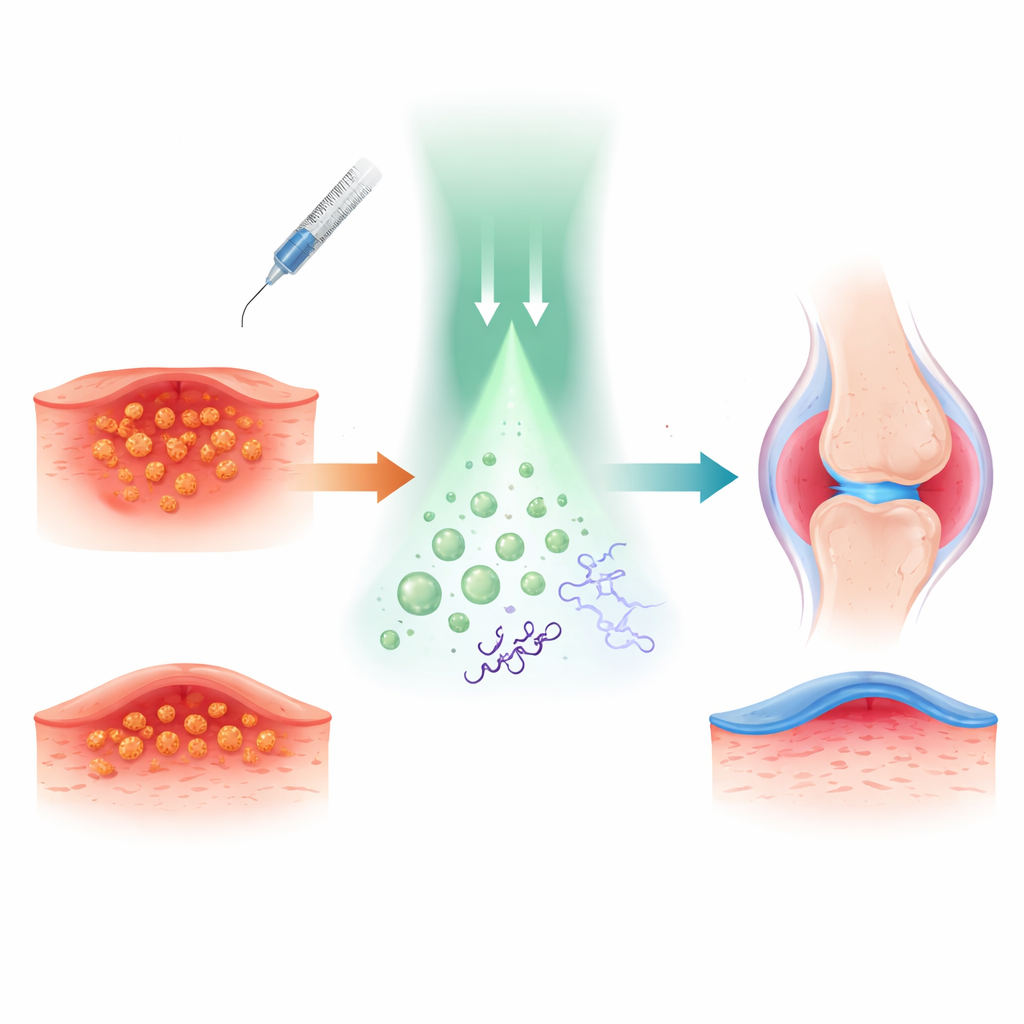
用温和光照开启药效
为理解该光控开关的机理,团队在溶液中研究了相关化学过程。他们证明了一种基于铱的光催化剂在绿光照射下能够向TTC-NO传递电子,削弱特定键并促使一氧化氮释出,同时使四卡因恢复为其活性形式。通过光谱学和色谱法测得,在这些条件下TTC-NO几乎完全转化为四卡因和一氧化氮,而在黑暗中则基本保持不变。将两种成分封装到胶束后,粒子仍然稳定,直径约80纳米,且仅在照射时释放载药物质,这证明了“药物笼控药物”概念可由体外光照精确控制。
促进感染性伤口更快愈合
随后团队在小鼠皮肤伤口的MRSA(耐甲氧西林金黄色葡萄球菌)感染模型上进行了测试。一些伤口使用常规处理如抗生素或生长因子,另一些则给予TTC-NO胶束并有或无光照处理。当开启光照时,TTC-NO体系显著降低细菌数量、减轻炎症、促进新生血管生成并增加胶原沉积,这些因素对伤口修复至关重要。这样处理的伤口愈合更快、更完整,优于仅用四卡因或在暗处保留的胶束,其疗效可与一线抗生素相媲美。重要的是,安全性检查未见主要器官损伤或血液化学异常。
缓解疼痛并抑制神经信号
由于感染和组织损伤会强烈激活疼痛通路,科学家在相同伤口模型中仔细测量了与疼痛相关的行为。传统四卡因短时间内提高触发疼痛反应所需的力,但数小时内失效。相比之下,经光激活的TTC-NO胶束可提供长达12小时的镇痛效果。对脊髓附近神经丛的显微观察以及对大脑感觉皮层的电活动记录显示,联合治疗在纯四卡因失效很久之后仍能抑制感痛神经元的放电。进一步试验表明,这种持续时长的延长不仅来自对神经的麻醉作用,还得益于一氧化氮通过降低细菌负荷与炎症所带来的附加效果。
保护感染并伴有剧痛的关节
研究者还在患有化脓性关节炎的小鼠中测试了该体系,这是一种发生在膝关节内的严重MRSA感染,会导致肿胀、骨质流失与剧烈疼痛。光激活的TTC-NO胶束减小了关节肿胀、降低了细菌数量并通过高分辨率扫描保护了骨结构。血液中有害炎症分子水平下降,而有利的信号分子上升。在行为学上,经治疗的小鼠对受累足爪能耐受更大的机械压力,并在开放场中活动更自由,显示出比单独四卡因更持久的缓解。神经与大脑测量结果与这些行为学收益一致,表明疼痛通路被广泛抑制且未见明显的局部或系统毒性。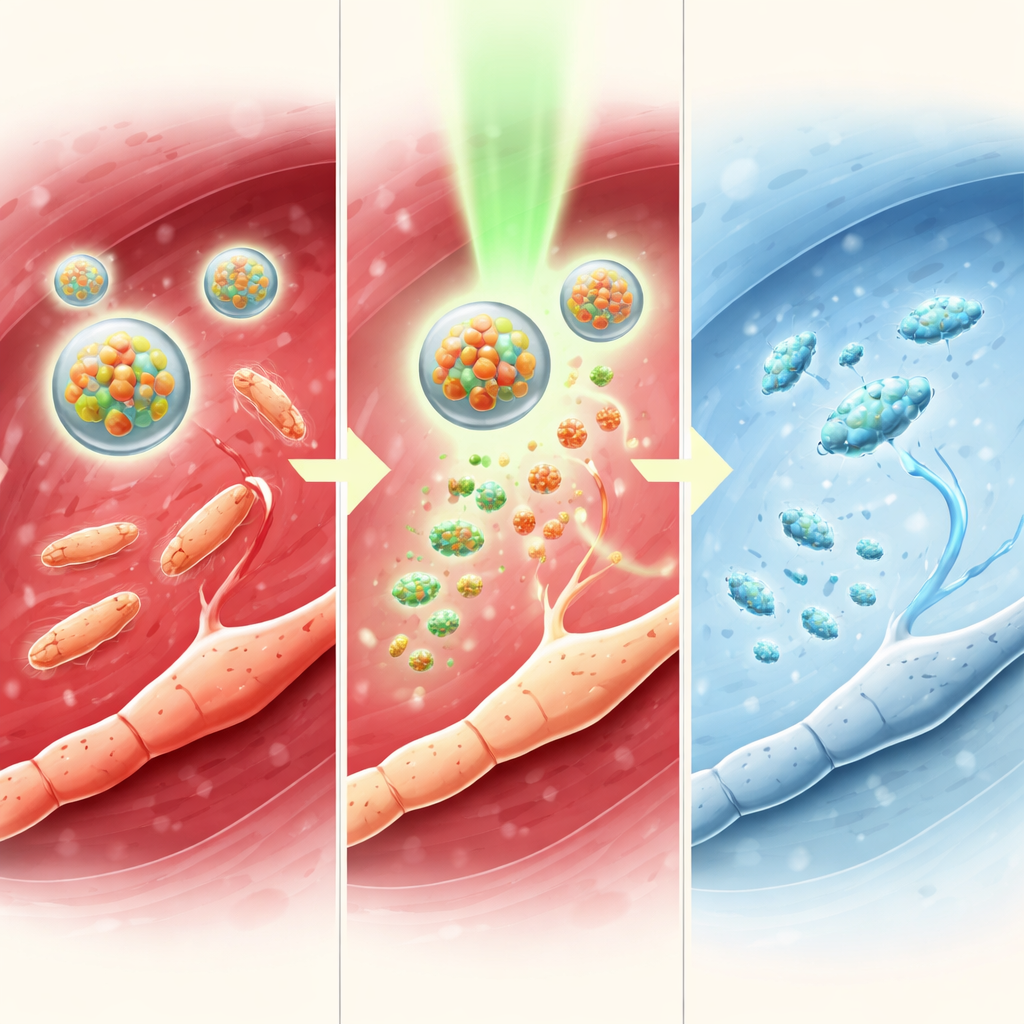
对患者可能的意义
总体而言,这项工作展示了一种单一的光控纳米体系,既能清除顽固细菌感染又能显著减轻相关疼痛。通过化学上将麻醉药“笼控”于释放一氧化氮的结构中并封装入胶束,作者实现了利用温和可见光按需、局部释放两种有效因子的目的。在皮肤伤口和关节感染的动物模型中,这一设计加快了愈合并延长了镇痛时间,优于传统局麻药。尽管在人类应用前仍需大量测试,该研究突出了可切换、智能药物未来有望使感染治疗更有效且更舒适的前景。
引用: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
关键词: 一氧化氮疗法, 光控药物, 抗菌镇痛, 纳米医学, 耐甲氧西林金黄色葡萄球菌(MRSA)感染