Clear Sky Science · zh
Treg-γδ T 细胞轴决定肝癌发生的性别二态性
为何某些肝癌更常侵袭男性
临床上早已观察到肝癌在男性中的发病率约为女性的两倍,但原因并不止于性激素的简单差异。此研究深入肿瘤内的免疫细胞网络,揭示了两类 T 细胞之间一段隐秘对话,解释了为何男性肝脏更易受侵,并指出了可能带来更有针对性治疗的新方向。
肝肿瘤内的免疫拉锯战
肝癌,尤其是肝细胞癌,生长在一个由免疫细胞、血管和瘢痕组织构成的复杂微环境中。作者比较了来自男性和女性的肿瘤样本(包括患者和小鼠模型),发现了显著的不平衡:男性肿瘤中富集了更多的调节性 T 细胞(Tregs),这类细胞通常用于抑制过度的免疫反应。与此同时,其他常见 T 细胞的总数在两性之间差异不大。由于高水平的 Tregs 与更差的生存率相关,研究团队怀疑这些细胞并非旁观者,而是帮助肿瘤逃避免疫攻击的共犯。 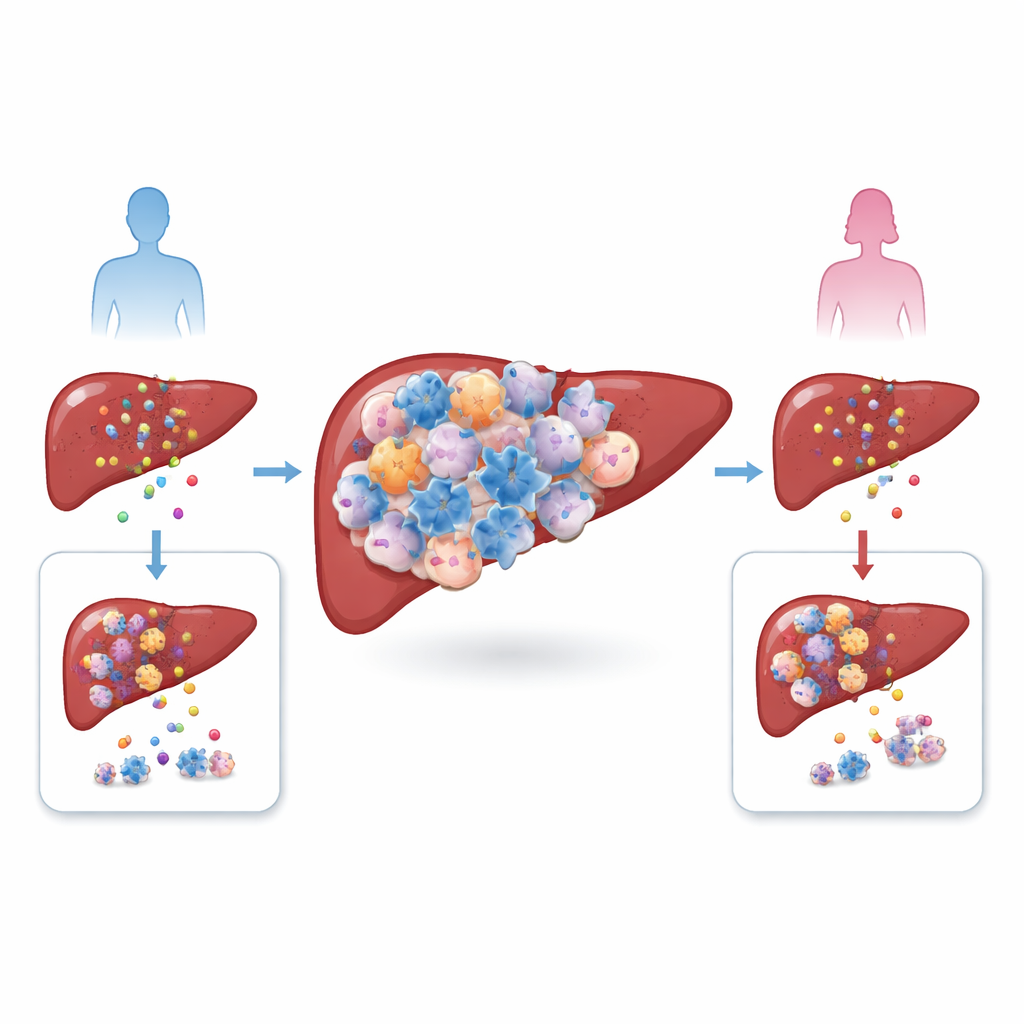
雄性激素如何招来抑制性细胞
为了解为何男性肿瘤招募更多 Tregs,研究者将注意力放在癌细胞产生的化学信号上。他们发现男性肝肿瘤产生更高水平的分子 Ccl2,而 Tregs 表达更多与之匹配的受体 Ccr2。这一配对像归巢信号一样将 Tregs 吸引到肿瘤中。当在小鼠中去除 Ccl2 信号或 Ccr2 受体时,肿瘤缩小,侵入肝脏的 Tregs 大幅减少,尤以雄性为著。研究团队进一步表明,主要雄性性激素睾酮驱动了这一过程:它激活肝癌细胞中的一条蛋白链,从而开启 Ccl2 基因,增强招募 Tregs 的化学信号。被阉割的雄性小鼠(睾酮减少)其肿瘤中 Ccl2 水平降低,浸润的 Tregs 也更少。
本可抵抗癌症却被压制的守卫细胞
另一类 T 细胞,称为 γδ T 细胞,可充当快速反应的“守卫者”,在无需常规抗原呈递的情况下识别并杀死肿瘤细胞。在健康肝脏中,这类细胞相对稀少,但在肝癌中它们可以成为强有力的抗肿瘤战士。研究发现,女性肿瘤中含有更多 γδ 细胞,且这些细胞更为活跃,携带更多毒性分子。去除小鼠体内的雄性激素会增加肿瘤中 γδ 细胞的数量和活力,而经典的杀伤性 CD8 T 细胞则基本不受影响。在体外培养中,γδ 细胞能有效损伤肝癌细胞,但当加入 Tregs 时,这种效应被削弱,表明 Tregs 特异性地抑制了这类有前景的抗肿瘤细胞群。
缺氧、秘密包裹与被沉默的防御者
继续深入探查,研究者问道 Tregs 是如何抑制 γδ T 细胞的。在肿瘤内部,氧气往往匮乏,这种状态称为缺氧。在低氧条件下,男性肿瘤中的 Tregs 开始大量产生一种名为 S100a4 的蛋白。S100a4 并非以游离分子的形式直接发挥作用,而是被封装进被膜包裹的微小颗粒——细胞外囊泡中。这些囊泡从 Tregs 出芽并被邻近的 γδ T 细胞摄取。进入细胞后,S100a4 重塑了这些细胞的基因调控:它降低了控制关键信号传导和杀伤分子的 DNA 区域的开放性并减弱了它们的活性。γδ 细胞对其 T 细胞受体介导的应答能力下降,释放毒性蛋白与细胞因子的能力也被削弱,从而实质性地钝化了它们的抗癌利刃。 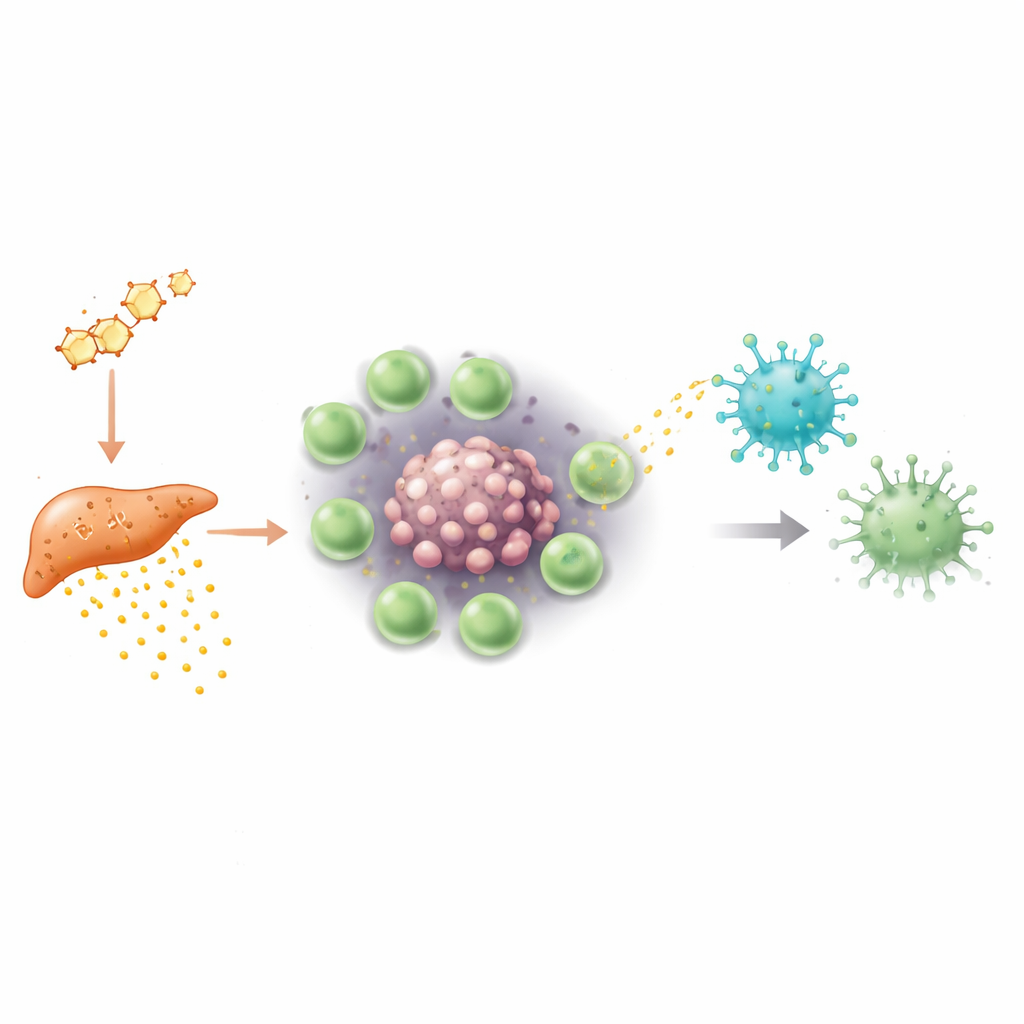
打破这一有害回路
最后,团队测试了若中断这条 Treg–S100a4–γδ 通路会如何。在基因工程小鼠中,使 Tregs 无法产生 S100a4,雄性肝肿瘤缩小,肿瘤中整体 S100a4 水平下降,且 γδ T 细胞数量与活性上升。值得注意的是,肿瘤中 Tregs 的数量并未减少——只是它们对 γδ 细胞的抑制作用被解除。这一改变几乎消除了雄性与雌性小鼠之间肿瘤严重程度的常见差距,凸显了该通路在性别差异肝癌中的关键作用。
对未来治疗的意义
通俗地说,研究表明雄性激素促使肝癌细胞发出更强的“欢迎信号”以吸引免疫抑制性的 Tregs。Tregs 一旦进入肿瘤,并在低氧压力下,会通过分泌装载 S100a4 的囊泡悄然解除附近 γδ T 细胞的武装,而这些 γδ 细胞本可能对控制癌症至关重要。通过针对带来 Tregs 的 Ccl2 信号,或针对使 γδ 细胞沉默的 S100a4 信息,未来的治疗有望恢复机体自身防御,尤其是在男性患者中。这项工作提示,肝癌治疗或应考虑性别差异,并利用而非忽视 γδ T 细胞的独特优势。
引用: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
关键词: 肝细胞癌, 调节性 T 细胞, γδ T 细胞, 性别差异, 肿瘤免疫学