Clear Sky Science · zh
嘧啶能钙信号将肾小管代谢与肾脏疾病中的纤维化连接起来
为何肾脏瘢痕很重要
慢性肾脏病在全球悄然影响数亿人,常常以肾脏出现瘢痕和僵硬为终点。一旦这种称为纤维化的瘢痕形成,丧失的肾功能很难恢复。然而,临床上仍缺乏能专门阻止纤维化的药物。本研究提出了一个基础但关键的问题:肾小管的短期损伤如何逐步演变为持久的瘢痕组织,阻断这一过程是否能减缓或预防肾功能衰竭?
繁忙的肾小管及其隐藏的化学活动
肾脏的近曲小管是微观的工作单元,回收血液中过滤出的绝大部分水分和营养物质。为完成这项工作,它们的代谢非常活跃。研究者通过分析小鼠肾脏的单细胞基因表达数据发现,这些小管细胞富含参与嘧啶处理的基因——嘧啶是一类通常用于构建和修复 DNA 与 RNA 的小分子。在受损的小管中,一条“回收”通路中的酶——胞苷脱氨酶明显上调,提示受损细胞通过重新调整嘧啶利用来维持某些能量丰富的构建单元(包括一种名为 UDP 的化合物)的供应。
从受损细胞溢出的信号
当团队用模拟化疗或叶酸过量的毒性物质损伤培养中的类人肾小管细胞时,细胞向周围液体释放了 UDP。在实际受伤的小鼠肾脏组织切片染色中,既可见小管中嘧啶处理酶的高表达,也可见邻近的支持细胞——成纤维细胞——出现活化和形态变化的迹象。成纤维细胞通常安静地位于小管之间,但一旦被激活,它们会增殖并沉积胶原与其它纤维,导致肾组织增厚和僵硬。这些观察提示了一个简单想法:受损小管可能在“泄露”化学应激信号,邻近的成纤维细胞能够感知到这些信号。
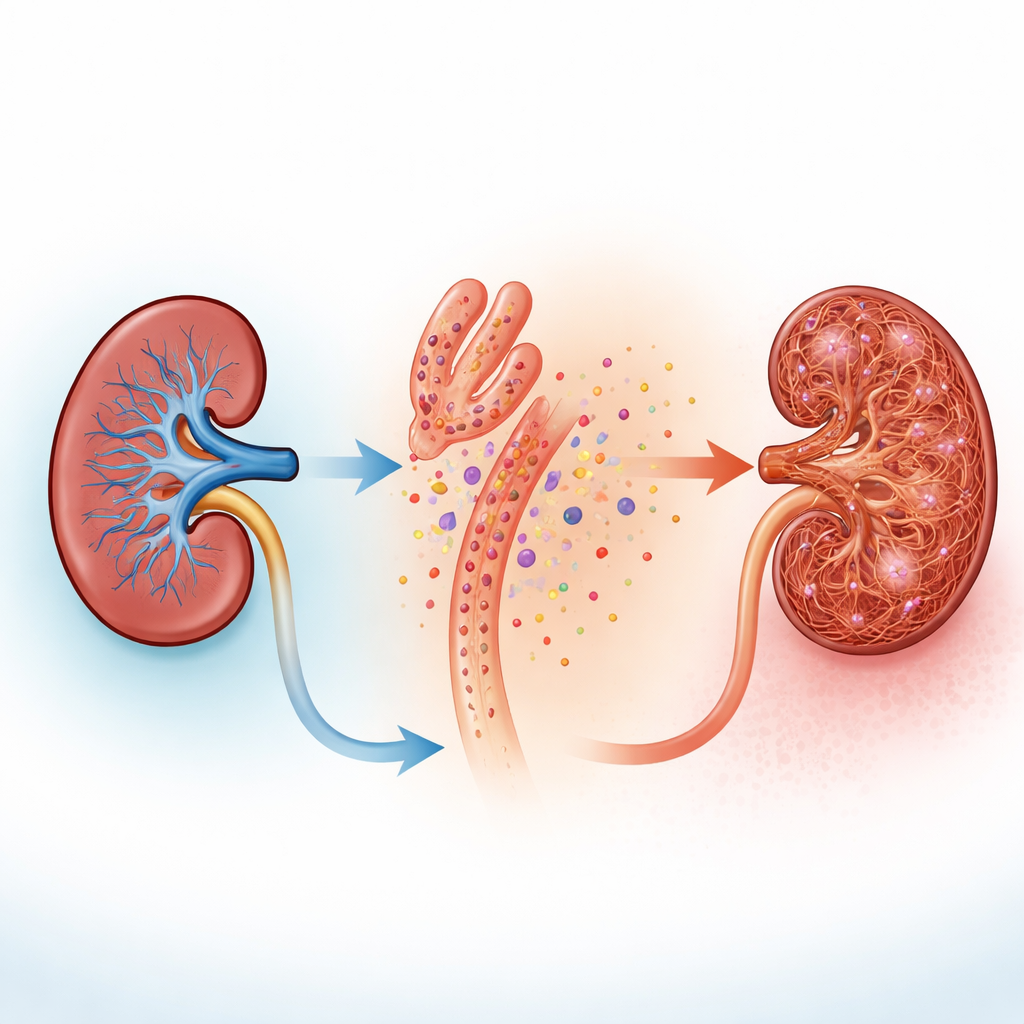
成纤维细胞如何通过钙闪烁“倾听”
成纤维细胞上负责“监听”的疑似分子是 P2Y6 受体——一种对 UDP 有反应的表面蛋白。作者挖掘了多组单细胞数据,发现 P2Y6 在基质细胞上表达,并在慢性肾病小鼠模型中进一步升高。对整个肾脏的测量也证实在两种不同的纤维化模型中 P2Y6 水平显著上调。在新鲜肾切片和经过工程改造、在细胞内钙升高时会发光的培养肾脏成纤维细胞中,加入 UDP 或激活 P2Y6 的药物会触发快速的钙激增。这些钙闪烁从包绕小管的细长突起开始,然后传播到细胞体,当 P2Y6 被阻断或钙被化学方式清除时,这些闪烁消失。在活体小鼠中,高分辨率体内显微镜显示包绕小管的成纤维细胞频繁出现不规则的钙活动,并且在小管受损时这种活动显著增强,即便小管细胞自身趋于沉寂。
从短暂信号到持久瘢痕
细胞内的钙爆发不仅是瞬间现象;它们可以重新编程细胞行为。当培养的成纤维细胞暴露于激活 P2Y6 的化合物时,它们增殖更快、迁移更活跃,并启动与更具攻击性的“肌成纤维细胞”状态相关的基因。这些基因编码的蛋白质(如纤维连接蛋白、中间纤维蛋白 vimentin 和胶原)直接促进瘢痕形成。阻断 P2Y6 或阻止钙升高可以抹去这些改变,敲低该受体基因也会削弱反应。在小鼠中,两种不同形式的肾损伤——输尿管阻塞和叶酸性肾病——表现出相同的模式:受损肾脏中增殖的成纤维细胞更多、肌成纤维细胞标志物增多、胶原沉积更多且纤维化面积更大。
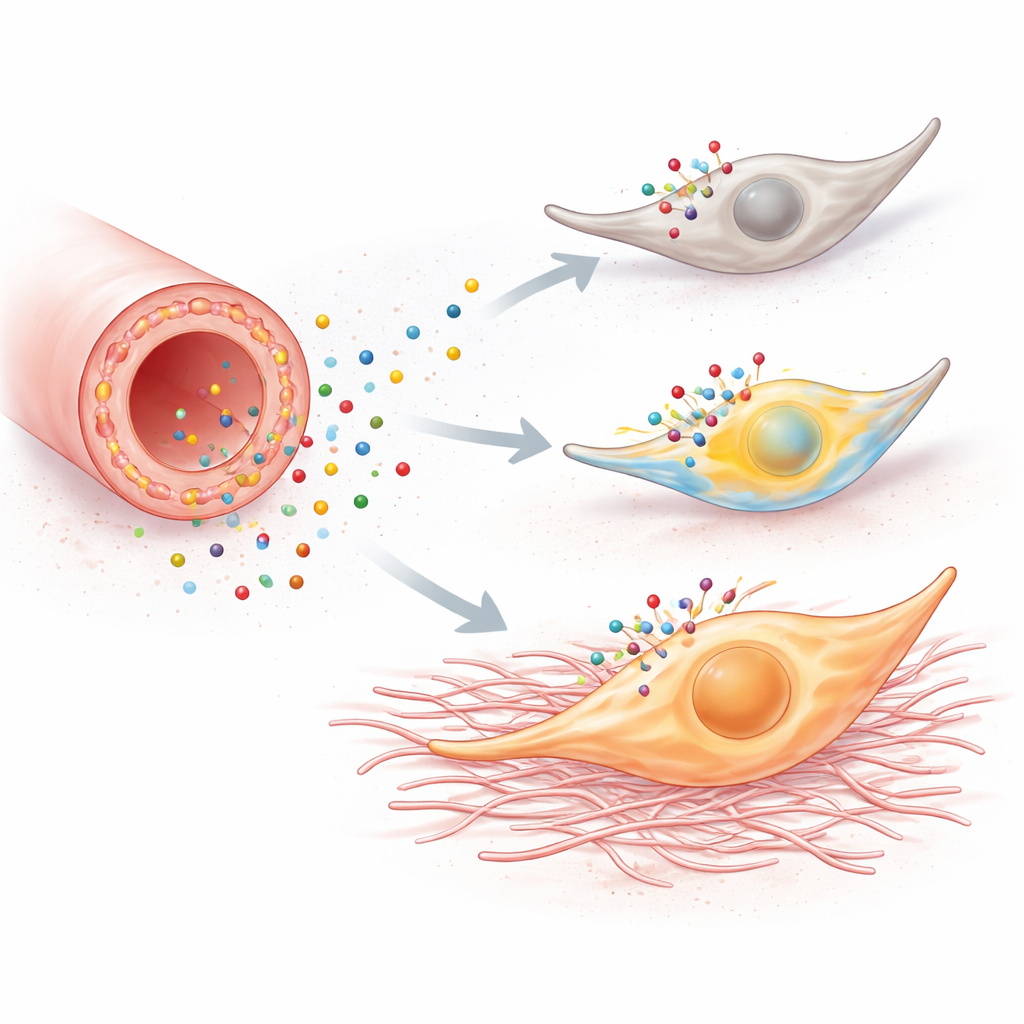
降低有害信号的音量
为了测试这一路径是否不仅存在而且确实有害,研究者通过遗传去除 P2Y6 或用药物阻断它。缺失该受体的小鼠在输尿管阻塞或叶酸损伤后发展出更少的肾纤维化:它们的成纤维细胞增殖更少、纤维基质沉积更少、招募的炎性细胞更少。血液检测显示,这些敲除动物的肾小球滤过功能也保留得更好。用 P2Y6 阻断化合物处理正常小鼠也获得了可比的保护,包括成纤维细胞钙活动被抑制和纤维化减少,尽管血液标志物的改善程度更为可变。
对未来治疗的意义
综合来看,这项工作揭示了一条简单但有力的事件链:当肾小管细胞受伤时,它们改变内部代谢并向周围组织释放 UDP。邻近的成纤维细胞通过其 P2Y6 受体感知这一分子,细胞内出现钙爆发,随后转为促瘢痕模式——增殖、迁移并沉积胶原。中断这种基于嘧啶的钙信号传导,特别是在 P2Y6 这一步,能在多种小鼠模型中显著减轻纤维化。对患者而言,这提示了一类新的药物靶点:选择性阻断肾脏中 P2Y6 的化合物可能有助于切断常见肾损伤与导致慢性肾脏病的缓慢、不可逆瘢痕化之间的联系。
引用: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
关键词: 慢性肾脏病, 肾脏纤维化, 成纤维细胞信号传导, 嘧啶代谢, P2Y6 受体