Clear Sky Science · zh
两分子CCM2同时招募到KRIT1抑制KLF4表达
为何大脑血管需要精细调控
大脑中的血管需在两者之间取得平衡:它们必须足够坚固以防止渗漏,同时又要足够灵活以响应机体需求。当这种平衡失衡时,可能出现脑海绵状血管畸形——由易损、泡状的血管簇组成,可能出血并引发癫痫或中风。本研究揭示了三种蛋白之间此前未知的分子“握手”机制,说明该机制如何维持脑血管的稳定,以及该握手被破坏如何促发疾病。
血管健康的把关者
血管内皮细胞依赖一组主开关——KLF2 和 KLF4——来调控维持血管强度和身份的基因。当这些开关被过度激活时,血管会异常并易受损伤。另有两种蛋白,KRIT1 和 CCM2,被认为是该系统的守护者。遗传上携带这两种蛋白任一缺陷版本的人,罹患脑海绵状血管畸形的风险很高。然而迄今为止,科学家尚未完全弄清 KRIT1 与 CCM2 如何协同作用以抑制 KLF4。
出人意料的三人团队
研究者在实验室中使用类人内皮细胞,并用基因工具选择性降低 CCM2 或 KRIT1 的含量。任一蛋白被耗减时,KLF4 水平大幅上升,这与动物模型和患者中的观察一致。恢复正常水平的 CCM2 或 KRIT1 可使 KLF4 回落——但前提是恢复的蛋白仍能彼此结合。通过在 CCM2 与 KRIT1 相互作用的区域进行精确改造,团队表明这种物理接触对于防止 KLF4 上升至关重要。这些实验将 KRIT1–CCM2 的伙伴关系确立为控制该强大转录因子的核心机制。
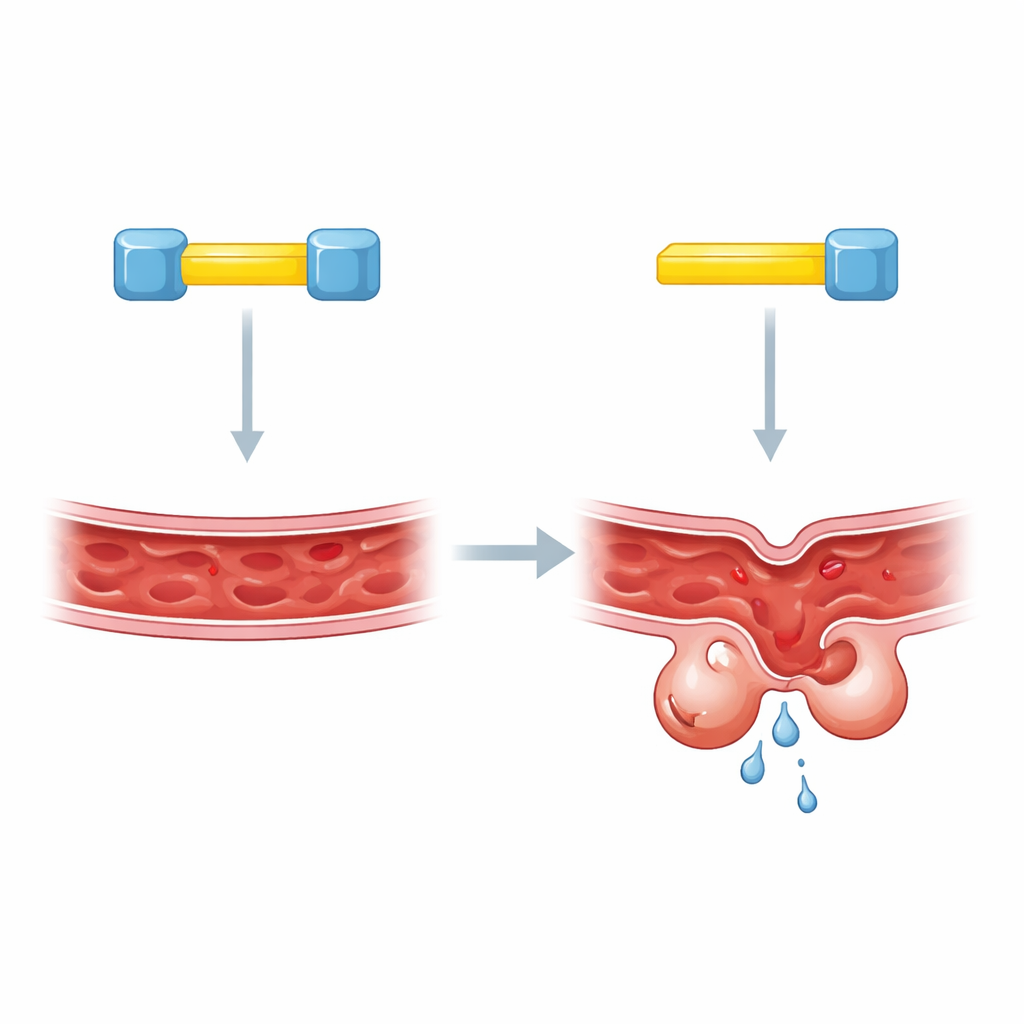
一把钥匙两个锁
为进一步深入研究,作者聚焦于 KRIT1 中作为分子对接位点的短片段。早期工作提示 CCM2 可在其中一处位点与 KRIT1 结合,但不同方法得出了互相矛盾的结论。新研究揭示了混淆的根源在于真实情况更为复杂:KRIT1 带有两个相邻的对接片段,且两者都必需。任一片段被破坏时,KLF4 水平仍异常升高,就像完全缺失 KRIT1 一样。经过工程改造的细胞中的生化检测显示,单个 KRIT1 蛋白可以同时桥接两个独立的 CCM2 分子,暗示一种出人意料的三方组装结构。
详见分子夹子的结构
接着,团队纯化了 CCM2 与 KRIT1 的相关片段,并在溶液与晶体中检查它们如何聚合。对复合体质量的测量显示,关键 CCM2 区域的两个拷贝可结合到带有这一对对接位点的单条 KRIT1 片段上。高分辨率的结构快照确认了这种 2:1 的排列:一条延伸的 KRIT1 肽段穿插在两个 CCM2 结构域之间,每个对接位点嵌入不同 CCM2 分子上的相似口袋中。对接位点之间的一段短螺旋有助于将两个 CCM2 结构域并排定位,形成紧密如夹子的结构。这种双重结合——两个结合结构域钩住同一伙伴上的串联位点——在此类蛋白模块家族中此前未曾见过。
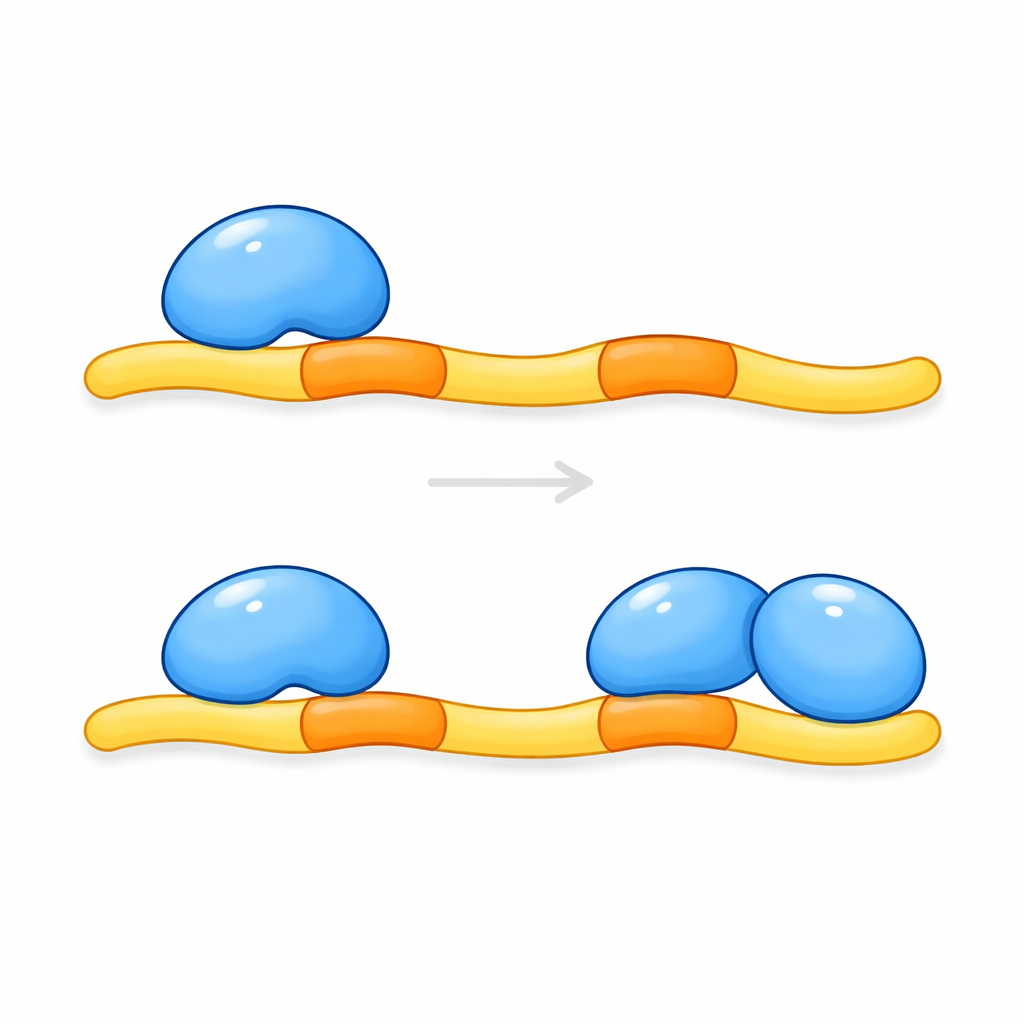
对脑部疾病及更广泛领域的意义
这些发现表明 KRIT1 并非仅仅结合一个 CCM2 分子;相反,它充当支架,招募一对 CCM2 蛋白。只有当 KRIT1 的两个对接位点都被占据时,该复合体才能恰当地抑制 KLF4 的产生,从而有助于防止脆弱血管的形成。因此,干扰任一对接位点的 KRIT1 突变预计会削弱这一保护性夹子,或可解释某些遗传性脑海绵状血管畸形的成因。鉴于许多其它人类蛋白也携带类似的双位点结构,这项研究还提示了一个更广泛的原则:相关结构域成对结合可能是细胞微调信号网络的常见方式。理解这种三方相互作用最终可能为稳固有出血风险人群的血管提供策略方向。
引用: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
关键词: 脑海绵状血管畸形, 内皮细胞, KRIT1, CCM2, KLF4