Clear Sky Science · zh
基于纳米抗体的IgG同时抑制优势蜂毒过敏原的致敏和酶学活性
为什么蜂蜇过敏很重要
对大多数人来说,蜂蜇会带来短暂的疼痛。但对另一些人,蜂蜇可触发危及生命的全身反应——过敏性休克。当前主要的预防性治疗是蜜蜂毒免疫疗法,能帮助许多患者,但需要多年时间、频繁注射,并且本身可能引发过敏副作用。本研究探索了一种更有针对性的保护方法,通过在关键毒性成分造成伤害之前使其失效,来保护对蜂毒高度过敏的人群。
蜂毒中的主要祸首
蜂毒是由多种分子组成的混合物,但有一种蛋白——磷脂酶 A2(亦称 Api m 1)尤为突出。它是蜂毒过敏患者的主要致敏原,几乎存在于所有此类患者体内。Api m 1 扮演双重角色:它能破坏细胞膜,促成蜇伤部位的疼痛和炎症;同时,它也是诱发过敏的抗体(IgE)的主要靶标。当 Api m 1 与锚定于肥大细胞和嗜碱细胞等免疫细胞表面的 IgE 结合时,可能引发级联反应,导致炎性介质的突然释放,在严重情况下引发过敏性休克。
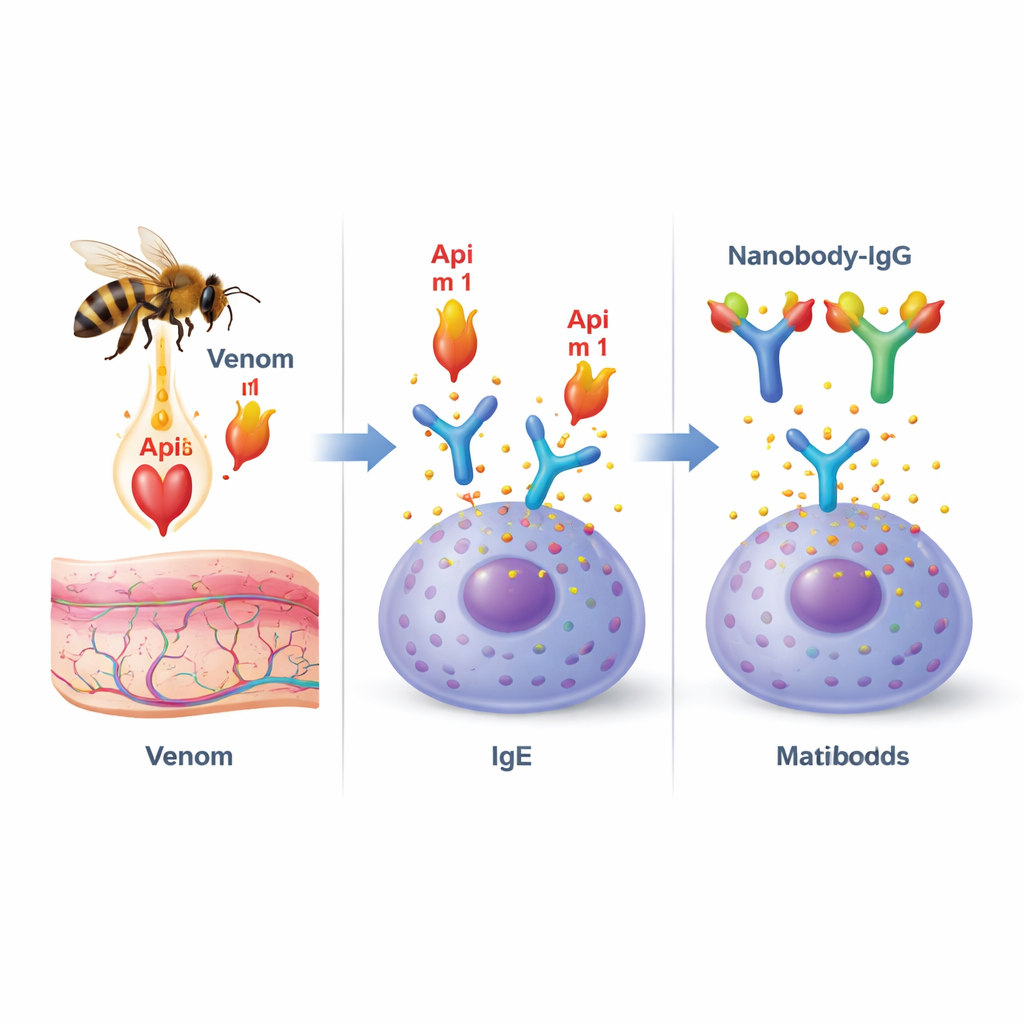
设计微小抗体阻断过敏原
研究者转向了“纳米抗体”——一种最初在骆驼科动物中发现的微小、稳定的抗体片段。纳米抗体体积小、形状细长,擅长嵌入蛋白表面的沟槽与口袋中。团队从免疫文库中分离出针对 Api m 1 的纳米抗体,并挑选出两种表现突出的候选者,命名为 AM1‑1 和 AM1‑4。通过 X 射线晶体学的详细结构研究表明,这两种纳米抗体夹持于 Api m 1 的相对两侧,彼此不互相干扰。纳米抗体 AM1‑1 正好位于酶的活性中心之上,提示其可能阻断 Api m 1 的膜破坏功能;而 AM1‑4 则停靠在蛋白表面的另一个独立口袋中。
将纳米抗体转变为强效阻断剂
为了将这些小型结合体转化为长效药物,科学家将每种纳米抗体与人类 IgG1 的 Fc 片段融合,制成更大、在血液中更稳定的类抗体分子。他们还设计了一种“双特异性”版本,在单一的 IgG 样分子上同时携带 AM1‑1 与 AM1‑4。体外实验显示,这些纳米抗体‑IgG 融合体以极高亲和力结合 Api m 1,并能显著减少来自蜂毒过敏患者血液中 IgE 与 Api m 1 的结合。在细胞实验中,它们降低了嗜碱细胞的激活——这些免疫细胞在过敏个体暴露于 Api m 1 时通常会强烈反应。
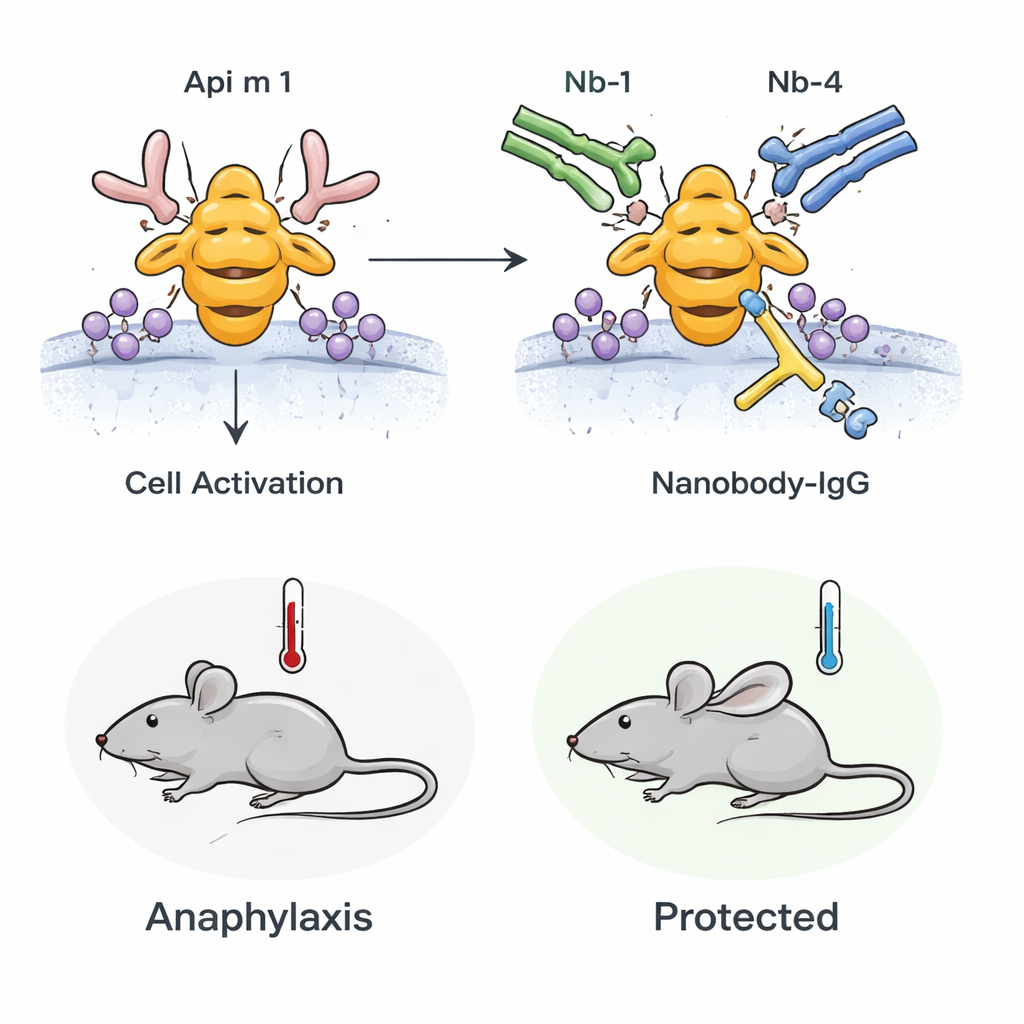
从试管到活体动物
研究团队接着检验这种阻断作用在活体中能否维持。他们使用对蜂毒致敏的小鼠,使其免疫系统对 Api m 1 的反应模拟人类过敏。当这些小鼠受到 Api m 1 挑战时,会出现过敏性休克的体征,包括体温下降和血中肥大细胞活化标志物上升。然而,如果在挑战前用双特异性纳米抗体‑IgG 预处理,小鼠的体温下降和肥大细胞激活均显著减轻。这表明,既有的高亲和力阻断抗体可以在体内减弱对 Api m 1 的全身性过敏反应。
这对蜂毒过敏患者意味着什么
总体而言,该研究表明,经过精心设计的基于纳米抗体的 IgG 分子能够同时阻断 Api m 1 的致敏与酶学活性——这是蜂毒过敏中的主要罪魁祸首。对患者来说,这提出了一种季节性被动免疫的可能性:在蜂蜇高发的几个月里注射几次此类抗体,或可提供对严重反应的暂时保护,而无需传统蜜蜂毒免疫疗法那样长期的承诺与风险。尽管仍需更多工作以将该策略推广到其他毒素成分并在人体中检验安全性与有效性,但这种纳米抗体策略为保护易感个体免受致命蜂蜇提供了一种精确的新途径。
引用: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
关键词: 蜂毒过敏, 纳米抗体, 被动免疫治疗, 磷脂酶A2, 预防过敏性休克