Clear Sky Science · zh
磷酸甘油酸脱氢酶介导的丝氨酸重编程加剧小鼠铜绿假单胞菌肺炎中的巨噬细胞过度炎症反应
当身体的防御者走得太远
由细菌铜绿假单胞菌引起的肺炎 notoriously 难以治疗,尤其是在肺功能受损的人群中。抗生素针对微生物,但这种疾病常常致命,不仅因为细菌本身,还因为机体自身的免疫反应失控。本研究揭示了免疫细胞内的一个代谢“开关”如何将其从有益推向有害——并提示通过调整饮食或细胞代谢可能缓解危及生命的肺部炎症。
病原体与免疫系统之间的危险舞蹈
铜绿假单胞菌是一种常见的革兰氏阴性细菌,可入侵下呼吸道并诱发严重肺炎。通常,驻留在肺内的免疫细胞称为巨噬细胞,它们在肺泡中巡逻,吞噬入侵者并通过化学信号发出警报。但当细菌负荷很高时,这些细胞会从血液中招募大量后备巨噬细胞。结果可能是一场炎性分子风暴,损伤脆弱的肺组织,干扰修复过程,在严重情况下导致呼吸衰竭和死亡。作者探讨了这些巨噬细胞的内部代谢是否可能驱动这种有害的过度反应。
代谢酶处于风口浪尖
研究小组将注意力集中在一种称为磷酸甘油酸脱氢酶(PHGDH)的酶上,它是细胞将葡萄糖转化为氨基酸丝氨酸的通路中的关键起点。在小鼠铜绿假单胞菌肺部感染模型中,肺组织中尤其是巨噬细胞内的PHGDH水平和活性显著上升。当小鼠接受小分子PHGDH抑制剂处理,或当PHGDH基因在髓系细胞(包括巨噬细胞)中被特异性删除时,动物的结局更好:存活时间更长、肺损伤减少、细菌载量下降,并且如白细胞介素‑6和白细胞介素‑1β等强效炎性细胞因子的产生降低。在细胞水平上,阻断PHGDH使巨噬细胞远离强烈促炎表型,但并未促进相对的伤口修复表型。
助燃因素:丝氨酸与过度活跃的信号回路
进一步探究显示,感染将巨噬细胞重编程为将更多葡萄糖导入新生丝氨酸的合成,且这种丝氨酸反过来加剧炎症。额外的丝氨酸使巨噬细胞分泌更多炎性细胞因子并表达更多激活相关的表面标志,而限制丝氨酸的饮食则保护了受感染的小鼠并降低了细菌计数。在机制上,丝氨酸进入“一碳”代谢循环,帮助供应细胞的甲基供体,即参与表观遗传调控的化学标记。这增强了靠近抑制性蛋白DUSP4基因的特定组蛋白标记H3K27三甲基化,而DUSP4通常有助于关闭ERK1/2信号通路。当DUSP4受到抑制时,ERK1/2持续处于开启状态,放大炎性信号。抑制PHGDH或降低丝氨酸可以逆转这一链条,恢复DUSP4并减少ERK1/2的磷酸化。
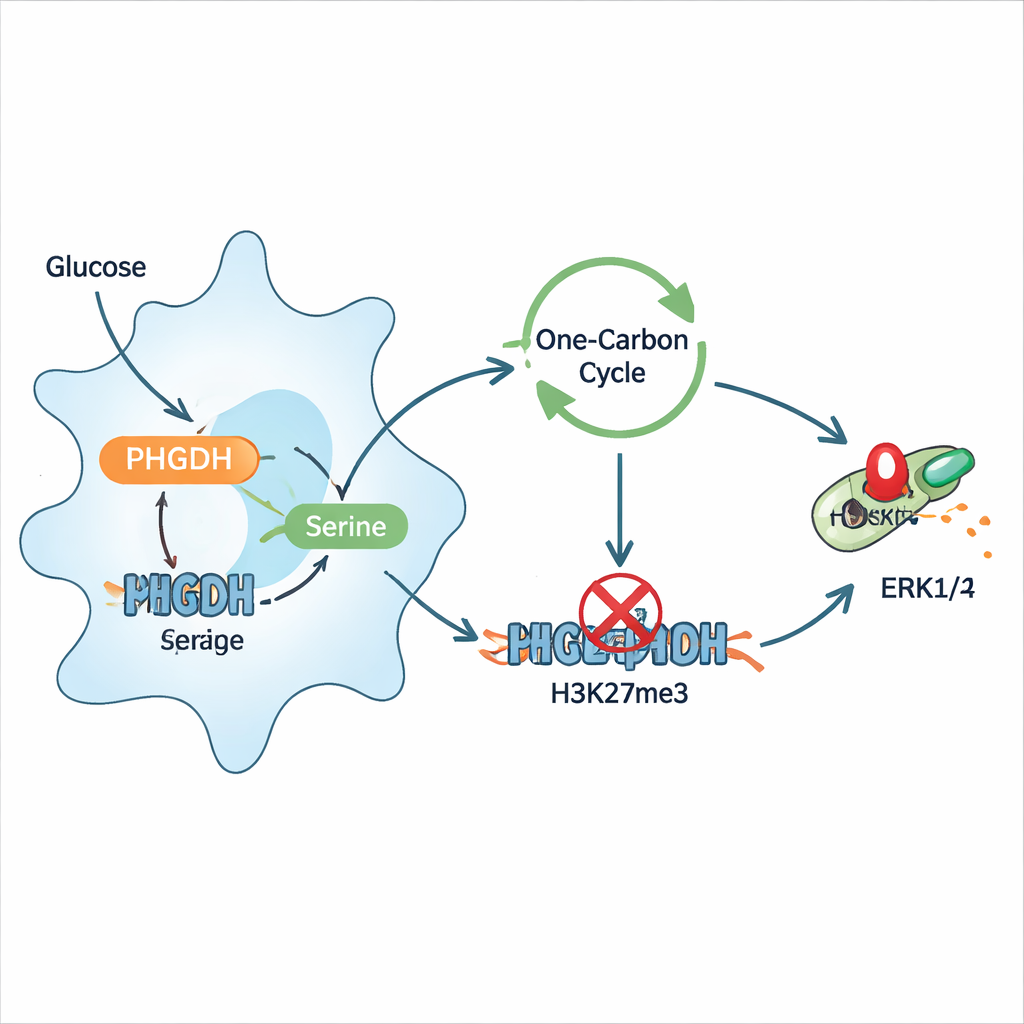
在不削弱防御的情况下重新平衡巨噬细胞
重要的是,调低PHGDH并没有简单地瘫痪免疫系统。实际上,缺乏PHGDH的巨噬细胞在感染早期更善于吞噬并杀死铜绿假单胞菌,同时产生更少的有害细胞因子。将这些缺乏PHGDH的巨噬细胞转移到正常小鼠体内后,在细菌挑战后改善了结局,强调益处来自于改写宿主反应而非直接针对微生物。这项工作也提示,富含丝氨酸的饮食在严重细菌性肺炎期间可能无意中促进超量炎症,而受控的丝氨酸限制可能提供一种新的方式来抑制过度的肺损伤。
对难治性肺炎治疗的意义
通俗地说,这项研究表明,在铜绿假单胞菌肺炎中,部分巨噬细胞以一种使其产生额外丝氨酸的方式燃烧糖类,而这一代谢偏离使其炎症机制长时间处于过度运转状态。通过阻断酶PHGDH或限制丝氨酸,研究者能够平息这种过度反应,保护肺组织,同时仍允许免疫细胞清除细菌。尽管这些工作基于小鼠且距离临床应用尚远,但它提出了一个有前景的思路:将传统抗生素与可微调免疫细胞代谢的药物或饮食策略配合,可能把毁灭性的免疫大火变成受控的抗菌之焰。
引用: Chen, R., Zeng, R., Shi, M. et al. Phosphoglycerate dehydrogenase-mediated serine reprogramming aggravates macrophage hyperinflammation in murine Pseudomonas aeruginosa pneumonia. Nat Commun 17, 1944 (2026). https://doi.org/10.1038/s41467-026-69539-1
关键词: 铜绿假单胞菌肺炎, 巨噬细胞代谢, 丝氨酸生物合成, 肺部炎症, PHGDH