Clear Sky Science · zh
FOXF2 调控围管细胞—内皮细胞的信号传导,对新生儿高氧肺损伤后的血管稳态至关重要
为什么新生儿肺需要小心保护
对于早产婴儿来说,呼吸可能十分困难。许多婴儿需要额外供氧以维持生命,但这种救命疗法也可能损伤他们脆弱的肺组织和血管,促成一种名为支气管肺发育不良的慢性病。本研究考察了一类少为人知、包裹在肺微小血管周围的支持细胞,并揭示了一个关键的基因开关,帮助这些细胞在氧损伤后保护并修复新生儿肺。
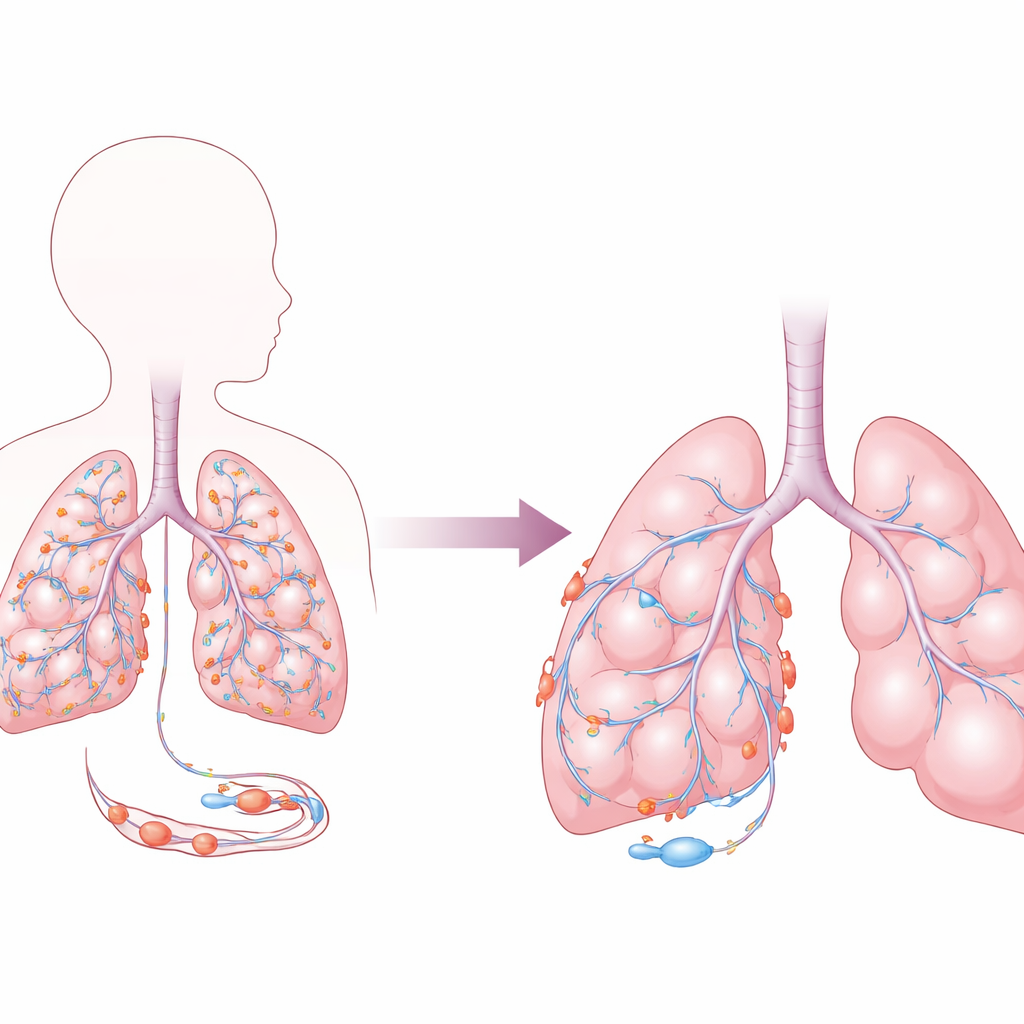
围绕肺血管的隐形助力者
肺中的气囊是氧进入血液的场所,其表面布满致密的毛细血管网。许多毛细血管外包裹着围管细胞,这些支持细胞有助于维持血管稳定、指导新血管生长,并保持紧密屏障以防液体渗入气腔。作者聚焦于名为 FOXF2 的基因——一种在围管细胞内控制其他基因开启或关闭的转录因子。通过分析来自发育中小鼠肺的单细胞 RNA 数据,他们发现围管细胞中的 Foxf2 活性在出生后随围管细胞成熟、血管发育和细胞迁移相关基因一同上升。相比之下,邻近其他细胞类型中该基因活性明显较低,提示其在这些血管支持细胞中具有专门化作用。
当对围管细胞的“刹车”被移除
为检验 FOXF2 的实际功能,研究团队构建了可以在出生后特异性删除 PDGFRβ 阳性围管细胞中 Foxf2 的小鼠。在正常氧条件下,整体肺结构和血氧水平大体正常,但细节显示出不同的景象。围管细胞过度增殖并在毛细血管周围密集堆积,同时成熟且功能良好的围管细胞标志物下降。这些围管细胞更可能处于细胞周期的 DNA 合成期,体外实验也证实,直接阻断培养的围管细胞中的 Foxf2 会促进它们增殖并降低其迁移能力。与此同时,通常有助于血管生长和稳定的基因(如 Angptl4 和 Angpt2)表达下调,而驱动细胞分裂和能量代谢的基因上调。综合来看,这描绘出数量增多但能力下降的围管细胞状态。
氧应激揭示关键弱点
当新生小鼠暴露于高氧水平——一种标准的早产肺损伤模型——时,后果变得更为严重。在小鼠肺以及来自患有支气管肺发育不良婴儿的人类样本中,围管细胞中的 FOXF2 在此类损伤后明显减少。Foxf2 缺失的小鼠在高氧暴露下存活率大幅下降,血氧饱和度降低,气囊变大且变得简单化,表明肺泡发育受损。与此同时,肺泡内的毛细血管覆盖减少,内皮细胞分裂减少,更多的荧光示踪剂从血管渗出到肺组织——这是血管屏障失效的信号。流式细胞术证实,在损伤条件下,内皮细胞数量下降而围管细胞进一步积累并保持高度增殖,突出显示这两类细胞之间正常协作的崩溃。
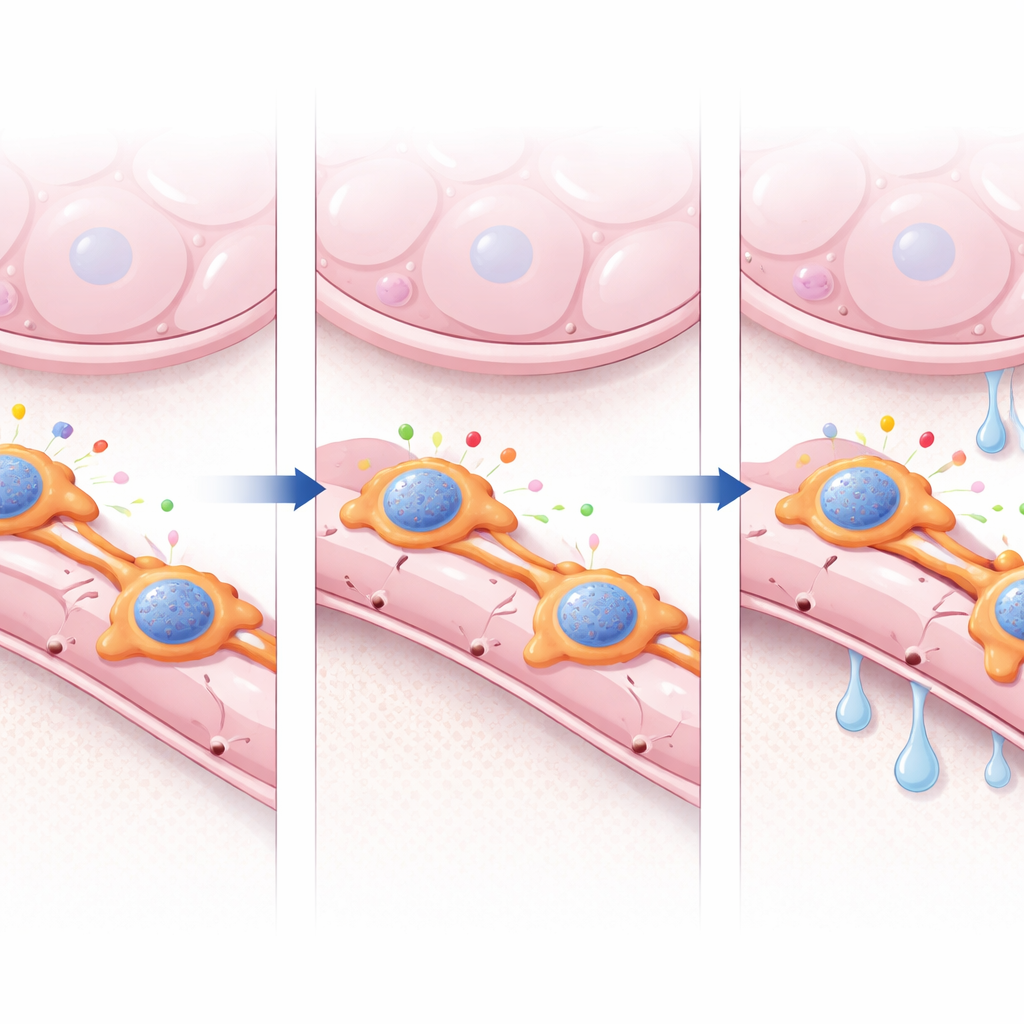
围管细胞信号如何塑造血管修复
进一步探查分子层面的串话,研究者使用计算工具绘制了围管细胞与内皮细胞之间的信号通路图。在健康肺中,促进血管生长与稳定的通路占主导地位,包括涉及 ANGPTL4 的通路——一种具有促血管生成和调节屏障功能的分泌蛋白。在 Foxf2 缺失的肺中,这些有益信号减弱,而应激和炎症通路增强。从 Foxf2 缺失围管细胞的条件培养基对人肺内皮细胞进行体外试验,可见其支持的管腔形成减少,但加入重组 ANGPTL4 部分挽救了这一缺陷,指向 FOXF2–ANGPTL4 轴作为修复的关键驱动因子。染色质组学分析进一步显示 FOXF2 结合于许多促血管生成基因附近并帮助维持其周围 DNA 区域的开放性。当 FOXF2 丧失时,上千个这些位点的可及性下降,包括 Angptl4 基因座,提示 FOXF2 充当染色质组织者,使其他因子能够维持健康的围管细胞基因程序。
对脆弱新生儿肺的意义
综上所述,这些发现表明 FOXF2 为一位主调控因子,维持新生儿肺围管细胞的成熟,限制其过度生长,并使其能够向邻近内皮细胞发送适宜的信号。当氧损伤导致 FOXF2 水平下降时,围管细胞数量增多但功能受损:它们分泌诸如 ANGPTL4 等滋养性信号减少,毛细血管无法正常再生,血管壁变得渗漏,气囊结构退化。对于照护早产婴儿的家庭和临床医生而言,这项工作强调了围管细胞——以及驱动其功能的 FOXF2 基因网络——作为未来治疗的有希望目标,旨在保护微小血管、改善气体交换并减少早期生命供氧暴露后的长期肺损伤。
引用: Sun, F., Zhao, Y., Do, J. et al. FOXF2 regulates pericyte–endothelial signaling required for vascular homeostasis after neonatal hyperoxic lung injury. Nat Commun 17, 2691 (2026). https://doi.org/10.1038/s41467-026-69525-7
关键词: 支气管肺发育不良, 肺发育, 围管细胞, 血管生成, 新生儿高氧