Clear Sky Science · zh
软骨发育不良中FGFR3信号过度导致静止区软骨细胞周转失衡,通过CREB信号通路介导
这项骨骼生长研究为何重要
软骨发育不良是遗传性短肢侏儒症最常见的病因。它不仅影响身高,还会波及脊柱健康、行动能力和生活质量。现有治疗能带来改善,但不能完全恢复骨骼生长。本研究使用复杂的小鼠模型,揭示了生长中的骨骼中一个先前被忽视的问题区域,并指出一个新的信号开关——CREB,作为未来治疗的有前景靶点。
健康骨骼如何纵向生长
长骨(例如大腿的股骨)在近端和远端的生长板处伸长。生长板由三层主要的软骨细胞区组织而成。顶部是静止区,细胞表现为干细胞库,分裂缓慢并将子细胞向下输送。下面的增殖区包含快速分裂并以有序柱状排列堆叠的细胞,推动骨骼纵向增长。最远端的肥大区则包含增大的成熟细胞,帮助引导新骨形成。这些区域之间的平衡确保骨骼以合适的速率和形态生长。
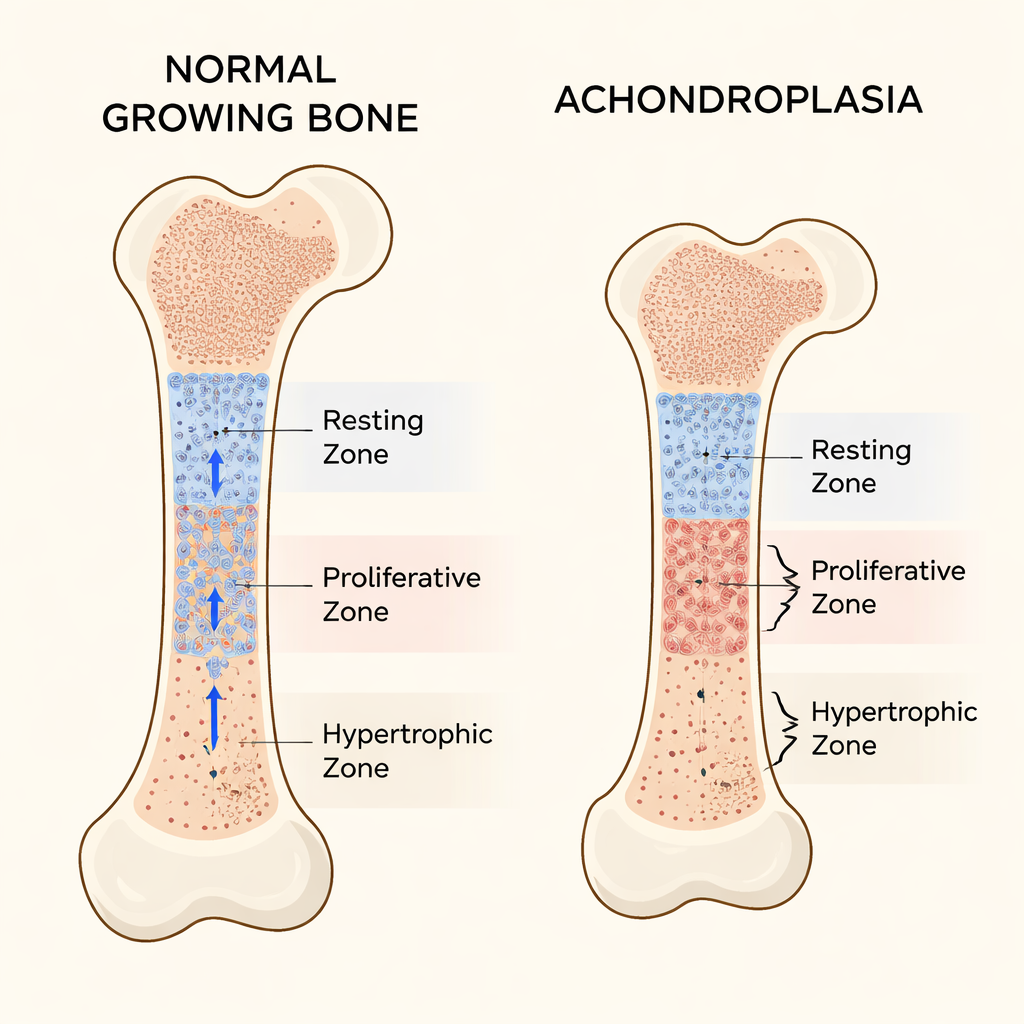
软骨发育不良中发生了什么异常
在大多数软骨发育不良患者中,FGFR3基因的单一突变使其受体过度活化,从而抑制骨骼生长。先前的研究表明,该信号会减慢增殖区的细胞分裂并阻碍肥大区细胞的最终增大。利用携带人类软骨发育不良突变的工程小鼠,作者证实了严重的短肢和缩短的生长板。但精细测量揭示了一个此前多被忽视的现象:静止区异常增厚。该区域并未维持作为稳定、良性运行的干细胞库,而是扩张并包含缺乏正常软骨基质的细胞。
静止区细胞失去“类干细胞”行为
为了解这种扩张,研究团队追踪了生长板细胞随时间的分裂与迁移。在正常小鼠中,静止区细胞很少分裂,其子代细胞沿直线向下迁移,补充增殖区。在突变小鼠中,静止区中更多细胞虽分裂缓慢但停留在原位,导致一层拥挤的细胞堆积,未能适当补给下层区域。多色基因标记的谱系追踪显示,克隆性柱状结构短小且紊乱,子代细胞向随机方向游走,而非形成整齐的堆叠。诸如CD73等类干细胞身份标志在扩大的静止区中丢失,提示过度活化的FGFR3破坏了正常的干细胞利基环境。
新的信号罪魁:CREB
研究者随后使用单细胞RNA测序对数千个生长板细胞进行谱系分析。他们识别出一个与扩张静止区相匹配的独特细胞簇,该簇富含名为Spon1的基因等。通路分析强调了CREB的激活,CREB是一种在被磷酸化后能开启基因表达的蛋白。显微镜下显示,突变小鼠的静止区细胞强烈表达活化的CREB及其共激活因子CBP,同时伴随高水平的FGFR3和下游分子如STAT5。在细胞培养中,刺激FGFR3通路会增强CREB活性并增加SPONDIN1(SPON1蛋白),而阻断FGFR3或CREB则减弱这些信号。这将CREB置于细胞表面过度活化受体与静止区细胞异常行为之间的关键中继位置。
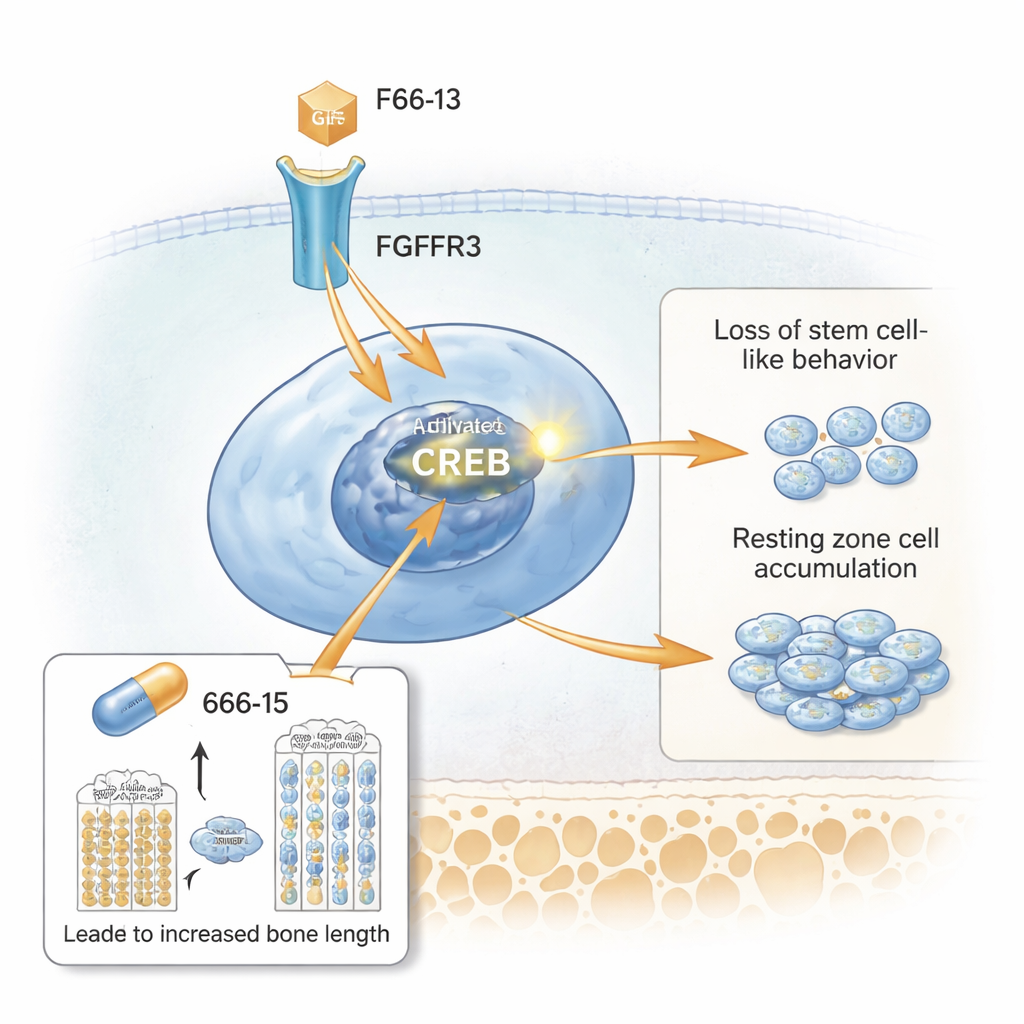
测试一种抑制CREB的药物
最后,研究团队探讨了抑制CREB是否能缓解生长问题。他们在出生后快速生长期期间,用一种小分子CREB抑制剂666-15处理软骨发育不良模型小鼠。与未治疗的突变小鼠相比,接受666-15处理的小鼠体重更大、股骨更长。其生长板形态更接近正常:静止区变薄,增殖区和肥大区恢复高度,软骨基质蛋白重新出现。静止区内CREB过度活化的标志物(包括磷酸化CREB、SPONDIN1和STAT5)降低,而类干细胞标志CD73则恢复。重要的是,在所测试剂量下,同样的药物对健康对照小鼠影响甚微,提示其主要在CREB异常升高时发挥作用。
这对未来治疗意味着什么
该研究表明,在软骨发育不良中,过度活化的FGFR3不仅抑制增殖区和肥大区的细胞分裂与增大;它还通过激活CREB扰乱静止区的安静、类干细胞状态。这种破坏使下层生长板区域得不到足够的新细胞,进而导致骨骼缩短。现有药物如vosoritide主要作用于增殖区和肥大区的其他通路,仅能部分恢复骨长。将CREB加入潜在靶点名单——尤其是针对静止区——未来的联合疗法或许能更全面地恢复软骨发育不良儿童的生长。
引用: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
关键词: 软骨发育不良, FGFR3, 生长板, 软骨干细胞, CREB信号通路