Clear Sky Science · zh
同时靶向 STING、TGF-β 和 PD-L1 增强 CXCL16–CXCR6 信号以产生强效抗肿瘤反应
将“冷肿瘤”变为“热肿瘤”
癌症免疫治疗已经为部分患者带来了革命性的改变,然而许多肿瘤仍能逃避这些强效药物。本研究探讨了某些癌症为何对现代免疫“检查点”药物产生抗性,并提出了一种更智能的三管齐下策略:唤醒机体防御、吸引精英杀伤性 T 细胞,并在肿瘤内部持续保持它们的活性。
为何现有免疫药物仍不够
大多数获批的免疫疗法针对免疫细胞上的单一路径制动器,如 PD-1/PD-L1 通路。新一类药物试图更进一步,同时阻断强烈抑制晚期癌症免疫的分子 TGF-β。其中一种药物 YM101 将 TGF-β 和 PD-L1 阻断合成在一株单抗中,并在小鼠中显示出潜力。但即便在遗传上相同的动物间,仍有部分肿瘤几乎没有缩小。通过比较对治疗敏感与耐受的肿瘤,研究者发现成功的治疗伴随强烈的“先天”免疫激活,特别是通过名为 STING 的通路,该通路感知异常 DNA 并触发类似抗病毒的警报信号。
加入第三个杠杆:STING 通路
研究团队怀疑先天免疫激活不足是缺失的一环,于是在多个小鼠肿瘤模型(包括通常难治的“冷”肿瘤)中,将 YM101 与口服类 STING 激动剂 MSA-2 联合使用。三重策略——激活 STING 加上 TGF-β 和 PD-L1 阻断——更有效地缩小肿瘤、延长生存,并常在再次挑战后保护小鼠免于肿瘤复发,表明产生了持久的免疫记忆。该组合优于更常规的将 STING 激动剂与仅 PD-L1 阻断配对,甚至在只阻断 TGF-β 的情况下也能增强 STING 激动剂疗法,表明 TGF-β 本身对 STING 驱动的免疫起到重要抑制作用。 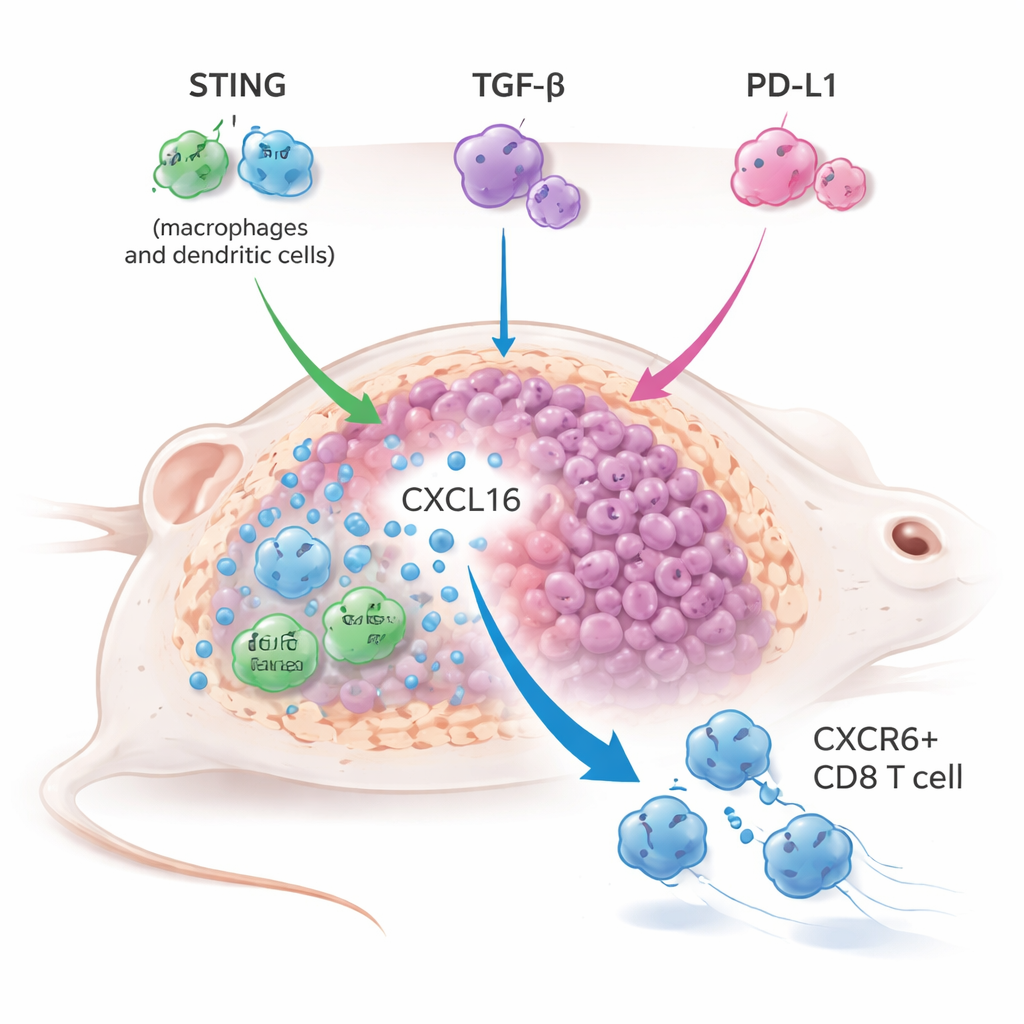
招募一支专门的杀手小队
为了解三重策略的工作机制,研究者对治疗后肿瘤进行了单细胞 RNA 测序和详尽的免疫分型。他们发现一种标记为受体 CXCR6 的特定杀伤性 T 细胞亚群显著扩增。这些 CXCR6+ CD8 T 细胞武器精良,表达高水平的颗粒酶、穿孔素和炎性分子,并显示出强烈的活化与增殖迹象。与此同时,肿瘤相关的巨噬细胞和树突状细胞上调产生一种名为 CXCL16 的趋化因子,CXCL16 与 CXCR6 结合,有助于将这些 T 细胞保留在肿瘤中。当 CXCL16–CXCR6 轴被破坏——无论是通过阻断 CXCL16 还是在 T 细胞中基因敲除 CXCR6——联合治疗的大部分抗肿瘤活性都会丧失,证明该轴对疗法成功至关重要。
该信号级联如何被开启
进一步探究表明,研究团队考察了 STING 激活与 TGF-β 阻断如何协同提升 CXCL16。在人和小鼠免疫细胞中,STING 激动剂显著增加了 CXCL16 和抗病毒细胞因子 IFN‑β,而额外加入的 TGF-β 则明显抑制两者。研究者展示了 STING 触发 I 型干扰素(IFN‑I)信号,激活转录因子 STAT1;STAT1 随后直接结合 CXCL16 基因的调控区并启动其表达。TGF-β 通过干扰 STING 信号传导中的关键步骤来破坏这一链条,可能涉及名为 HDAC4 的蛋白和活性氧(ROS),削弱 IRF3 的活化及下游的 IFN‑β 与 CXCL16 生成。阻断 TGF-β 则移除了这一刹车,使 STING 激动剂能够在髓系细胞中充分点燃 STAT1–CXCL16 通路,从而为 CXCR6+ T 细胞提供它们在肿瘤中停留并作战所需的信号。
构建单一精准药物
为使这一复杂疗法更实用且更聚焦于肿瘤,研究者构建了一种名为 Y101S 的单一“免疫刺激抗体偶联药”。该分子将双重阻断 TGF-β/PD-L1 的抗体与通过可裂解连接子连接的 STING 激动剂结合在一起。Y101S 定位于肿瘤中 PD-L1 阳性的髓系细胞,被内化后在这些细胞内释放 STING 药物。在多个小鼠肿瘤模型中,Y101S 的疗效与给予 YM101 加高剂量游离 STING 激动剂相当或更优,尽管其所携带的 STING 剂量仅为后者的一小部分。Y101S 提升了 CXCL16+ 的巨噬细胞和树突状细胞,扩增了 CXCR6+ CD8 T 细胞,诱导持久的免疫记忆,并将炎性信号集中于肿瘤而在健康器官中较少波及,在小鼠中表现出良好安全性。 
这对未来癌症治疗的意义
面向非专业读者的要点是,仅打开一到两个免疫开关可能不足以战胜肿瘤——尤其是当肿瘤主动抑制早期报警系统时。本研究表明,将 STING 激活与阻断 TGF-β 和 PD-L1 相结合,能够重塑肿瘤微环境,强有力地吸引并维持一类专门的杀伤性 T 细胞,并在前临床模型中实现更深更持久的应答。三重靶向的抗体-药物 Y101S 将这一策略浓缩到单一、可靶向的药物中,为针对目前对标准检查点药物耐药的肿瘤的下一代免疫疗法提供了路线图。
引用: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
关键词: 癌症免疫治疗, STING 通路, TGF-β 阻断, PD-L1 抗体, CXCL16 CXCR6 T 细胞