Clear Sky Science · zh
巨噬细胞诱导的一群表达 Fcer1g 的间充质细胞促进创伤诱导的纤维化
为何有些伤口留下持久瘢痕
我们大多数人身上都有刀伤、手术或事故留下的瘢痕,但为何有些伤口能平滑愈合而另一些却留下厚而隆起的痕迹,一直是个谜。该研究通过聚焦重建受损皮肤的细胞,深入探究这个问题。研究者发现了一类此前未被识别的造瘢痕细胞群,它们在损伤后早期被激活,受一种称为巨噬细胞的免疫细胞影响。理解这一隐秘协作关系可能为开发在高效闭合伤口的同时减少瘢痕的治疗策略提供线索。 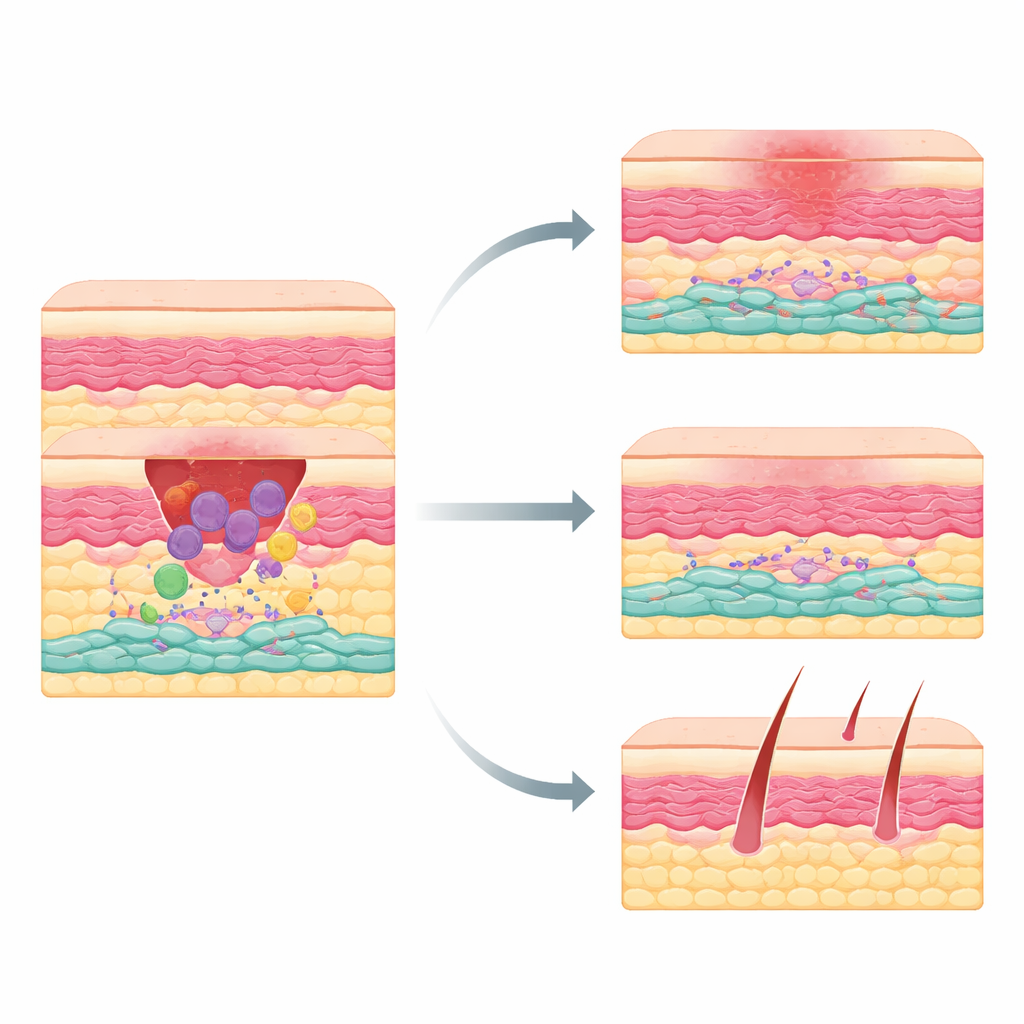
愈合皮肤中的隐性参与者
当皮肤受伤,机体经历一套协调的步骤:先是炎症以清除损伤,随后组织生长,最后重塑。巨噬细胞早期到达以清理碎屑并释放化学信号,召集其他细胞。响应者中有间充质细胞——类成纤维的“建筑者”,负责沉积胶原和其他支撑材料。这些建筑者并不完全相同:有些倾向再生,而有些则易于过度产生瘢痕组织。直到现在,科学家尚未明确成年皮肤中哪些间充质细胞亚群是导致厚重瘢痕的主要“元凶”。
默默为瘢痕铺路的免疫细胞
为探讨巨噬细胞如何影响瘢痕形成,研究团队使用了一种小鼠模型,可在伤后最初几天选择性地去除巨噬细胞。当这些早期巨噬细胞被清除时,伤口仍能闭合,但形成的瘢痕明显更小,胶原也不那么致密。单细胞 RNA 测序——一种逐细胞描绘基因活性的手段——显示大多数间充质亚群在失去巨噬细胞后并未改变。但有一个例外显著突出:一小部分 PDGFRα 阳性的间充质细胞激活了名为 Fcer1g 的基因。当巨噬细胞缺失时,这一亚群几乎消失,暗示巨噬细胞对该细胞的产生或维持是必要的。
增殖迅速、驱动瘢痕的细胞群
进一步的实验绘制了这些 Fcer1g 阳性间充质细胞出现的时空分布。在未受伤的皮肤中它们很稀少,但受伤后迅速扩增,先出现在伤口边缘,随后集中到伤口床,到第七天时它们构成了大多数 PDGFRα 阳性细胞。与其他间充质细胞相比,这些细胞分裂更快且迁移性低,表明局部增殖推动了它们的扩增。当研究者使用巧妙的遗传系统选择性消除同时表达 PDGFRα 与 Fcer1g 的细胞时,伤口闭合仍然正常——但瘢痕缩小了超过20%,胶原含量下降约30%,修复皮肤的胶原网络更接近未受伤的皮肤。被消除这些细胞的伤口中毛囊更多,提示愈合更具再生性。 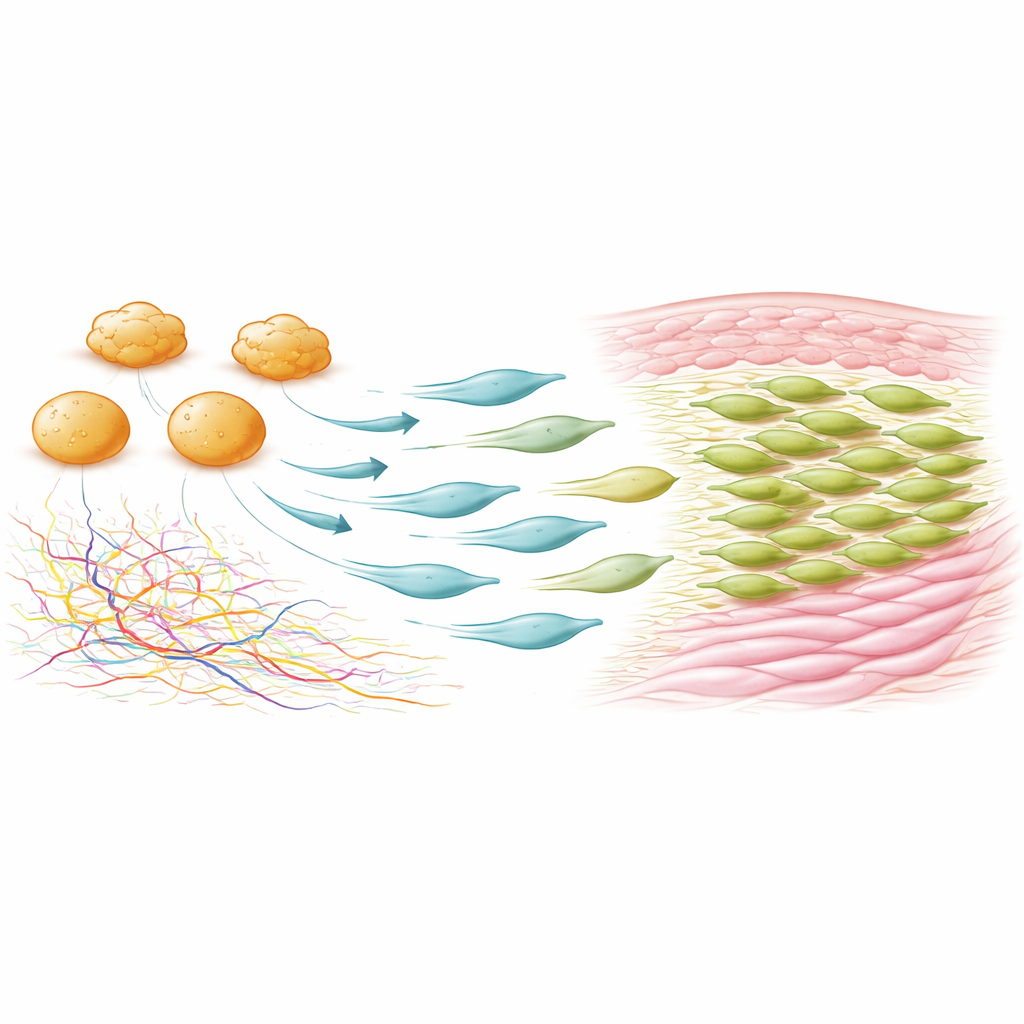
巨噬细胞如何向“建筑者”发出过度瘢痕的信号
为了解巨噬细胞如何触发这种易瘢痕化状态,团队分析了细胞类型之间可能的通讯路径。一个主要候选是纤连蛋白——一种在新鲜伤口临时基质中形成的“粘性”蛋白。早期伤口中的巨噬细胞是纤连蛋白的重要来源,当巨噬细胞被去除时其水平显著下降。在被工程化为缺失伤口相关纤连蛋白(EDA 形式)的小鼠中,Fcer1g 阳性间充质细胞大幅减少,瘢痕也更轻。在体外培养中,与巨噬细胞的直接接触足以将普通真皮成纤维细胞转换为 Fcer1g 阳性、PDGFRα 阳性的细胞,强调巨噬细胞能够直接诱导这一状态。
小鼠与人类间共享的瘢痕程序
为了检验这种细胞类型在人类中的意义,研究者重新分析了现有的人类皮肤伤口数据集,包含单细胞和整体组织分辨率的数据。他们发现在人类伤口中存在一个匹配的间充质亚群,表达 FCER1G 并具有相似的基因特征,约在损伤后一周达到顶峰——与小鼠中的时间一致。在一百多个包括正常皮肤、急性伤口、慢性伤口和隆起瘢痕的样本中,FCER1G 相关的基因程式清楚地区分了受伤或瘢痕组织与未受伤皮肤,并在伤后早期最为强烈。这种跨物种的相似性表明新定义的细胞状态是一个进化上保守的纤维化修复驱动因子。
朝着更温和、更少瘢痕的愈合方向
综上所述,研究结果揭示了一条此前被低估的事件链:早期到达的巨噬细胞在伤口富集纤连蛋白,纤连蛋白帮助将局部间充质细胞转化为增殖迅速的 FCER1G 阳性状态,而这一专门化亚群随后沉积过量胶原,形成瘢痕组织。因为在小鼠中去除这些细胞能在不延缓伤口闭合的情况下减少瘢痕,它们成为未来治疗的有吸引力的靶点。通过干预产生或维持该细胞状态的信号——例如调节巨噬细胞行为或改变纤连蛋白微环境——的药物或生物制剂,有望在未来帮助患者以更少、更不明显的瘢痕愈合皮肤损伤。
引用: Ma, X., Wang, E., Puviindran, V. et al. A macrophage-induced subpopulation of mesenchymal cells expressing Fcer1g contributes to wound-induced fibrosis. Nat Commun 17, 2686 (2026). https://doi.org/10.1038/s41467-026-69449-2
关键词: 伤口愈合, 皮肤纤维化, 巨噬细胞, 成纤维细胞, 瘢痕形成