Clear Sky Science · zh
RAS 结合域与富半胱氨酸域之间的正协同通过横向再结合调控 RAF 在膜上的结合动力学
为何这场微小的分子舞蹈至关重要
在细胞内部,关于生长、分裂和存活的生死决策常在细胞膜表面做出。RAF 蛋白是这些决定中的关键参与者,它帮助传递生长信号,并且在癌症中经常发生错误连接。本文以前所未有的动力学细节揭示了 RAF 如何附着于细胞膜、停留多久,以及为什么被 RAS 蛋白拥挤的斑块会使 RAF 比预期更长时间保持活性。
信号在细胞表面交汇
RAF 在称为 MAPK 的主要信号通路中发挥作用,该通路将外界线索(如生长因子)与基因活动的改变连接起来。在静止状态下,RAF 折叠成自抑制的构象并漂浮在细胞内部。只有当它遇到锚定在细胞膜内侧的小开关 RAS 时才被激活。RAS 必须处于“开启”状态并嵌入适当类型的脂质中,才能招募并激活 RAF。由于 RAF 分子相对于许多其他信号成分而言较为稀少,它们如何与膜结合并避免过早脱落,会强烈影响细胞对生长信号的响应强弱。
抓住膜的两只“手”
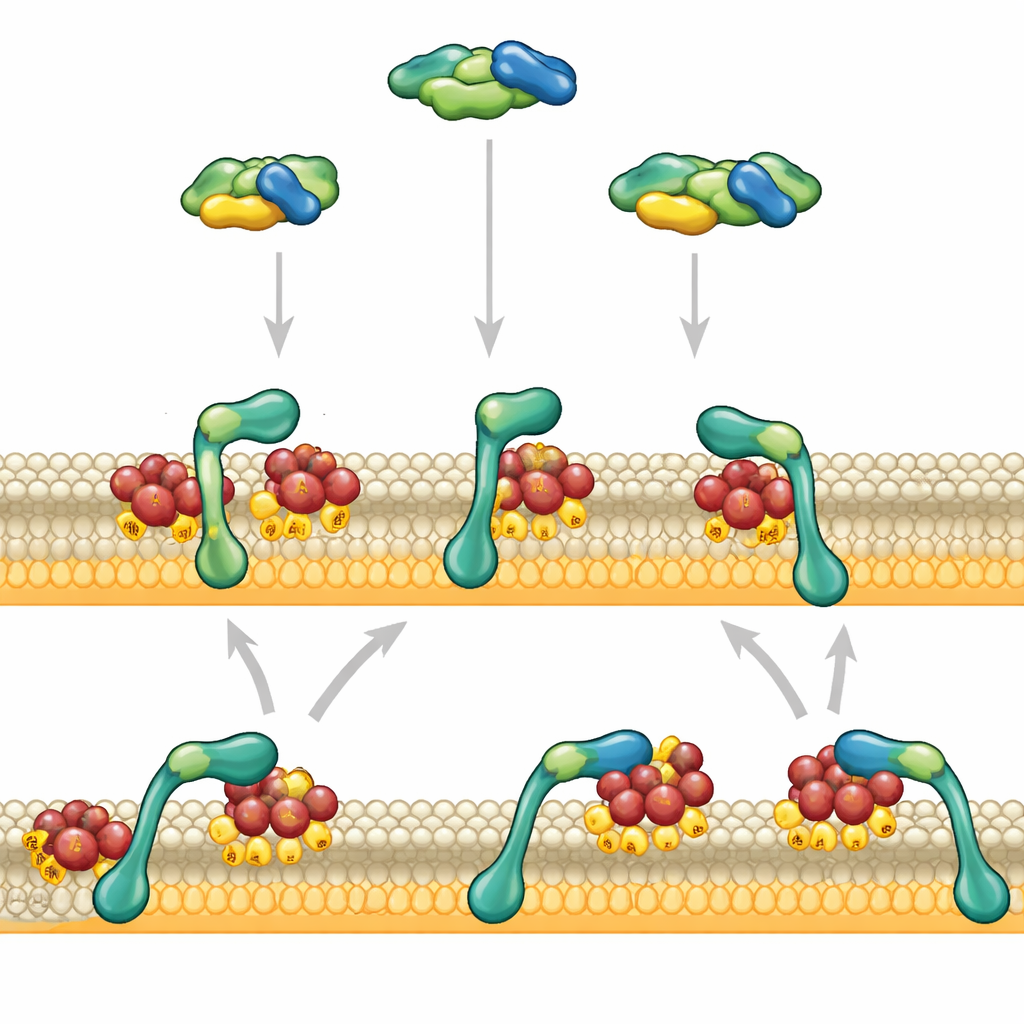
作者关注于 RAF 前端的两个区域:一个与 RAS 结合,另一个偏爱带负电的膜脂质。利用人工膜和纯化蛋白,他们用先进显微技术观察单个 RAF 片段与装饰了 RAS 的表面结合。当仅有 RAS 结合区域时,它短暂接触膜并在约一秒内脱落。仅有亲脂区时,几乎不附着。但当这两个区域连接在一起时,行为发生了显著改变:RAF 强烈附着并在膜上停留数十秒,尤其是在膜含有与真实细胞相似的多种带负电脂质时。
减慢离开过程的协同作用
这种显著变化并非因为 RAF 更快找到膜,而是因为它离开得更慢。首先,RAF 的 RAS 结合段识别被激活的 RAS 并将 RAF 停靠在膜上。只有在这第一次握手之后,亲脂区域才完全接触周围脂质,减缓 RAF 的侧向移动并更牢固地锚定它。第二次接触反过来稳定了最初的 RAS–RAF 相互作用,在线状蛋白–蛋白与蛋白–脂质接触之间形成正反馈环路。改变连接两区段的短连接子(linker)的实验表明,它们的精确空间配合至关重要:使连接子更柔软或更长会削弱 RAF 在膜上停留的能力。
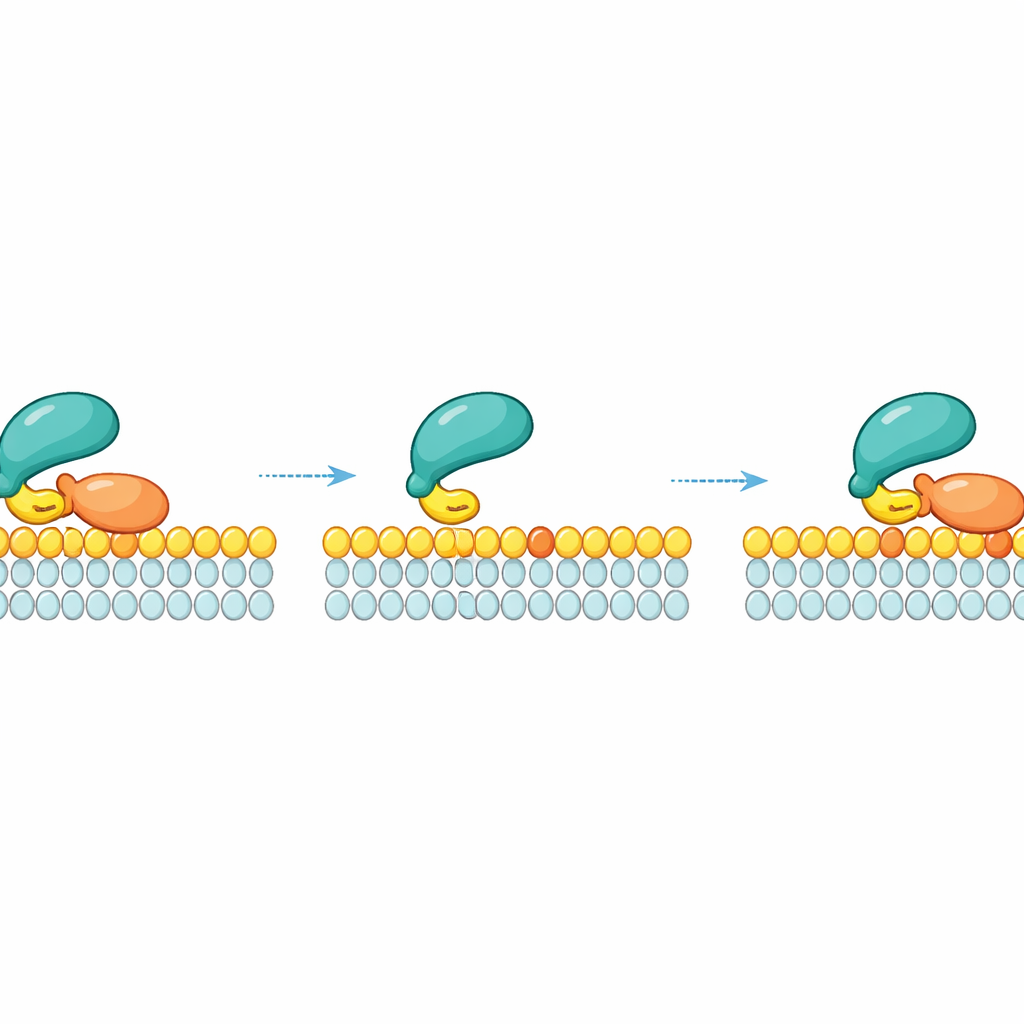
横向再结合:滑动而非脱落
这项工作的一项关键见解是,RAF 在放开某个特定 RAS 分子后并不会简单地脱落进入周围液相。相反,在 RAS 释放后,RAF 可以通过其较弱的脂质接触短暂地仍被系留在膜上并向侧向滑动。在这一瞬态状态中,它可以在同一膜片上“重新抓住”邻近的 RAS 分子。这种横向再结合形成了一个动力学安全网:在 RAS 局部密度高的情况下——例如 RAS 分子紧密聚集的纳米簇——RAF 有多次机会在漂离之前再次与 RAS 结合。测量和模拟显示,膜上活性 RAS 密度越高,RAF 由于反复的局部再结合而停留在膜上的时间越长。
从延长驻留到可靠激活
RAF 在膜上延长的停留时间具有重要后果。RAF 的激活不是单一事件,而是包含构象变化、抑制性修饰的移除以及两个 RAF 分子配对形成活性二聚体等多步序列。研究表明,只有在膜上停留足够久的 RAF 分子才能完成这一序列,这是一种“动力学校对”形式,帮助细胞避免因短暂、微弱的信号而意外激活。通过揭示 RAS 结合、脂质接触和横向再结合如何共同决定 RAF 在膜上的驻留时间,这项工作勾勒出一种普遍策略:细胞可利用膜上众多微弱相互作用来精细调控强效的信号通路。
引用: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
关键词: RAS, RAF 激酶, 细胞膜信号, 横向再结合, 动力学校对